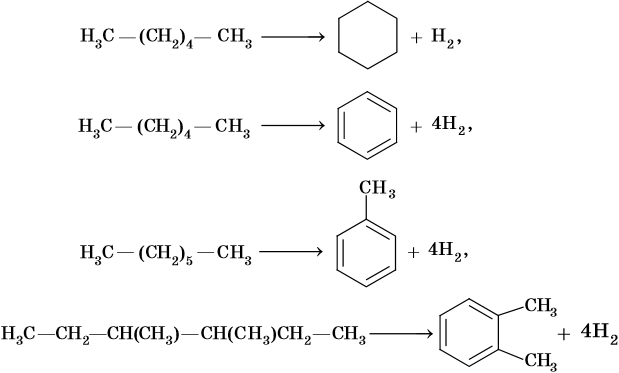
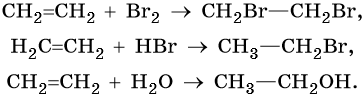
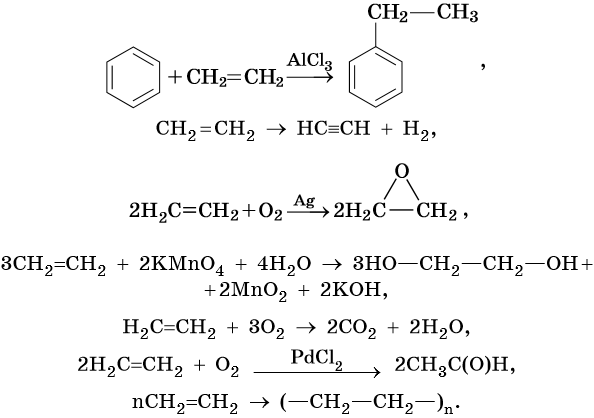
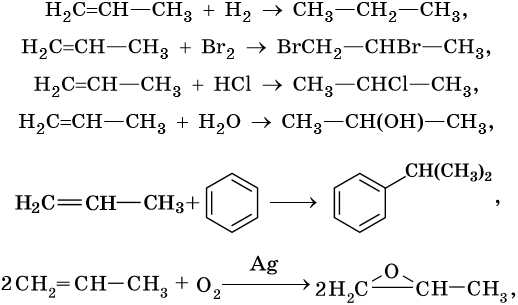
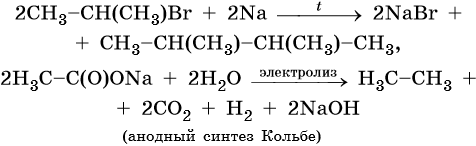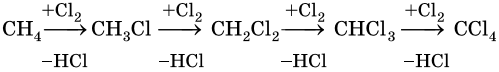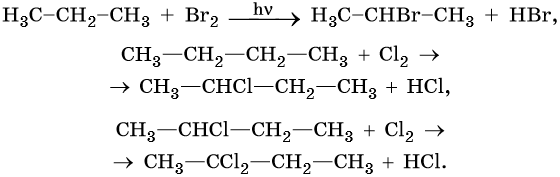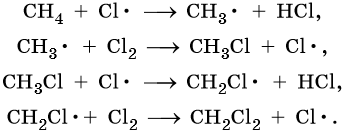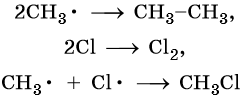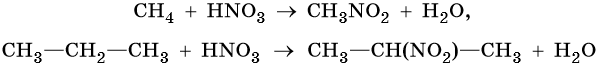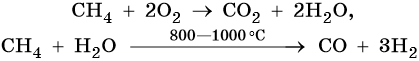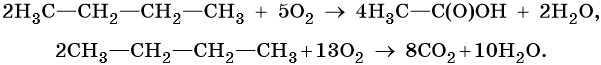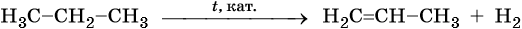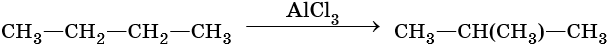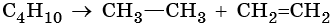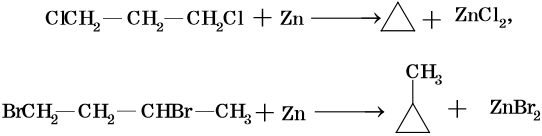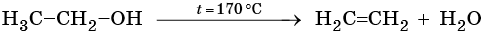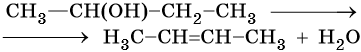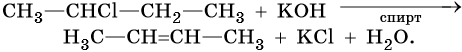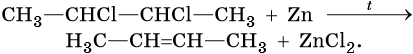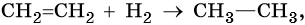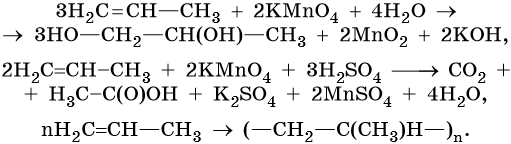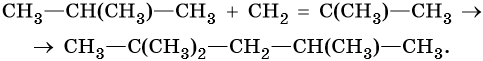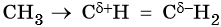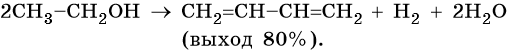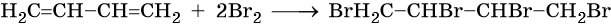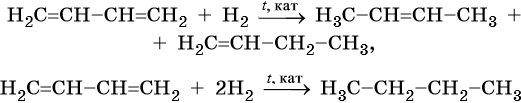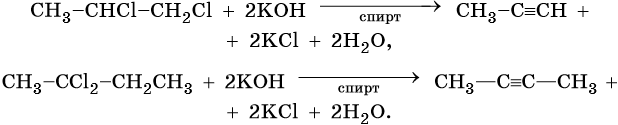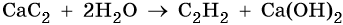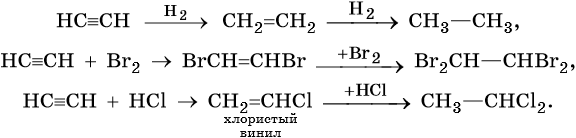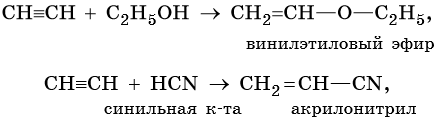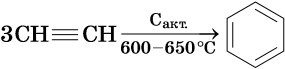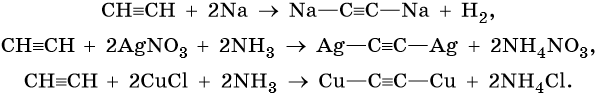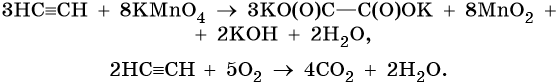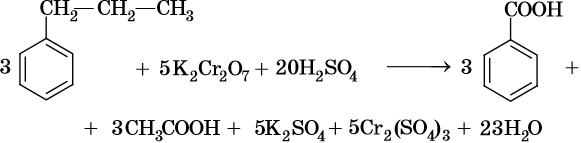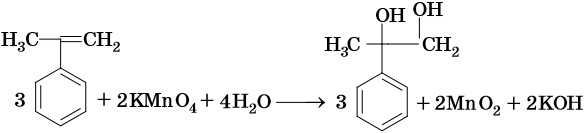алифатические углеводороды что это такое примеры
Алифатические углеводороды
Смотреть что такое «Алифатические углеводороды» в других словарях:
Жирные углеводороды, или алифатические углеводороды — ► aliphatics, aliphatic hydrocarbons Углеводороды с открытой цепью. Представлены следующими гомологическими рядами: ■ метановые углеводороды СnН2n+2 ■ олефиновые (этиленовые) углеводороды СnН2n с одной двойной связью ■ ацетиленовые углеводороды… … Нефтегазовая микроэнциклопедия
УГЛЕВОДОРОДЫ МЕТАНОВЫЕ (АЛКАНЫ, ПАРАФИНЫ) — насыщенные алифатические углеводороды (см. Соединения алифатические (жирные) общей формулы CnH2n+2. Низшие члены ряда У. м. до бутана (С4H10) включительно вещества газообразные при комнатной температуре, от С5Н12 до С15Н32 жидкости, от С16Н34… … Геологическая энциклопедия
углеводороды — см. алифатические углеводороды. карбоциклические углеводороды … Идеографический словарь русского языка
углеводороды — углеводороды: Смесь паров всех несгоревших и частично окисленных углеводородов топлива и масла, образующихся в процессах горения топлива и выпуска продуктов сгорания из цилиндра, обозначаемая символом СН. Источник … Словарь-справочник терминов нормативно-технической документации
Алифатические соединения — в органической химии соединения, не содержащие ароматических связей. Алифатические соединения могут представлять собой открытые цепи (ациклические соединения) или замкнутые (алициклические или циклоалифатические соединения).[1] Иногда к… … Википедия
УГЛЕВОДОРОДЫ — (УВ) органические соединения, молекулы которых состоят только из атомов углерода и водорода. Являются важнейшими компонентами нефти и природного газа, продуктов их переработки. Широко применяют как сырье в промышленности, как топливо и др.… … Российская энциклопедия по охране труда
Углеводороды — орг. соединения, состоящие только из углерода и водорода газообразные, жидкие и твердые в зависимости от молекулярного веса и от хим. структуры. Существуют У. с открытой цепью (см. Соединения алифатические (жирные) и циклические, Соединения… … Геологическая энциклопедия
Углеводороды суммарные — cmHn Углеводороды алифатические предельные С, С|0 (в пересчете на С), относящиеся к классу опасности IV Источник: ГОСТ Р 51206 98: Автотранспорт … Словарь-справочник терминов нормативно-технической документации
углеводороды — органические соединения, молекулы которых построены только из атомов углерода и водорода. Различают алифатические, или ациклические, углеводороды, в молекулах которых атомы углерода образуют линейные или разветвлённые «открытые» цепи (например,… … Энциклопедический словарь
алифатические соединения — (от греч. áleiphar, род. п. aléiphatos жир) (жирные соединения, ациклические соединения), органические соединения, в молекулах которых атомы углерода образуют «открытые» линейные (алифатические соединения нормального строения) или разветвлённые… … Энциклопедический словарь
Общая формула алканов
Представители данного класса характеризуются общей формулой СпН2п+2. К парафинам относят все соединения, имеющие открытую цепь, где атомы соединяются между собой простыми связями. В связи с тем, что при нормальных условиях алифатические углеводороды это малоактивные соединения, они получили свое название «парафины». Выясним некоторые особенности строения представителей данного класса, характер связи в молекулах, отрасли применения.
Краткая характеристика метана
Метан является при нормальных условиях газообразным веществом, не имеющим запаха и цвета. Образуется это соединение в природе при разложении без присутствия кислорода воздуха животных и растительных организмов. К примеру, он обнаружен в природном газе, поэтому в настоящее время в больших количествах используется в качестве топлива на производстве и в быту.
Какую химическую связь имеют эти углеводороды? Алифатические, предельные органические соединения являются ковалентными полярными молекулами.
Особенности гомологов метана
Помимо метана в природном газе и нефти содержатся другие углеводороды, которые имеют с ним сходное строение. Четыре первых представителя гомологического ряда парафинов находятся в газообразном агрегатном состоянии, имеют незначительную растворимость в воде.
По мере повышения величины относительной молекулярной массы наблюдается увеличение температур кипения и плавления СхНу. Между отдельными представителями ряда есть определенная разница СН2, которая называется гомологической разностью. Она является прямым подтверждением принадлежности соединения к этому органическому ряду.
Изомерия ряда
Для представителей ряда парафинов характерна изомерия углеродного скелета. Она объясняется возможностью пространственного вращения углеродного атома вокруг химических связей. Например, для соединения состава С4Н10 можно взять углеводород с прямым углеродным скелетом – бутаном. В качестве структурного изомера будет выступать 2-метилпропан, имеющий разветвленное строение.
Среди типичных химических свойств, характерных для парафинов, необходимо отметить реакции замещения. Насыщенность связей объясняет сложность протекания реакции, ее радикальный механизм. Для того чтобы получить галогенопроизводные алифатических углеводородов, необходимо провести реакцию галогенирования, протекающую при наличии УФ-излучения. Цепной характер этого взаимодействия наблюдается у всех представителей данного ряда. Образующиеся продукты называют галогенпроизводными. Они широко используются в химической промышленности в качестве органических растворителей.
Кроме того, все алифатические и ароматические углеводороды горят при наличии кислорода, образуя воду и углекислый газ. В зависимости от процентного содержания в молекуле углерода выделяется разное количество теплоты. Независимо от принадлежности к классу органических соединений, все процессы горения являются экзотермическими реакциями, используются в быту и промышленности.
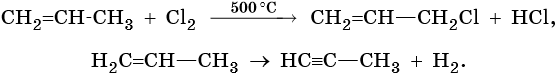
Практическое применение имеет и дегидрирование метана (отщепление водорода). В результате этого процесса образуется ацетилен, являющийся ценным химическим сырьем.
Применение алканов и хлорпроизводных алканов
Ненасыщенные углеводороды
Непредельные алифатические углеводороды – это представители ряда этилена и ацетилена. Проанализируем их основные свойства и применение. Для алкенов характерно наличие двойной связи, поэтому общая формула ряда имеет вид СпН2п.
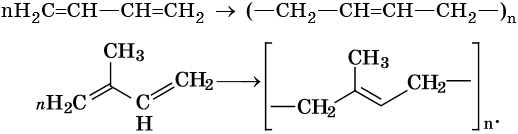
Учитывая непредельный характер этих веществ, можно отметить, что они вступают в реакции соединения: гидрирования, галогенирования, гидратации, гидрогалогенирования. Кроме того, представители ряда этилена способны к полимеризации. Именно эта их особенность делает представителей данного класса востребованными в современном химическом производстве. Полиэтилен и полипропилен – вещества, составляющие основу полимерной промышленности.
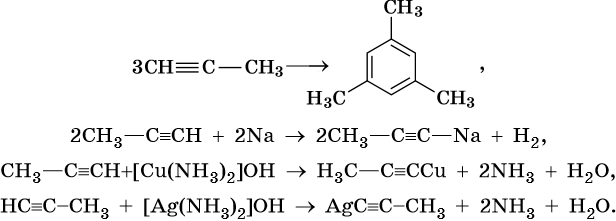
Ацетилен – первый представитель ряда, имеющего общую формулу СпН2п-2. Среди отличительных особенностей этих соединений можно выделить наличие тройной связи. Ее присутствие поясняет протекание реакций соединения с галогенами, водой, галогеноводородом, водородом. Если тройная связь в таких соединениях располагается в первом положении, то для алкинов характерна качественная реакция замещения с комплексной солью серебра. Именно эта способность является качественной реакцией на алкин, используется для обнаружения его в смеси с алкеном и алканом.
Ароматические углеводороды являются циклическими непредельными соединениями, поэтому не считаются алифатическими соединениями.
Заключение
Несмотря на различия по количественному составу, существующие у представителей предельных и непредельных алифатических соединений, они сходны по качественному показателю, содержат в молекулах углерод и водород. Отличия в количественном составе (различные общие формулы) у представителей насыщенных и ненасыщенных СхНу объясняют разницу в механизмах реакций получения различных продуктов.
Именно поэтому представители всех классов таких соединений вступают в реакции горения, образуя углекислый газ, воду, выделяя определенное количество тепловой энергии, что делает их востребованными в качестве топлива в быту и промышленности.
Алифатические углеводороды
Алифатические соединения в органической химии — соединения, не содержащие ароматических связей. Алифатические соединения могут представлять собой открытые цепи (ациклические соединения) или замкнутые (алициклические, или циклоалифатические соединения). [1] Иногда к алифатическим соединениям относят только ациклические, а алициклические выделяют в отдельный класс.
Содержание
Общая информация [ | ]
В органической химии соединения разделяются на два класса: ароматические — содержащие бензольное кольцо и другие подобные замкнутые структуры, и алифатические соединения, которые их не содержат. В алифатических соединениях атомы углерода могут соединяться между собой в прямые цепочки, разветвлённые цепочки или кольца (в этом случае они называются алициклические соединения). Атомы углерода могут соединяться одинарными связями (алканы), двойными связями (алкены), и тройными связями (алкины). Кроме водорода к углеродной цепочке могут присоединяться и другие элементы, наиболее распространённые — кислород, азот, сера, галогены.
Многие алифатические соединения горючи, что позволяет использовать их, в частности углеводороды (метан), спирты (этанол) в лабораторных горелках Бунзена и спиртовках; ацетилен используется в сварке.
Ациклические соединения [ | ]
Ациклические соединения — органические соединения, в молекулах которых отсутствуют циклы, и все атомы углерода соединены между собой в прямые или разветвлённые (открытые) цепи. Различают две основные группы ациклических соединений — насыщенные (предельные) углеводороды, у которых все атомы углерода связаны между собой только простыми связями (напр., гомологический ряд метана), и ненасыщенные (непредельные) углеводороды, у которых между атомами углерода имеются, кроме простых (одинарных) связей, также двойные, тройные связи (напр., ряды этилена, ацетилена).
Углеводороды
Углеводородами называют органические вещества, состоящие только из углерода и водорода. По составу их классифицируют на насыщенные и ненасыщенные, по строению — на алифатические, циклические и ароматические.
Алканами называют предельные алифатические углеводороды, отвечающие общей формуле CnH2n+2, в молекулах которых атомы углерода связаны между собой простой (одинарной) σ-связью.
Для алканов характерна изомерия углеродного скелета.
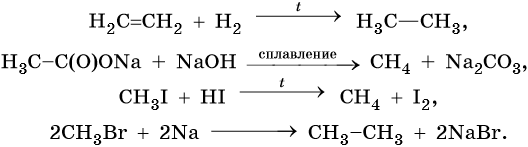
Способы получения алканов. Как правило, алканы получают из природного сырья, однако известно большое число синтетических методов их получения. Это реакции гидрирования алкенов и алкинов, декарбоксилирование натриевых или калиевых солей карбоновых кислот, восстановление йодалканов йодоводородом, реакция Вюрца:
Для алканов характерны реакции замещения, которые идут при нагревании или УФ-облучении. При этом происходит разрыв связи C—H с последующей заменой атома водорода на другой атом или группу атомов или же разрыв молекулы по связи C—С.
Большинство реакций алканов протекают по механизму радикального замещения SR. В этих реакциях реакционная способность атомов водорода убывает в ряду: третичные > вторичные > первичные.
Ниже приведены уравнения химических реакций, характерных для алканов.
1. Галогенирование:
Реакция идет на свету или при температуре 250— 400 °С.
Реакционная способность галогенов в этой реакции уменьшается в ряду F2 > Cl2 > Br2 > I2.
Реакции замещения в алканах протекают по радикальному механизму. При этом легче всего происходит замещение атома водорода, связанного с третичным углеродным атомом, затем — со вторичным и наконец — с первичным. Это объясняют значением энергии связей C–H, имеющих величину для первичной около 419 кДж/моль, вторичной — 393,6 кДж/моль и третичной — 372,6 кДж/ моль.
Наиболее широко известны реакции галогенирования алканов. Эти реакции идут на свету или при нагревании в присутствии инициаторов радикальных реакций. Рассмотрим механизм реакции на примере хлорирования метана.
На первой стадии этой реакции происходит распад молекулы хлора на два свободных радикала:
Cl:Cl → 2Cl• — зарождение, или инициирование цепи. Затем начинается рост цепи, связанный с взаимодействием свободного радикала с молекулой метана, что приводит к образованию новых радикалов:
Реакция заканчивается обрывом цепи, который наступает в результате взаимодействия между собой свободных радикалов:
Механизм реакции галогенирования был установлен академиком Н.Н. Семеновым.
2. Нитрование:
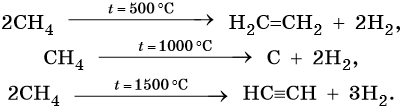
3. Термические превращения:
4. Окисление:
Каталитическое окисление бутана приводит к уксусной кислоте, а горение в кислороде — к углекислому газу и воде:
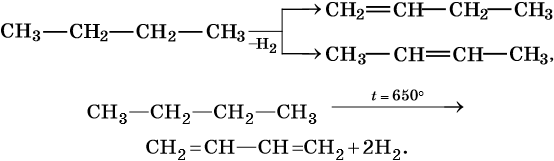
5. Дегидрирование:
Реакции дегидрирования (отщепления водорода) протекают по разным направлениям:
Реакции циклизации и ароматизации:
Последние две реакции идут при температурах 450–500 °С с использованием в качестве катализаторов оксидов хрома или алюминия.
Алициклическими называют углеводороды, которые содержат один или несколько циклов неароматического характера. По своим свойствам они схожи с соответствующими соединениями алифатического ряда. Термин «алициклические» означает «алифатические циклические» углеводороды. Несмотря на большое сходство между алифатическими и алициклическими соединениями, у последних имеются некоторые специфические свойства, обусловленные их циклической структурой. Общая формула гомологического ряда циклоалканов CnH2n.
Иногда циклоалканы называют нафтенами, т. к. производные циклопентана и циклогексана содержатся в некоторых сортах нефти.
Для гомологов и производных циклоалканов возможны следующие виды изомерии: изомерия, связанная с размером цикла, например, циклобутан является изомером метилциклопропана; изомерия положений заместителей в цикле; изомерия боковых цепей.
Циклопентан, циклогексан и их производные широко распространены в природе и составляют основную часть некоторых сортов нефти.
Низшие циклы синтезируют циклизацией дигалоидпроизводных, например:
Циклобутан и циклопентан получают циклизацией 1,4-дибромбутана и 1,5-дибромпентана под действием амальгамы лития. Циклогексан и его производные получают из нефти или гидрированием бензола и его производных.
Химические свойства циклоалканов во многом определяются размерами цикла. Наибольшей химической стойкостью обладают пяти- и шестичленные циклы. Циклопропан склонен к многочисленным реакциям раскрытия цикла.
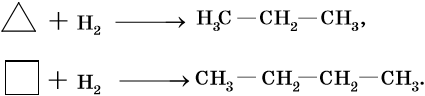
Гидрирование циклопропана и циклобутана идет над никелевым катализатором при температуре 80 и 120 °С соответственно. При этом образуются пропан и бутан.
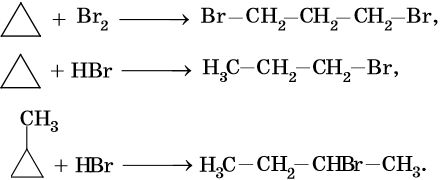
Циклопропановый цикл легко раскрывают при бромировании или гидробромировании, например:
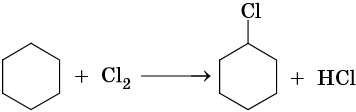
В аналогичных условиях углеводороды от циклобутана до циклогексана вступают в реакции замещения:
Циклопропан используют в качестве анестезирующего средства. Циклогексан используют как растворитель. Окислением циклогексана получают циклогексанол C6H11OH, циклогексанон C6H10O и адиптиновую кислоту HOOC(CH2)4COOH. Циклогексанон является промежуточным продуктом при получении полиамидного волокна — капрона.
Алкенами, или олефинами, называют алифатические непредельные углеводороды, молекулы которых отвечают общей формуле CnH2n и имеют в своем составе одну двойную связь C=C. Родоначальником этого класса органических соединений является этилен CH2=CH2. Для алкенов характерна изомерия углеродного скелета, изомерия положения кратной связи, геометрическая изомерия, а также межклассовая изомерия с циклоалканами.
Способы получения алкенов. Этилен, пропилен и бутилены выделяют из газов нефтепереработки, образующихся при термическом крекинге. Алкены также образуются в большом количестве при пиролизе нефти.
Промышленным способом получения алкенов является дегидрирование алканов на катализаторе (K2O—Cr2O3—Al2O3), при температуре 560—620 °C из н-бутана образуются изомерные бутены. Еще легче этот процесс идет в случае изобутана:
Алкены получают дегидратацией спиртов при катализе серной или фосфорной кислотами, оксидом алюминия или хлоридом цинка:
При дегидратации спиртов атом водорода наиболее легко отщепляется от наименее гидрогенизированного атома углерода (правило Зайцева):
Алкены образуются при действии на галоидные алкилы спиртовой или измельченной твердой щелочи. Эта реакция дегидрогалогенирования также идет по правилу Зайцева:
Алкены можно получить обработкой цинковым или магниевым порошком вицинальных дигалоидалканов:
Алкены вступают в реакции соединения по двойной связи. Они протекают по механизму электрофильного присоединения, или AE. Присоединение галогеноводородов и воды к несимметричным алкенам идет по правилу Марковникова: атом водорода присоединяется к наиболее гидрогенизированному, т. е. связанному с наибольшим числом водородных атомов, атому углерода. По легкости присоединения к алкенам галогеноводороды можно расположить в ряд: HI > HBr > HCl > HF.
Ниже приведены реакции алкенов на примере этена и пропена:
Реакция гидратации катализируется кислотами.
Реакция алкилирования протекает между алканами и алкенами в присутствии катализаторов:
Кроме реакций соединения для алкенов возможны отдельные реакции замещения, которые протекают по радикальному механизму, а также реакции разложения:
C позиции электронной теории правило Марковникова объясняют так: под действием метильного радикала в молекуле пропилена происходит перераспределение электронной плотности электронного облака π-связи в сторону крайнего ненасыщенного атома углерода, в результате чего на атомах углерода, связанных двойной связью, возникают частичные заряды:
При взаимодействии такой молекулы с галогенводородом присоединение положительно заряженного иона водорода идет по атому углерода с частичным отрицательным зарядом, а отрицательно заряженного галогенидиона — по атому углерода с частичным положительным зарядом.
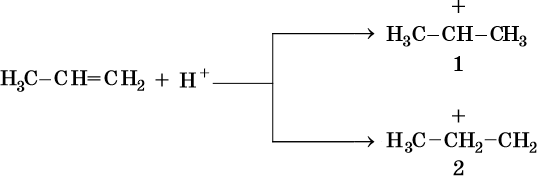
Другое объяснение правила Марковникова следующее. В результате электрофильного присоединения возможно образование двух различных карбокатионов: из-за положительного индуктивного эффекта двух метильных групп карбокатион 1 более стабилен, чем карбокатион 2.
Таким образом, реакции электрофильного присоединения по двойной связи идут в направлении образования наиболее устойчивого промежуточного карбокатиона.
Существуют исключения из правила Марковникова. Это присоединение бромоводорода к алкенам в присутствии органических пероксидов или кислорода. В этом случае из пропена и бромоводорода образуется 1-бромпропан (перекисный эффект Хараша). Подчеркнем особо: перекисный эффект имеет место только в случае реакции алкенов с бромоводородом. При присоединении к алкенам HCl, H2O, HI пероксиды не влияют на направление реакции, и она идет по правилу Марковникова.
Диеновыми углеводородами называют класс химических соединений, молекулы которых отвечают общей формуле CnH2n–2 и содержат в своем составе две двойные углерод-углеродные связи. Для диенов характерна изомерия углеродного скелета, изомерия положения кратных связей, геометрическая изомерия, а также межклассовая изомерия с ацетиленовыми углеводородами.
Способы получения диенов. Дивинил и изопрен выделяют из продуктов пиролиза нефти. Основным промышленным способом получения бутадиена-1,3 является дегидрирование бутан-бутеновой смеси над катализатором, состоящим из окиси хрома, нанесенной на окись алюминия.
Метод получения дивинила по С.В. Лебедеву заключается в дегидрировании-дегидратации этилового спирта над катализатором MoO — ZnO при 450 °С.
Диены, у которых двойные связи разделены более чем одной одинарной связью, в химическом отношении ведут себя подобно алкенам.
Диены, у которых двойные связи разделены одной простой связью, называют конъюгированными или сопряженными диенами. Эти соединения обладают специфическими химическими свойствами и имеют важное практическое значение.
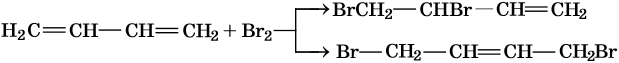
Своеобразные химические свойства диенов проявляются в реакциях присоединения, которые идут не только по одной или двум отдельным двойным связям (1,2-присоединение), но и по противоположным концам молекулы (1,4-присоединение). Выход продуктов 1,2- или 1,4-присоединения определяется характером реагента и условиями реакции.
При низких температурах преобладают продукты 1,2-присоединения, при повышенных — 1,4-присоединения.
Полное бромирование бутадиена-1,3 приведет к 1,2,3,4-тетрабромбутану:
Неполное гидрирование диенов приводит к смеси алкенов, а при полном образуются алканы:
Окисление сопряженных диенов, в зависимости от используемого окислителя и условий проведения реакции, может протекать с образованием различных кислородсодержащих соединений. При частичном окислении в нейтральной среде образуется щавелевая кислота, а действие перманганата калия в кислой среде при нагревании приведет к полному окислению диена до углекислого газа и воды.
Ацетиленовыми углеводородами, или алкинами, называют класс органических соединений, которые соответствуют общей формуле CnH2n–2 и содержат в молекуле одну тройную связь. Родоначальником этого класса соединений является ацетилен, или этин, — HC≡CH. Для ацетиленовых углеводородов характерна изомерия углеродной цепи, изомерия положения кратной связи и межклассовая изомерия с диеновыми углеводородами.
Общим методом получения алкинов является реакция спиртовых растворов щелочи с дигалоидалканами, содержащими два атома галогена при одном атоме углерода или двух соседних атомах углерода:
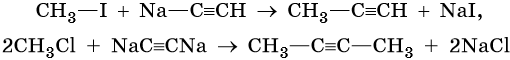
Производные ацетилена можно получить, действуя на его металлические производные галоидными алкилами:
Ацетилен получают действием воды на карбид кальция:
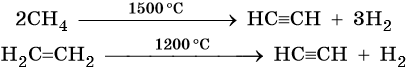
Кроме того, ацетилен получают термолизом метана и дегидрированием этилена:
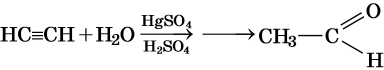
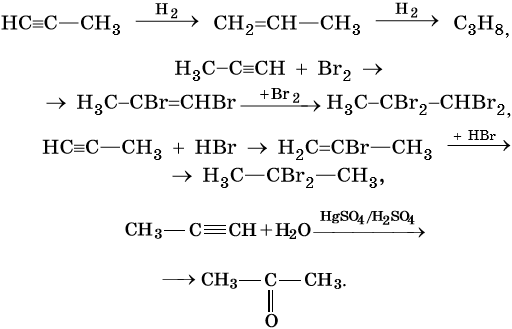
Для алкинов характерны реакции соединения и некоторые реакции замещения, которые приведены ниже на примере ацетилена и пропина. Катализаторами для реакций гидрирования алкинов являются Pd или PbO. Следует отметить, что реакции галогенирования и гидрогалогенирования алкинов идут медленнее, чем с алкенами.
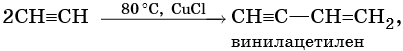
Реакции ди- и тримеризации:
Ароматическими углеводородами, или аренами, называют класс химических соединений, который отвечает общей формуле CnH2n–6 и имеет в своем составе устойчивую циклическую группировку (бензольное кольцо), обладающую особыми химическими свойствами.
Получение ароматических углеводородов. Основным природным источником ароматических углеводородов является нефть. Для получения гомологов бензола разработаны многочисленные синтетические методы.
Некоторые сорта нефти содержат достаточное количество ароматических углеводородов, которые выделяют простой перегонкой, пиролизом или каталитическим крекингом.
Синтетические методы — это ароматизация алканов, алкилирование бензола и т.д.
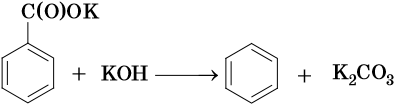
Так, например, бензол можно получить реакцией декарбоксилирования бензоата натрия или калия:
Для ароматических углеводородов наиболее характерны реакции замещения и некоторые реакции присоединения.
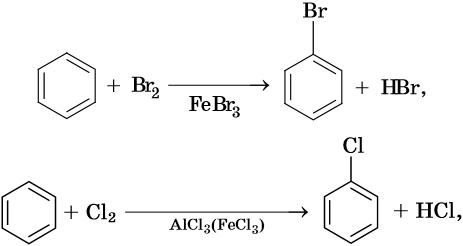
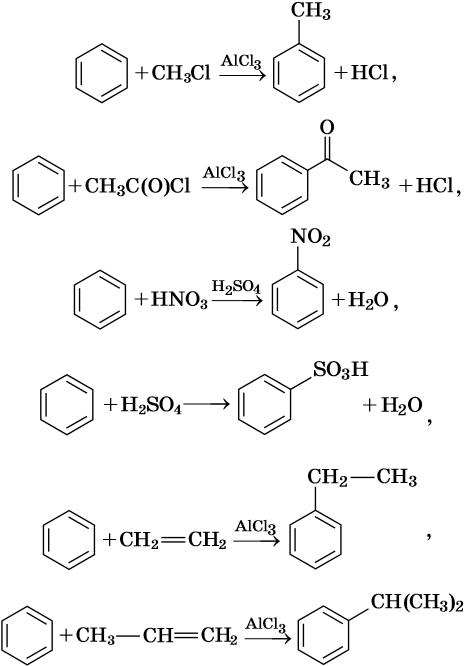
Как правило, все реакции замещения в ароматических соединениях протекают по электрофильному механизму SE. К таким реакциям относятся реакции алкилирования, галогенирования, нитрования, сульфирования, ацилирования и другие. Характерные химические свойства бензола:
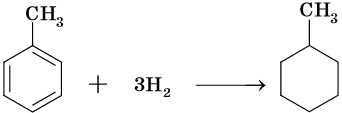
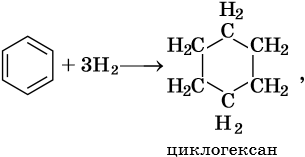
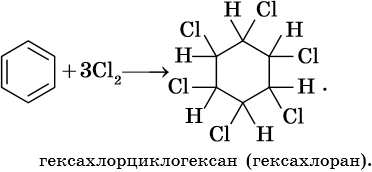
Гидрирование бензола до циклогексана идет при повышенной температуре, в присутствие катализатора (никель, платина), а хлорирование до гексахлорциклогексана — в газовой фазе под ультрафиолетовым излучением.
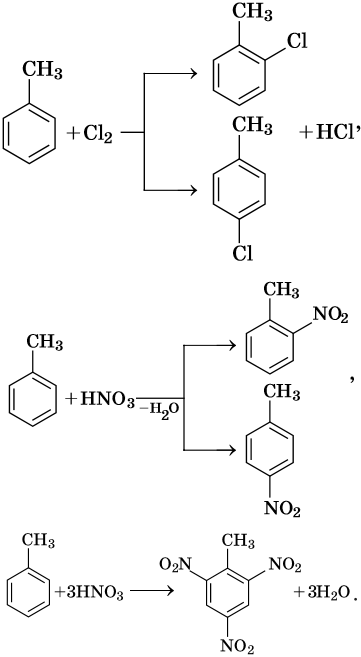
В молекуле толуола проявляется взаимное влияние метильного радикала на ароматическое ядро и ароматического ядра на метильный радикал. Толуол вступает в реакции замещения легче, чем бензол. При этом метильная группа ориентирует вхождение заместителей в орто— и пара-положения:
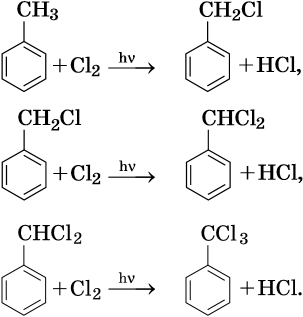
Галогенирование атомов водорода боковой цепи:
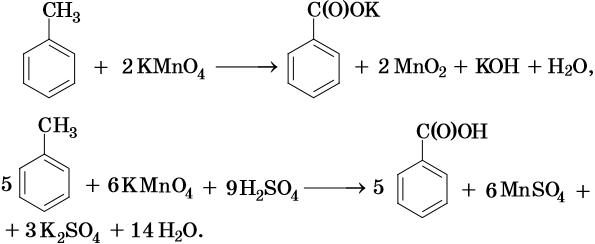
Окисление метильного радикала сильными окислителями, в зависимости от среды реакции, идет по разным направлениям:
В ходе реакций окисления алкилбензолов происходит окисление боковой цепи, а бензольное кольцо изменений не претерпевает:
Исключением являются третбутильные группы, связанные с бензольным кольцом — бензольное кольцо окисляется легче, чем эти группы.
При окислении жирноароматических соединений, содержащих ненасыщенные радикалы, соблюдаются общие закономерности, например:
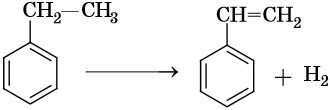
Этилбензол вступает в реакцию дегидрирования с образованием стирола:
Реакция протекает с высоким (92%) выходом при катализе оксидом цинка при температуре 600–650 °С.
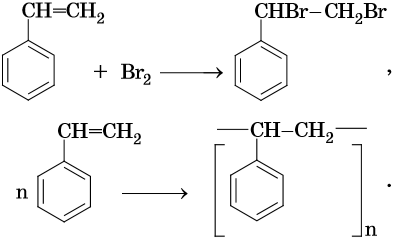
Стирол легко вступает в реакции по двойной связи и в реакции полимеризации и сополимеризации:
Свойства бутадиен-стирольных каучуков зависят от их состава. На их основе изготавливают шины и другие резинотехнические изделия.