антисеротониновое действие что это такое
Антисеротониновое действие что это такое
Серотонин (5-гидрокситриптамин, 5-НТ) синтезируется из L-триптофана. В качестве нейромедиатора серотонин участвует во множестве функций в ЦНС. Кроме того, он действует и как медиатор на периферии.
В кишечнике он действует а) как нейромедиатор в нервном сплетении мышечной оболочки кишечника и б) местно как гормон, выделяясь из энтерохромаффинных клеток (EC-клеток) кишечного эпителия. Серотонин усиливает перистальтику кишечника. Эти EC-клетки также могут влиять на ЦНС и косвенно на кровообращение.
Присутствие токсичных веществ (цитостатиков при химиотерапии рака) в кишечнике стимулирует эти клетки, в ответ они могут вызывать рвоту посредством выброса серотонина, стимулирующего афферентные нервные окончания блуждающего нерва. Более того, они выполняют функцию «серотониновой заправки» для тромбоцитов, т. к. сами тромбоциты не могут производить серотонин. Серотонин тромбоцитов участвует в тромбообразовании и свертывании крови.
Серотонин способен влиять на гладкую мускулатуру сосудов в двух противоположных направлениях. Он вызывает выход сосудорасширяющих посредников (NO, простациклина) в интактных эндотелиальных клетках, а при прямом действии на гладкую мускулатуру сосудов вызывает сосудосуживающий эффект.
а) Серотониновые рецепторы. В организме находится огромное количество различных подтипов серотониновых рецепторов. Из них в фармакологической терапии важны 5-НТ1, 5-НТ2 (оба с подтипами), 5-НТ3 и 5-НТ4. Большинство типов рецепторов связано с G-белками. Подтип 5-НТ3 представляет собой неселективный катионный канал (лйгандзависимый ионный канал).
б) Инактивация. Так же как биогенные амины норадреналин и дофамин, выделенный нейронами серотонин инактивируется путем нейронального обратного захвата с помощью специфического серотонинового транспортера (SERT) плазмолеммы. Неспецифический транспортер VMAT опосредует захват серотонина везикулами. Кроме того, серотонин может разрушаться внутри клеток МАО.
Средства, вызывающие эффекты серотонина
а) «Триптаны» при приступах мигрени. Суматриптан был первым препаратом, использованным для лечения мигрени; он действует как агонист 5-НТ1D рецепторов, а также 5-НТ1B-рецепторов. Он вызывает сужение внутричерепных сосудов, возможно, за счет угнетения выброса нейропептидов, которые запускают нейрогенное воспаление, либо за счет прямого действия на кровеносные сосуды. Чувство стеснения в груди может свидетельствовать о спазме коронарных сосудов.
Этот механизм действия доказал свою эффективность, и сейчас на рынке представлено много других триптанов.
б) Антидепрессанты. Многие представители этой группы веществ ингибируют обратный нейрональный захват 5-НТ. Флуоксетин — основной представитель СИОЗС.
в) Прочие. Сибутрамин, ингибитор обратного нейронального захвата серотонина и норадреналина,продается как средство против ожирения. Дулоксетин, который также угнетает обратный нейрональный захват норадреналина и серотонина, был предложен в качестве средства для лечения стрессового недержания мочи, а затем в качестве антидепрессанта.
г) Ингибиторы серотонина. «Сетроны» при рвоте, вызванной цитостатиками. Ондансетрон обладает выраженным противорвотным свойством после введения цитостатических препаратов. Это антагонист 5-НТ3-рецепторов, которые локализуются на афферентных волокнах блуждающего нерва в слизистой оболочке кишечника, а также в головном мозге, включая самое заднее поле. Цитотоксические вещества способны попасть в обе эти области, вызывая рвоту. Трописетрон и гранисетрон характеризуются аналогичным действием.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Блокаторы H1‑рецепторов: подсказки первостольнику
Показания, переносимость и особенности фармацевтического консультирования
Антагонисты гистаминовых рецепторов 1‑го типа, или блокаторы Н1‑рецепторов широко применяются в клинической практике более 70 лет. Их основным показанием и сегодня остаётся симптоматическое и базисное лечение одного из самых распространённых заболеваний, которым страдает практически каждый пятый человек в мире — аллергии. На сегодня в РФ зарегистрировано более 150 наименований Н 1 ‑блокаторов, которые представлены несколькими десятками действующих веществ. Знать их свойства, показания, противопоказания и лекарственные взаимодействия необходимо, чтобы консультировать клиентов с рецептами и запросами на противоаллергические препараты. Эта статья поможет нашим читателям «расставить по полочкам» представителей этой обширной фармакологической группы.
Два поколения Н1‑блокаторов
Один из важнейших медиаторов аллергических реакций — гистамин, высвобождаемый тучными клетками, — проявляет комплекс патологических эффектов после взаимодействия с гистаминовыми Н1‑рецепторами. Их стимуляция сопровождается расширением артериол, увеличением проницаемости сосудистой стенки, отёком тканей, местным покраснением кожи, зудом.
Блокаторы Н1‑рецепторов (Н1‑блокаторы) предотвращают эффекты гистамина, играя важную роль в лечении аллергических реакций — аллергического ринита, крапивницы и так далее. Следует отметить, что они блокируют действие гистамина на Н1‑рецепторы по механизму конкурентного ингибирования, и сродство их к рецепторам значительно ниже, чем у гистамина. Поэтому антигистаминные препараты не могут вытеснить гистамин, ранее связавшийся с рецептором, — они способны лишь блокировать незанятые или высвобождаемые рецепторы. В связи с этим Н1‑блокаторы рецепторов гистамина наиболее эффективны для предупреждения аллергических реакций немедленного типа, а при уже развившейся аллергии — для предотвращения воздействия новых «порций» гистамина.
На сегодняшний момент выделяют два поколения Н1‑блокаторов.
Препараты первого поколения — дифенгидрамин (димедрол), хлоропирамин, клемастин, диметиндена малеат, мебгидролин хорошо проникают в центральную нервную систему. Это связано с развитием сильного седативного эффекта наряду с противоаллергическим. Кроме того, средства этой подгруппы оказывают:
Препараты второго поколения (цетиризин, левоцетиризин, лоратадин, дезлоратадин, фексофенадин, эбастин) не проникают через гематоэнцефалический барьер и не оказывают седативного действия. Наряду с этим они способны селективно блокировать Н1‑рецепторы, быстро проявляя клинический эффект, сохраняющийся на протяжении 24 часов.
По данным исследований, эффективность препаратов первого и второго поколения в терапевтических дозах сопоставима, и основное их отличие — в переносимости. Несмотря на существенную разницу в профиле безопасности, представители обоих поколений занимают свою нишу и широко применяются в клинической практике.
«Седативные» Н1‑блокаторы
Антигистаминные препараты I поколения сегодня не входят в клинические рекомендации по лечению аллергических заболеваний, в частности, аллергического ринита. Их ведущее показание — купирование острых аллергических реакций в ситуациях, когда преобладают реакции ранней фазы аллергического воспаления, в частности:
Востребованность Н1‑блокаторов I поколения обусловлена рядом их достоинств по сравнению с более современными средствами. Так, седативные антигистаминные имеют парентеральные формы, которые целесообразно вводить при острых аллергических реакциях и оказании неотложной помощи, в то время как препараты II поколения выпускаются большей частью в пероральной форме.
Ещё одно существенное отличие препаратов I поколения — способность значительно уменьшать выраженность зуда на коже за счёт антихолинергического и седативного эффектов. Средства этой группы также применяют для симптоматического лечения ОРВИ — как местно, так и системно. Доказано, что они способствуют уменьшению зуда в носу, чихания, уменьшению назальной секреции.
Антигистаминные препараты I поколения также выделяются широким спектром фармакологической активности, позволяющим применять их не только при аллергических заболеваниях. Так, седативные Н1‑блокаторы назначают для потенцирования действия анальгетиков и местных анестетиков (в качестве компонента литических смесей); для лечения ожогов, порезов, укусов насекомых (диметиндена малеат); в составе комплексной терапии тревожных расстройств (гидроксизин); при бессоннице, а также ряде других патологических состояний, в частности, при вестибулярных расстройствах, рвоте (в том числе у беременных, включая 1 триместр), мигрени (доксиламин, дименгидринат) и др.
Нельзя не отметить, что Н1‑блокаторы I поколения имеют и существенный недостаток, связанный с не самым высоким профилем безопасности. Побочные эффекты этих препаратов вызваны их проникновением через гематоэнцефалический барьер: на фоне их приёма могут развиваться вялость, сонливость, нарушение координации, головокружение, снижение способности и концентрации внимания. У детей иногда развиваются парадоксальные реакции — перевозбуждение. Возможна тахифилаксия, побочные эффекты со стороны пищеварительной системы — дискомфорт в эпигастрии, тошнота, рвота, учащение стула.
О чем предупредить клиента?
Отпуская седативные антигистаминные по рецепту врача, важно сообщить о способности этих препаратов снижать концентрацию внимания и оказывать снотворный эффект, а также рекомендовать посетителю избегать вождения автомобиля во время лечения.
Н1‑блокаторы II поколения
Антигистаминные препараты II поколения были разработаны для устранения недостатков их предшественников. В отличие от последних, современные Н1‑блокаторы связываются и диссоциируют с Н1‑рецепторами медленно. Благодаря продолжительной связи с гистаминовыми рецепторами они способны обеспечивать длительный эффект, позволяющий применять их 1–2 раза в сутки. Доказано, что при регулярном приёме всех препаратов II поколения на протяжении месяца их терапевтический ответ не снижается, то есть тахифилаксия не развивается.
Неседативные антигистаминные препараты являются препаратами первой линии для лечения лёгких и умеренных форм аллергического ринита. Их уместно рекомендовать клиентам с незначительными симптомами аллергических заболеваний, а также аллергией средней тяжести.
Будучи сопоставимыми с первыми Н1‑блокаторами по антиаллергической активности, представители II поколения не проявляют седативный эффект и многие другие неблагоприятные реакции, что связано с их высокой селективностью и значительно меньшей способностью проникать через гематоэнцефалический барьер.
К преимуществам следует отнести длительное действие, возможность однократного применения в сутки, а также отсутствие тахифилаксии.
Несмотря на очевидные преимущества, некоторые препараты II поколения обладают редким, но серьёзным побочным эффектом, — способность вызывать нарушения сердечного ритма в виде удлинения интервала QT, развития желудочковой аритмии (типа «пируэт»), атриовентрикулярной блокады и блокады ножек пучка Гиса. Подобные аритмии проявляются эпизодами головокружения, обмороками, однако нередко могут протекать бессимптомно.
Кардиотоксический эффект носит дозозависимый характер. При применении препаратов в терапевтических дозах аритмогенные свойства практически не проявляются. Это связано с тем, что большинство антигистаминных II поколения представляют собой пролекарства, которые почти не определяются в кровотоке из‑за быстрой биотрансформации с образованием активных и длительно действующих метаболитов. Следует отметить, что биотрансформация антигистаминных препаратов II поколения происходит с помощью изофермента системы цитохрома Р450, активность которого могут угнетать некоторые препараты, в частности, кетоконазол, итраконазол, флуоксетин, флавоноид, содержащийся в соке грейпфрута и ряд других.
При передозировке, повышении концентрации пролекарства в крови, а также состояниях, при которых снижается скорость биотрансформации препарата (например, циррозе печени, одновременном назначении с препаратами, угнетающими активность изофермента системы цитохрома Р450), выраженность кардиотоксического эффекта Н1‑блокаторов II поколения увеличивается. Дополнительными факторами риска служат уже существующий синдром удлинённого интервала QT, одновременный приём препаратов с аритмогенной активностью, электролитные нарушения.
В то же время при правильном применении, соблюдении режима дозирования и противопоказаний антигистаминные II поколения хорошо переносятся и могут считаться безопасными для лечения аллергических заболеваний.
Аритмогенных свойств лишены лоратадин — как сам препарат, так и его активный метаболит, — а также дезлоратадин и фексофенадин. Кстати, последние не метаболизируются с участием изофермента системы цитохрома Р450 и не вступают в лекарственные взаимодействия с препаратами, угнетающими его активность.
О чём предупредить клиента?
Отпуская препараты этой подгруппы, важно напомнить о необходимости соблюдения режима дозирования во избежание развития побочных эффектов, в частности, кардиотоксического действия.
Кроме того, уместно обратить внимание клиента на то, что антигистаминные II поколения не следует принимать одновременно с препаратами, которые конкурируют с ними за печёночный метаболизм (кетоконазол, итраконазол, ранитидин, флуоксетин и другие).
Топические антигистаминные препараты
Местные Н1‑блокаторы позволяют обеспечить достижение достаточно высоких локальных концентраций препарата при низкой дозе и быстрое начало терапевтического эффекта — как правило, уже через 15 минут после введения. При этом количество побочных эффектов значимо уменьшается за счёт снижения системной концентрации препаратов.
Сегодня зарегистрирован ряд топических препаратов, в частности, антигистаминный препарат I поколения дифенгидрамин (применяется наружно) и представители II поколения Н1‑блокаторов левокабастин, азеластин и антазолин в комбинации с нафазолином (выпускаются в форме назального спрея и глазных капель).
По выраженности антигистаминного эффекта назальный спрей сравним с эффектом пероральных Н1‑блокаторов. Биодоступность при интраназальном введении выше, чем при использовании в форме глазных капель, что, скорее всего, связано с большей поверхностью всасывания и частичным проглатыванием препарата при орошении слизистой оболочки носа.
Левокабастин и азеластин можно рекомендовать посетителям с лёгким течением аллергического ринита и конъюнктивита, а при регулярном применении — для профилактики сезонной формы заболевания.
Рецептор медиатора настроения
Психонейрофармакологическая важность серотонина столь высока, что его химическая формула даже является узнаваемым образом во многих субкультурах, — в частности, её часто татуируют или исполняют в виде ювелирных украшений.
Автор
Редакторы
В 1948 году, когда был открыт серотонин (5-гидрокситриптамин), никто и не думал, что он настолько важен для физиологии человека [1]. Серотониновая система является молекулярной мишенью при лечении мигреней, депрессии, тревожных расстройств, тошноты, слизистого колита и других заболеваний, своим разнообразием подчёркивающих многогранность роли серотонина в работе всего организма [2]. В некотором смысле серотонин можно считать нейрофармакологической основой духовной сферы человека, — в частности, религиозного и мистического чувств [3].
G-белоксопряженные рецепторы
«Биомолекула» довольно скрупулёзно следит за структурной биологией G-белоксопряженных рецепторов, а поэтому об их роли и истории изучения можно весьма подробно прочесть на нашем сайте:
Рецепторы серотонина являются интегральными белками мембран нейронов, и экспериментальное их изучение затруднено необходимостью использовать мембраномоделирующие среды, позволяющие сохранить природное строение этих белков. Дополнительной хитростью является генно-инженерное встраивание вместо одной из цитоплазматических петель рецептора термостабильного бактериального белка апоцитохрома b562RIL (BRIL), стабилизирующего пространственную структуру и позволяющего формироваться кристаллам дифракционного качества, но не меняющего активность рецепторов. Структуру β2-адренорецептора получили в 2007 году тем же способом, только там вставляли не апоцитохром, а лизоцим, что произвело революцию в структурной биологии GPCR-рецепторов [7].
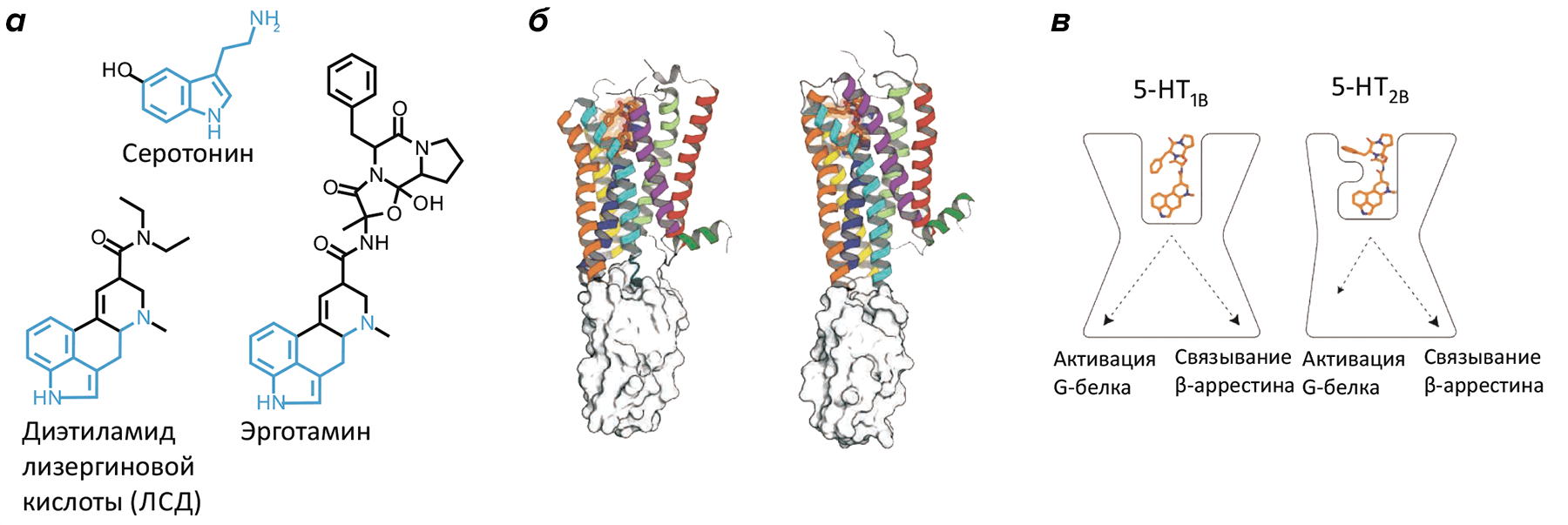
Рисунок 1. Молекулярные основы передачи сигнала серотониновыми рецепторами. а — Природный (серотонин) и синтетические (эрготамин, ЛСД) лиганды с общим индоламинным ядром. б — Кристаллографические структуры рецепторов 5-HT1B (слева) и 5-HT2B (справа) в комплексе с эрготамином. в — Эрготамин стабилизирует различные конформации у двух серотониновых рецепторов, объясняя биохимически установленный феномен «смещенной» рецепторной передачи.
Как уже было сказано, все серотониновые рецепторы, кроме 5-HT3, относятся к GPCR-рецепторам и передают сигнал в клетку либо через активацию G-белка, либо связываясь с альтернативным белком-эффектором — β-аррестином [8]. Близкое химическое строение серотонина и других биологически активных аминов — дофамина и адреналина, — а также высокое сходство рецепторов этих молекул объясняют, почему вещества, действующие на серотониновые рецепторы, могут действовать также на рецепторы других моноаминов, приводя к побочным эффектам. В частности, высокие дозы эрготамина и родственных ему алкалоидов, действующих, предположительно, через 5-HT1B и 5-HT1D рецепторы, могут запустить также α-адренорецепторы, что вызовет нежелательное сосудосуживающее действие [9]. Ещё один довольно скандальный пример связан с фенфлурамином — регулятором аппетита амфетаминовой природы, действующим через рецептор 5-HT2B и приводящим к появлению пороков сердца. Изъятие этого препарата с рынка в 1997 году было крупнейшим в истории фармакологии.
Уже известны примеры рационального дизайна лекарств [10], специфическим образом нацеленных на 5-HT1 рецепторы и используемых для избавления от мигреней [11], однако определение пространственной структуры серотониновых рецепторов обещает сделать процесс этого дизайна более прямолинейным. Детальное сравнение строения двух рецепторов позволит создать вещества, селективно действующие на рецептор 5-HT1B и лишённые кардиотоксического побочного действия, оказываемого через рецепторы 5-HT2B.
На первый взгляд, строение обоих серотониновых рецепторов такое же, как и у наиболее известного представителя семейства А рецепторов GPCR — родопсина [12]. Среднеквадратичное отклонение, используемое в качестве меры схожести двух пространственных структур, здесь составляет всего лишь 2.3–2.7 Å для 80% Cα-атомов любого из серотониновых рецепторов и родопсина, подчеркивая высочайшую похожесть пространственной организации этих рецепторов при совершенно различных функциях и аминокислотных последовательностях. Однако наличие структур двух рецепторов, определенных в комплексе с одним и тем же лигандом, открывает замечательную возможность для тонкого сравнения рецепторных сайтов распознавания и областей, в которых рецептор взаимодействует с цитоплазматическими белками-эффекторами. В частности, удалось объяснить, почему в случае 5-HT2B рецептора эрготамин активирует β-аррестин, в то время как для 5-HT1B это G-белок. Выявление таких тонких молекулярных нюансов — пока редкость для молекулярной биологии, но именно они позволяют предсказывать сигнальный ответ, вызываемый тем или иным соединением, а значит, и прогнозировать и создавать требуемое лекарственное воздействие.
Семейство рецепторов серотонина иногда сравнивают с двуликим Янусом, поскольку одни из них могут быть опасны (5-HT2B называют рецептором смерти из-за его кардиотоксического действия), а другие доставляют нам удовольствие. Например, при поедании шоколада в наш организм поступают предшественник серотонина аминокислота триптофан и некоторые другие серотониноподобные моноамины, и серотониновые рецепторы позволяют нам почувствовать это удовольствие [13].
Знание о деталях строения серотониновых рецепторов, несомненно, найдет применение в дизайне некардиотоксичных аналогов серотонина, которые будут выполнять свою целебную функцию и окажутся приятны во всех отношениях — как шоколад.
По материалам рубрики Perspectives журнала Science [14].
Селективные ингибиторы обратного захвата серотонина
В настоящее время для лечения депрессии, особенно в амбулаторной практике, используются относительно новые антидепрессанты — селективные ингибиторы обратного захвата серотонина (СИОЗС), обладающие значительно меньшим количеством побочных эффектов, чем трициклические антидепрессанты, за счет избирательного влияния на обмен серотонина (избирательное торможение захвата
СИОЗС представлены такими препаратами как: флуоксетин (прозак), флувоксамин (феварин), сертралин (золофт, стимулотон, асентра), пароксетин (паксил, рексетин), ципрамил (циталопрам, ципралекс).
В отличие от ТЦА, особенностью действия серотонинергических антидепрессантов является их селективное влияние на серотонинергическую систему, первоначально выявленное в лабораторных исследованиях (Wong D.,с соавт., 1974; Fuller R., с соавт., 1977). Эффективность терапии депрессии СИОЗС, составляет не менее 65% (Mulrow D., с соавт., 2000)
Благодаря сродству этих препаратов и их активных метаболитов к серотониновым рецепторам происходит блокада обратного захвата серотонина на уровне пресинаптических окончаний, тем самым повышается концентрация медиатора в синаптической щели, что в свою очередь ведет к снижению синтеза и кругооборота серотонина (Stark Р., с соавт., 1985).
Избирательное, но неспецифическое для определенного подтипа рецепторов (Stahl S., 1993) действие СИОЗС не всегда повышает эффективность лечения, особенно если речь идет о терапии пациентов, страдающих тяжелой депрессией (Anderson I., Tomenson B., 1994; Burce M., Prescorn S., 1995).
Препараты группы СИОЗС имеют совершенно разную химическую структуру и отличаются друг от друга по фармакокинетическим параметрам, дозировкам и профилям побочных эффектов. Селективность подавления обратного захвата уменьшает количество побочных эффектов, улучшает переносимость и снижает частоту отказов от приема препаратов в сравнении с ТЦА (Anderson I., Tomenson T., 1994).
Таблица Сравнительная характеристика СИОЗС по интенсивность эффекта антидепрессанта
Препарат
Интенсивность эффекта
Пароксетин (рексетин, паксил)
Сертралин (стимулотон, золофт)
Ципрамил (ципралекс, циталопрам, целекса)
Флуоксетин (прозак, флуксал)
Необходимо подчеркнуть относительную безопасность СИОЗС (меньшее число и выраженность побочных явлений) и большую комфортность лечения (возможность проведения терапии в амбулаторных условиях).
СИОЗС отличаются также низкой токсичностью (риск смертельного исхода при отравлении или передозировке практически равен нулю), а также возможностью использования препаратов этой группы у пациентов с противопоказаниям к применению ТЦА (нарушение сердечного ритма, затруднение мочеиспускания в связи с гипертрофией предстательной железы, закрытоугольная глаукома) (Машковский М.Д., 1997).
Следует отметить, что в литературе отмечены случаи центральных и переферических побочных эффектов в процессе лечения СИОЗС (Baldessarini R., 1989).
Эти препараты являются более дорогостоящими антидепрессантами, по сравнению с другими препаратами, использующимися для лечения депрессии.
Большинство из селективных ингибиторов обратного захвата серотонина (СИОЗС) являются пролонгами и используются в фиксированных дозах. Фармакокинетика различных представителей группы СИОЗС имеет свои особенности в зависимости от возраста пациентов и соматической отягощенности. Так период полураспада флувоксамина несколько увеличивается у пожилых пациентов и больных с патологией печени (Raghoebar M., Roseboom H., 1988). На продолжительность периода полураспада сертралина также оказывает влияние возраст (Warrington S.1988), а на эффекте флуоксетина достаточно существенно отражаются функциональные возможности печени (Bergstrom M., Lemberg L, с соавт., 1988).
Клинические испытания СИОЗС продемонстрировали, что они, как и ТЦА, являются эффективным средством при большинстве депрессивных состояний, включающих в себя тревогу, нарушения сна, психомоторную ажитацию и заторможенность. ( Levine S. с соавт., 1987, Dunlop S. с соавт., 1990, Claghorn J., 1992, Kiev A., 1992).
Таблица Сравнительная оценка дополнительного терапевтического эффекта СИОЗС
Препарат
Терапевтический эффект
Флуоксетин (прозак, флуксал)
Сертралин (стимулотон, золофт)
Анксиолитический, антифобический, вегетативно-стабилизирующий
Ципрамил (ципралекс, циталопрам)
Пароксетин (паксил, рексетин)
Показаниями к применению СИОЗС являются выраженные и средне тяжелые депрессии (типа простой) с нерезко выраженной тревогой и беспокойством (Pujynski S., с соавт., 1994;. Pujynski S, 1996). Кроме того СИОЗС могут использоваться для терапии личностных расстройств, включающих в себя реакции гнева и проявления импульсивности.
В медицинской литературе подчеркивается чувствительность витальных нарушений к действию этих антидепрессантов (Laakmann G. с соавт. 1988).
В ряде исследований описано, что пациенты, у которых в структуре синдрома преобладала тоска, демонстрировали хороший терапевтический ответ при применении СИОЗС (Reimherr F. et al., 1990, Tignol G. et al., 1992; Мосолов С.Н., Калинин В.В., 1994).
Учитывая, хорошую переносимость данных лекарственных средств их рекомендуют применять в пожилом возрасте.
В течение последних лет были проведены исследования, в которых представлены сравнительные оценки СИОЗС с ТЦА. Большинство авторов отмечает, что активность новых соединений сравнима с традиционными препаратами (Guelri J.. с соавт., 1983; Shaw D., с соавт., 1986; Hale A. С соавт., 1991, Fontaine R. С соавт., 1991). При сравнении СИОЗС с ТЦА, традиционно применяющемся при лечении тревожно-депрессивных состояний, как правило, указывается, что различия в эффективности исследуемых препаратов по способности купировать чувство тревоги не являются статистически значимыми (Feighner J., 1985, Laws D. С соавт., 1990, Авруцкий Г.Я., Мосолов С.Н., 1991, Doogan D., Gailard V., 1992).
По мнению многих авторов СИОЗС в ряде случаев эффективны тогда, когда применение ТЦА оказалось нерезультативным (Weilburg J.B. с соавт., 1989, Beasley C.M. с соавт.. 1990; Иванов М.В. с совт., 1991; Бовин Р.Я. с соавт., 1992; Серебрякова Т.В., 1994; Бовин Р.Я., с соавт. 1995). По данным Beasley C., Sayler M. (1990), пациенты, резистентные к ТЦА, в случаев оказываются чувствительными к новым препаратам.
Необходимо подчеркнуть большую по сравнению с ТЦА безопасность СИОЗС (меньшее число и выраженность побочных явлений), большую комфортность лечения (возможность проведения терапии в амбулаторных условиях) (Boyer W. Feighner J., 1996).
При приеме ТЦА 30% пациентов вынуждены отказаться от лечения из-за выраженности побочных действий, тогда как в случае назначения новых препаратов только у 15% больных приходится прерывать прием лекарств (Cooper G., 1988).
S. Montgomery, S. Kasper (1995) показали, что частота прекращения приема препаратов из-за побочных эффектов была у 14 % пациентов, лечившихся СИОЗС и у 19 % — ТЦА. Преимущество антидепрессантов второго поколения особенно важно в ходе длительной терапии (Medavar Т. с соавт., 1987).
Р.Я. Бовин (1989) указывает на возрастающую опасность возникновения суицида на ранних этапах терапии ТЦА. В то время как, в большинстве исследований, посвященым СИОЗС, авторы обращают внимание на высокую направленность этих препаратов против суицида (Fava M. с соавт., 1991; Cohn D. с соавт., 1990; Sacchetti E. с соавт., 1991).
Помимо терапии депрессии, все чаще предпринимаются попытки длительного применения антидепрессантов (флуоксетин, сертралин) для профилактики ее рецидивов.
Cohn G.N. с соавт., (1990), учитывая хорошую переносимость СА, рекомендуют их использование в геронтопсихиатрии.
Не существует единого мнения относительно скорости наступления эффекта при применении СИОЗС. По мнению иностранных авторов, клинический эффект СИОЗС обнаруживается позднее, чем ТЦА (Roose S, с соавт. 1994). В то же время отечественные ученые указывают, что у CИОЗС регистрируется тенденция к более быстрому наступлению терапевтического эффекта, по сравнению с другими антидепрессантами (Авруцкий Г.Я, Мосолов С.Н, 1991).
В группе СИОЗС различные препараты отличаются по силе действия на рецепторы и уровню селективности. Причем селективность и сила действия не совпадают. Было установлено, что пароксетин является более мощным ингибитором серотонинового возврата, в то время как циталопрам — более селективным. Различия в селективности и мощности действия на рецепторы определяют не только особенности терапевтического эффекта того или иного препарата, но и наличие побочных эффектов (Thopas D., с соавт., 1987; Hyttel G., 1993).
При прочих равных условиях рецидивы депрессии чаще отмечаются после терапии флуоксетином, чем пароксетином и после лечения циталопрамом, чем сертралином; при почти равном количестве рецидивов на фоне лечения сертралином и пароксетином.
Поскольку флувоксамин и пароксетин обладают выраженным седативным и противотревожным эффектом, то они по спектру своей активности приближаются к таким препаратам, как амитриптилин или доксепин. Большинство других препаратов, особенно флуоксетин, больше напоминают профиль имипрамина, так как обладают растормаживающим эффектом и могут усилить проявления тревоги и беспокойства (Caley Ch.,1993; Pujynski S., с соавт., 1994; Montgomery S., Johnson F., 1995). В отечественной литературе также имеются указания на низкую эффективность, а иногда даже усиление тревоги при применении СИОЗС у больных с тревожной депрессией (Калинин В.В., Костюкова Е.Г., 1994, Лопухов И.Г. с соавт., 1994, Мосолов С.Н., с соавт., 1994).
Вследствие растормаживающего эффекта подобные препараты не следует применять при тревоге, беспокойстве, двигательной расторможенности, бессоннице, суицидальных мыслях и тенденциях. По мнению, S. Pujynski (1996) относительным противопоказанием к применению СИОЗС являются психотические формы депрессии. Однако, Feighner J., Bouer W (1988), напротив, отмечают позитивный эффект данных препаратов даже при психотическом варианте депрессии.
Наиболее частыми побочными эффектами при приеме ингибиторов серотонина считаются гастроинтестинальные расстройства: тошнота и рвота, запоры и жидкий стул. У ряда больных отмечается снижение веса.
Таблица Сравнительная характеристика СИОЗС по выраженности побочных эффектов