аспирация желудочного содержимого что это такое
Синдром Мендельсона – острый аспирационный пневмонит, развивающийся вследствие попадания в дыхательные пути кислого желудочного содержимого. Чаще возникает как осложнение анестезиологического пособия. Клиника синдрома Мендельсона разворачивается в считанные часы и включает в себя одышку, лихорадку, дыхательную недостаточность, присоединение бактериальной пневмонии. Синдром диагностируется на основании клинических, аускультативных и рентгенологических данных. Первая помощь предполагает аспирацию содержимого из дыхательных путей, устранение бронхоспазма, перевод больного на ИВЛ, проведение лечебной бронхоскопии. В дальнейшем назначается противоотечная и антибактериальная терапия.
МКБ-10
Общие сведения
Причины
Единственно возможной причиной синдрома Мендельсона является аспирация содержимого желудка, повреждающее действие которого связано с высокой кислотностью химуса. Агрессивный субстрат приводит к сильнейшему химическому ожогу и отеку слизистой дыхательных путей, быстрому разрушению эпителия бронхиол и альвеол и пропотеванию транссудата в альвеолы. Это сопровождается развитием некардиогенного отека легких и респираторного дистресс-синдрома (гипоксемической формы дыхательной недостаточности).
В некоторых случаях вместе с желудочным соком в дыхательные пути могут попадать частички непереваренной пищи, вызывающие механическую закупорку бронхов среднего калибра (асфиктическая форма дыхательной недостаточности). В обоих случаях в конечном итоге развивается бронхиальная обструкция.
Для возникновения клиники синдрома Мендельсона достаточно попадания в респираторный пути даже небольшого объема (20-30 мл) желудочного сока с низким рН. Самые тяжелые повреждения отмечаются при аспирации большого количества кислого содержимого (>0,4 мл/кг), имеющего рН 5.
Факторами, предрасполагающими к аспирации или регургитации содержимого желудка и развитию синдрома Мендельсона, выступают нарушения сознания, обусловленные общим наркозом, алкогольным или наркотическим опьянением, действием седативных препаратов, ЧМТ, комой. Чаще всего синдром Мендельсона возникает как осложнение экстренных хирургических вмешательств (чаще брюшнополостных операций и кесарева сечения), когда не уделяется должного внимания подготовке ЖКТ. Дополнительными факторами риска служат повышение внутрибрюшного давления (у беременных в III триместре, больных ожирением, при парезах кишечника), заболевания ЖКТ (язвенная болезнь желудка и ДПК, эзофагит, гастрит, расширение пищевода, дивертикул пищевода, грыжа пищеводного отверстия диафрагмы).
Симптомы
Клиника синдрома Мендельсона разворачивается очень быстро, в течение нескольких часов. Патологические изменения проходят три фазы: острого ларинго- и бронхиолоспазма, частичного купирования бронхиолоспазма и нарастания острой дыхательной недостаточности.
В первые минуты после аспирации в результате рефлекторного сужения бронхиол возникает кашель, экспираторная одышка, цианоз кожных покровов, тахикардия, снижение АД. Первую фазу синдрома Мендельсона нередко ошибочно принимают за приступ бронхиальной астмы. В легких прослушиваются разнокалиберные влажные и свистящие хрипы; происходит повышение ЦВД, набухание вен шеи. Быстро развивается ОДН I—III ст.; уже на первом этапе возможен летальный исход от асфиксии.
Вторая фаза знаменуется самопроизвольным частичным расширением бронхиол и некоторым клиническим улучшением. Состояние больного временно стабилизируется: уменьшается одышка, снижается давление. Примерно через 48 часов наступает третья фаза синдрома Мендельсона. В этот период быстро нарастают явления бронхиолита и пневмонита, что вызывает новое ухудшение состояния больного и прогрессирование дыхательной недостаточности. Присоединяются бактериальные осложнения – развивается аспирационная пневмония (лихорадка, кашель с мокротой, лейкоцитоз). Летальный исход обычно наступает от отека легких.
Диагностика
Для клинической диагностики синдрома Мендельсона имеет значение характерная триада симптомов (тахипноэ, тахикардия, цианоз), а также невозможность устранить гипоксемию даже при подаче чистого кислорода (данный признак указывает на шунтирование венозной крови). При мониторинге газового состава крови отмечается снижение РаО2 до 35-45 мм рт. ст. Аускультативная картина характеризуется наличием множественных свистящих хрипов (в нижних отделах – крипитирующих хрипов).
При проведении бронхоскопии выявляется отек и гиперемия слизистой, наличие в просвете бронхов аспирированной жидкости, нередко с комочками пищи. На рентгенограммах легких видны очаги гиповентиляции, диффузное затемнение легочных полей («шоковое легкое»). С присоединением вторичной бактериальной пневмонии появляются очаги инфильтрации.
Лечение синдрома Мендельсона
Неотложная помощь должна быть оказана больному сразу после установления факта аспирации желудочного содержимого. В первую очередь необходимо немедленно удалить аспират из полости рта и дыхательных путей с помощью электроотсоса. После этого производится интубация трахеи и перевод больного на ИВЛ в режиме гипервентиляции с ингаляцией 100% кислорода. В дальнейшем выполняется зондовое опорожнение желудка и санационная бронхоскопия: для бронхоальвеолярного лаважа используется стерильный физраствор. Лечение больного синдромом Мендельсона осуществляется в ОРИТ совместно анестезиологами-реаниматологами и пульмонологами.
С целью ликвидации бронхиолоспазма вводится атропин, эуфиллин, преднизолон или дексаметазон, орципреналин. Обязательно производится перкуссионный массаж грудной клетки. Для нейтрализации высокой кислотности осуществляются щелочные ингаляции раствора гидрокарбоната натрия. Проводится инфузия электролитных растворов, глюкозы, свежезамороженной плазмы, альбумина; стимуляция диуреза. Антибиотикотерапия показана для профилактики и лечения аспирационной пневмонии. Экстубация производится после восстановления спонтанного дыхания и самостоятельной способности поддержания адекватного газообмена.
Прогноз и профилактика
Летальные исходы при возникновении синдрома Мендельсона наблюдаются в 60% случаев, а в акушерской практике – более чем в 70% случаев. Чтобы предотвратить это грозное осложнение, перед экстренными операциями необходимо эвакуировать желудочное содержимое с помощью зонда (за исключением тех случаев, когда это противопоказано – например, при желудочном кровотечении). Перед плановыми операциями запрещается прием пищи и жидкости за 10-12 часов до вмешательства, при необходимости назначается прием антацидов, Н2-блокаторов и прокинетиков. Во избежание синдрома Мендельсона необходимо соблюдение правильного алгоритма анестезиологического пособия во время экстренных хирургических вмешательств.
Аспирация желудочного содержимого что это такое
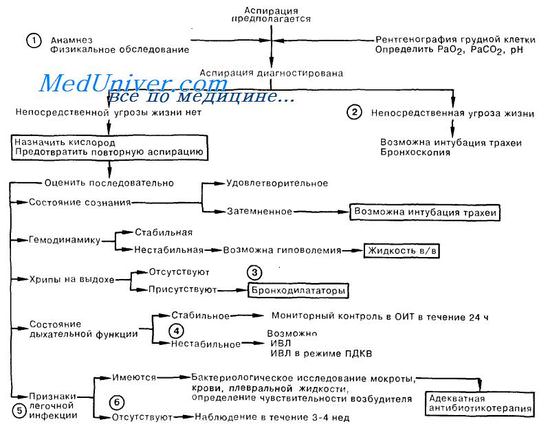
1. К первой группе факторов, предрасполагающих к аспирации желудочного содержимого, относятся: увеличение объема желудочного содержимого или повышение внутрижелудочного давления, наблюдаемые при обструкции привратника или асците. Факторы, которые позволяют осуществиться забросу содержимого желудка в глотку или провоцирующие этот заброс, составляют вторую группу. К ним относят грыжу пищеводного отверстия диафрагмы, а также введение гастроскопа. К третьей группе предрасполагающих факторов относят нарушения функции глотки, наступающие, например, при коме или местной анестезии и допускающие движение жидкого желудочного содержимого в трахею. Профилактика имеет решающее значение; среди больных с подтвержденной аспирацией смертность достигает 50%. Важное значение имеет тщательный уход за больными из группы риска по этому осложнению. Например, введение назогастрального зонда не всегда позволяет эффективно эвакуировать желудочное содержимое, но может привести к функциональной несостоятельности желудочно-пищеводного соединения, а также спровоцировать рвоту во время его введения. При уходе за больным, находящимся в полукоматозном состоянии, ему следует придать положение «лежа на боку» со слегка опущенной головой, а при кормлении через назогастральный зонд голову больного следует приподнять. При нарушении глотания или затемненном сознании иногда приходится вводить больному эндотрахеальную трубку с манжеткой.
2. Нередко диагноз аспирации ставится лишь методом исключения, но иногда медицинский персонал может быть свидетелем рвоты и аспирации у больного; или желчь обнаруживают в виде примеси в трахеальном секрете либо в виде пятен на подушке. Аспирация может представлять немедленную угрозу жизни больного; в зависимости от характера и количества может вызвать частичную или полную обструкцию дыхательных путей; признаками асфиксии в этом случае являются судорожные дыхательные движения либо апноэ. Решающую роль играет немедленное удаление аспирата всеми доступными методами; следует прочистить пальцем глотку, опустить голову больного, отсосать аспират или провести прямую ларингоскопию.
3. Другим вариантом клинической картины является прогрессирующее угнетение дыхания и гемодинамическая нестабильность в течение первых 24 ч. Химическое раздражение кислым желудочным содержимым, особенно если его рН менее 2,5, приводит к воспалению и отеку. Часто встречающаяся гиповолемия требует коррекции в/в введением жидкости. Хрипы на выдохе указывают на обструкцию бронхов малого калибра. Лечение заключается во введении эуфиллина в/в и орципреналина ингаляционно. Противоречивые данные об эффективности кортикостероидов при аспирации не позволяют рекомендовать их широкое применение; однако показанием к введению стероидов может быть резистентное к другим препаратам повышение сопротивления дыхательных путей.
4. Признаками продолжающегося нарушения дыхательной функции являются тахипноэ, тахикардия, гипоксия при вдыхании воздуха с высоким содержанием кислорода, а также часто встречающееся после аспирации чередование гиперкапнии с гипокапнией. В ходе лечения может возникнуть необходимость эндотра-хеальной интубации и проведения ИВЛ.
5. Непосредственной реакцией на аспирацию, даже в отсутствие инфекции, может быть лихорадка, лейкоцитоз и увеличение вязкости мокроты. Легочная инфекция развивается чаще всего в течение 2—14 сут после аспирации. Распознать инфекционное осложнение позволяют ухудшение состояния больного, обнаружение возбудителя в мазке или при бактериологическом исследовании мокроты и/или крови, плевральной жидкости, а также появление или увеличение ранее имевшихся инфильтратов на рентгенограмме грудной клетки. Выбор антибиотика зависит от возбудителя, обнаруженного при бактериологическом исследовании, и определения его чувствительности. При необходимости антибиотикотерапию начинают до получения результатов таким образом, чтобы назначаемые препараты были эффективны в отношении внебольничных анаэробных возбудителей, а также действовали на возбудителей больничных аэробных и анаэробных инфекций. Профилактически антибиотики назначают лишь в случае аспирации желудочных масс, заведомо содержащих большое количество патогенных микроорганизмов.
6. Даже в отсутствие признаков инфекции при аспирации желудочного содержимого наблюдение за больным должно продолжаться 3—4 нед, так как иногда легочная инфекция может развиться более чем через 2 нед после эпизода аспирации.
ГИПЕРЕРГИЧЕСКИЙ АСПИРАЦИОННЫЙ ПНЕВМОНИТ
(СИНДРОМ МЕНДЕЛЬСОНА)
Е. М. Шифман
ГУЗ «Республиканский перинатальный центр»
МЗ СРС Республики Карелия, г. Петрозаводск
В любой клинике может встретиться такое сочетание, когда нарушены гортанные рефлексы и на этом фоне возникает рвота или регургитация. Чем же так сильно провинилось акушерство?
Желудочно-кишечный тракт: изменения во время беременности и родов. При беременности пассаж пищи по пищеварительному тракту замедлен, кислотность желудочного сока повышена и возникновение регургитации облегчено. Почему это происходит?
Во-первых, желудок и кишечник значительно смещены кверху из-за увеличения матки, а ось желудка сменяет свое вертикальное положение на горизонтальное. Это приводит к увеличению внутрижелудочного давления и к изменению пищеводно-желудочного угла, что может закончиться несостоятельностью антрального сфинктера.
Во-вторых, тонус и моторика желудка снижены так, что эвакуация желудочного содержимого замедлена. Беременность сопровождается прогрессирующим ростом прогестерона. Кроме благотворного влияния на кровообращение и функцию внешнего дыхания, есть и отрицательная сторона этих влияний. Под влиянием прогестерона замедляется моторика пищеварительного тракта и уменьшается тонус гастроэзофагеального сфинктера.
В-третьих, секреторная активность желудка (кислота, хлориды и ферменты) к концу беременности повышается.
Роды сами по себе не вызывают изменений функции желудка. Однако боль и беспокойство, положение тела и множество лекарств, принимаемых перорально и вводимых парентерально, могут, сочетаясь, вызвать задержку эвакуации желудочного содержимого.
Изменение функций желудка особенно заметно во время и после родов. В родах и ближайшем послеродовом периоде время опорожнения желудка несколько удлиняется. Время эвакуации желудочного содержимого возвращается к норме уже спустя 18 часов после родоразрешения. Кислотность и остаточный желудочный объем уже спустя 8 часов после родов не отличается от таковых показателей у небеременных женщин. Таким образом, при лечении родильницы в раннем послеродовом периоде ее нужно рассматривать как пациентку «с полным желудком».
Патологическая физиология. История вопроса весьма поучительна. Впервые аспирацию желудочным содержимым как причину смерти привел Джеймс Янг Симпсон в 1848 г. Первое описание аспирации при анестезии появилось только в 1853 г.
Опыт медицины Первой мировой войны также внес свою лепту в исследование этой проблемы. В 1920 г. M. C. Winternitz et al. отметили сходство между повреждением легочной ткани при вдыхании боевых отравляющих веществ и при развитии пневмонии [8]. Эту малоизвестную работу, как ни странно, можно считать первым экспериментальным исследованием механизмов повреждения легких при аспирационных пневмонитах. Следующее описание аспирационных осложнений, но уже более осмысленное, приводит C. C. Hall, который в 1940 г. ввел термин «химический пневмонит». Начало систематическому изучению аспирационного гиперергического пневмонита положило исследование нью-йоркского акушера Кёртиса Мендельсона, который фактически подтвердил, что тяжесть повреждения легких уменьшается при нейтрализации желудочного содержимого. Он анализировал 66 случаев аспирации при общей анестезии в родах и показал, что при этом возникают два вида аспирационных осложнений.
Первый, более редкий, – обструкция дыхательных путей пищевыми массами – не отличается от аспирационных синдромов в других разделах медицины.
Второй, получивший название синдрома Мендельсона, – астмоподобная реакция на кислое желудочное содержимое – аспирационный гиперергический пневмонит.
К. Мендельсон предложил также основные принципы профилактики аспирационных пневмонитов, которые впоследствии превратились в незыблемые акушерские догмы. Для пользы дальнейших рассуждений мы позволим себе процитировать первоисточник [28]:
а) не кормить рожениц, а при необходимости использовать парентеральное питание;
б) шире пользоваться местным обезболиванием родов, когда оно показано и выполнимо;
в) ощелачивать и опорожнять желудок от содержимого до наркоза;
г) грамотно проводить наркоз, хорошо представляя опасность аспирации при введении в наркоз и при пробуждении;
е) дифференцировать два вида аспирационных синдромов и применять срочную терапию при каждом из них.
Введение принципов Мендельсона в клиническое акушерство и анестезиологию, безусловно, носило положительный характер. Кроме клинической настороженности и разработки принципов борьбы с аспирацией желудочного содержимого, это остановило беспорядочный характер кормления женщин в родильных залах. Но что тогда можно считать рациональным и безопасным режимом кормления в родах? Оправдан ли один казенный вариант подхода ко всем женщинам, которым предстоят операция кесарева сечения или роды?
Первое, что получило широкое распространение в родильных залах, – строгий голод: запрет под страхом всех кар небесных какого-либо приема пищи и жидкости. Можно не удивляться широкому распространению этого приема, так как техника его выполнения довольно проста и, кроме строгости, не требует никаких материальных и интеллектуальных затрат.
Сторонники этих строгих мер считают, что, исключив еду и питье, они уменьшают вероятность возникновения аспирационных осложнений. Какова частота аспирационных осложнений там, где свято чтят заветы Мендельсона?
Прискорбно, но факт, что в последние десятилетия в некоторых экономически развитых странах анестезия вышла на первое место среди причин материнской смертности. Строгие ограничительные тенденции 40-х гг. не привели к ожидавшемуся серьезному снижению частоты материнской смертности от аспирационного пневмонита. J. S. Crawford [цит. по 18] показал, что с момента введения строгих «голодных» режимов в родильных залах уровень материнской смертности от аспирационного синдрома не только не уменьшился, но даже периодически возрастает. Несмотря на ночное голодание, у 25% женщин, которым предстоит операция кесарева сечения, объем желудочного содержимого более 25 мл и рН меньше 2,5, то есть они составляют серьезную группу по аспирации или регургитации кислым желудочным содержимым.
Строгая политика голодания в родах является скорее результатом консерватизма, чем вдумчивого отношения к проблеме. Длительное голодание вызывает увеличение секреции желудочного сока, а отсутствие питья серьезным образом замедляет эвакуацию желудочного содержимого по пищеварительному тракту. Когда такой «голодный» состав желудочного содержимого аспирируется, следует ожидать более тяжелого течения синдрома Мендельсона. Сторонникам «самых строгих правил» наверняка будут интересны результаты исследований, когда пациенткам за несколько часов до операции назначался легкий завтрак из чая и сухарей и при этом не было отмечено значительного увеличения объема и кислотности желудочного содержимого по сравнению с «голодной» группой [21].
Пересмотреть традиционные взгляды на принципы профилактики аспирационных осложнений заставила случайная находка при исследовании эффективности премедикации диазепамом в зависимости от способа его введения [30]. В группе пациентов, которые принимали диазепам внутрь, запивая 50 мл воды, объем и кислотность желудочного содержимого были значительно ниже. Понадобился такой «изощренный» эксперимент, чтобы только в 1982 г. смогли прийти к выводу, что прием воды за 2 часа до операции оказывает благоприятное влияние на этих пациентов. Справедливости ради следует отметить, что сам по себе диазепам также уменьшает объем и кислотность желудочного содержимого, но этот эффект оказался куда менее выраженным, чем прием нескольких глотков воды.
Вода является нейтральной жидкостью, которая быстро покидает желудок, увлекая за собой его содержимое. К тому же вода разводит желудочное содержимое, повышая его рН. Холодная жидкость стимулирует перистальтику и ускоряет опорожнение желудка. С этим связано, что некоторые акушеры дают роженицам периодически сосать ледяные шарики. Мы не оригинальны в своих рекомендациях, так как E. M. Grady и A. G. Macdonald советуют назначение 100 мл воды за 2 часа до вводного наркоза [27]. Но предложено это было только в 1988 г., и промежуток 2 часа представляется слишком значительным.
Безусловно, что тяжесть аспирационных пневмонитов в какой-то степени, кроме кислотности, зависит еще и от объема аспирата. Аспирация 0,6 мл/кг желудочного содержимого, рН которого равен 1, приводит к слабым клиническим проявлениям, в большинстве случаев рентгеннегативным и не требующим лечения. Аспирация 0,8 мл/кг характеризуется тяжелым течением синдрома Мендельсона и высокой степенью летальности.
В большинстве случаев регургитация является грозным осложнением, не менее опасным, чем рвота. И не случайно в английской анестезиологической литературе к термину «регургитация» часто добавляют эпитет «silent» – немая, безмолвная. Она может быть причиной очень многих респираторных осложнений не только во время проведения анестезии, но и в раннем послеоперационном периоде.
Замедление эвакуации желудочного содержимого в послеоперационном периоде может значительно увеличивать риск как аспирации, так и регургитации [8]. Все будет зависеть от степени выраженности в данный момент постнаркозной депрессии. Задержка в опорожнении желудка вызывает к его расширению. Это приводит к растяжению механорецепторов гладкомышечных волокон стенки желудка и через стимуляцию вагуса провоцирует тошноту с последующей рвотой.
Механизмы аспирации. Пищевые массы аспирируются больными при рвоте и регургитации – пассивном пищеводном рефлюксе.
Рвотный центр находится под влиянием физических факторов, вестибулярных ядер, хеморецепторной триггерной зоны, а также сенсорной афферентации от глотки, желудочно-кишечного тракта, брюшины и гениталий. Он очень тесно взаимодействует с другими вегетативными центрами ствола мозга, поэтому рвоту могут провоцировать иногда самые незначительные факторы. Анестезиологам достаточно хорошо знакома ситуация у родильниц, когда поверхностная анальгезия, расширение шейки матки или даже попытка сесть могут быть достаточными для возникновения рвоты. Последнюю также часто провоцируют эпидуральная и спинномозговая анестезии. Это является большей частью результатом развивающейся артериальной гипотонии. Данной теме посвящены другие наши работы, в которых приведены результаты исследования факторов риска и эффективности различных медикаментов, используемых для премедикации [4].
При сохранении рефлекторной регуляции возникающий в момент рвоты ларингоспазм и поднятие мягкого нёба препятствуют попаданию рвотных масс в дыхательные пути. Эти защитные реакции значительно ослабевают при введении наркотических анальгетиков в родах.
Регургитация, или пассивный желудочно-пищеводный рефлюкс, возникает, когда давление в желудке выше, чем в пищеводе и глотке, а естественные сфинктеры открыты.
При каждом вдохе внутрижелудочное давление бывает на 15–25 см вод. ст. выше внутрипищеводного, и если бы природой не было придумано специальных препятствий, то с каждым вдохом возникал бы желудочно-пищеводный рефлюкс. Однако этому препятствуют пищеводно-желудочный угол, играющий роль клапана; кардиальный сфинктер, расположенный ниже диафрагмы и находящийся под высоким внутрибрюшным давлением; слизистый клапан-розетка вокруг кардии, образующий особый тонус и имеющий собственную мышечную оболочку, и, наконец, сдавление пищевода в диафрагмальном отверстии. При беременности повышение внутрибрюшного давления и поднятие купола диафрагмы изменяют пищеводно-желудочный угол, а значит, несколько уменьшают эффективность этого защитного механизма. Желудочно-пищеводный сфинктер имеет длину от 2 до 5 см и движется вверх при вдохе и вниз при выдохе. Он простирается выше и ниже диафрагмы, и давление его сжатия во много раз превышает давление внутри желудка.
У здоровых небеременных женщин внутрижелудочное и внутрипищеводное давление составляют соответственно около 20 и 2 см вод. ст. Следовательно, не будь сфинктера, происходил бы обратный ток жидкости (рефлюкс) под давлением около 18 см вод. ст. Но усилие желудочно-пищеводного сфинктера составляет около 55 см вод. ст., и его с избытком (свыше 30 см вод. ст.) хватает, чтобы препятствовать регургитации.
Иные соотношения наблюдаются у беременных, особенно у имеющих повышенную кислотность желудочного содержимого. У них внутрижелудочное давление на 6–7 см вод. ст. выше, а сфинктерное – на 10 см ниже нормального, благодаря чему барьерное различие, препятствующее регургитации, снижается почти вдвое. У беременных довольно часто регистрируется гастроэзофагеальный рефлюкс, который исчезает спустя 8 часов после родоразрешения. Изжога, довольно часто встречающаяся у беременных, уменьшает барьерное различие еще в два раза [16]. Эти женщины должны составлять серьезную группу риска.
Возникновению регургитации у рожениц способствует замедление пассажа пищи, которое принято связывать с увеличением внутрибрюшного давления. Если организм действительно задуман как саморегулирующаяся система, то увеличение внутрибрюшного давления должно вызывать ответный рост давления сфинктера [20]. Это действительно происходит, к примеру, при асците, когда эвакуация асцитической жидкости или назначение мочегонных препаратов приводит к уменьшению давления сфинктера. При проведении лапароскопии отмечается увеличение тонуса сфинктера в момент раздувания брюшной полости углекислым газом [23]. При беременности же, напротив, с увеличением срока и ростом внутрибрюшного давления прогрессивно снижается тонус сфинктера. Рост внутрижелудочного давления начинается в ранние сроки и не связан с ростом беременной матки [35]. Следовательно, механический фактор при этих нарушениях не столь значительный, как гормональный. Это подтверждает тот факт, что уровень барьерных давлений возвращается к норме только спустя 6 недель после родов [15], то есть после окончательной нормализации прогестерон-эстрогеновой активности. Последняя гипотеза подтверждается снижением давления сфинктера у женщин, принимающих пероральные гормональные контрацептивы [29], что, кроме всего прочего, также необходимо учитывать при подготовке их к плановым оперативным вмешательствам.
В гормональных влияниях следует винить не только прогестерон. Интересно, что у беременных плацента довольно активно синтезирует гастрин [50]. Таким образом, любой вид плацентарной недостаточности уменьшает секрецию гастрина и замедляет моторику желудочно-кишечного тракта. Известно, что между уровнем кислотности и количеством гастрина имеется обратно пропорциональная зависимость, а кислотность желудочного сока при беременности может возрастать. Вероятно, что снижение уровня гастрина сопряжено не только с уровнем кислотности желудочного содержимого. Гистамин вызывает резкое увеличение кислотного компонента секреции. В этой связи аспирация желудочного содержимого у беременных с преэклампсией всегда сопряжена с большей опасностью.
Давление желудочно-пищеводного сфинктера падает до своей самой низкой отметки в сроке 36 недель беременности, а это не всегда сопровождается максимальным снижением рН желудочного содержимого. Сложные механизмы регуляции тонуса желудочно-пищеводного сфинктера должны привести нас к мысли, что если на данном этапе мы не можем серьезно и в короткий срок увеличить его эффективное давление, то, по крайней мере, должны избегать там, где это возможно, ситуаций и средств, уменьшающих его тонус.
Механизмы нарушения дыхания. После попадания в дыхательные пути желудочного содержимого отмечаются нарушения дыхания и кровообращения. В то же время частота аспирационных осложнений может быть гораздо выше, если учесть, что часть аспираций во время анестезии остается незамеченной. Часть из них может действительно пройти бесследно, если pH желудочного сока > 2,5 [16]. Аспирация опасна не столько механическим препятствием дыханию, сколько немедленными рефлекторными реакциями и последующим пневмонитом, то есть преимущественным отечно-воспалительным поражением интерстициальной, периальвеолярной и перибронхиальной ткани.
Первичная реакция на кислое желудочное содержимое в легких – это ларинго- и бронхоспазм, а также брадиаритмия, которые возникают как вагальный рефлекс на раздражение дыхательных путей, что приводит к спадению легочного синуса. Нарушение вентиляции проявляется тахипноэ, диспноэ, клокочущим дыханием и цианозом [2]. После этого может наблюдаться короткий бессимптомный период, а затем начинается довольно характерная клиника гиперергического пневмонита. Гиперергическое течение пневмонита у рожениц обусловлено, с одной стороны, значительным увеличением внесосудистой воды в легких, которое присутствует еще до попадания желудочного содержимого. В последующем это способствует более значительному интерстициальному отеку и увеличивает тяжесть острого повреждения легких. С другой стороны, пневмонит, как реакция легочной ткани, зависит от иммунологического фона, создающегося беременностью, что во многом определяет последующий сценарий синдрома системной воспалительной реакции.
Рентгенография может помочь в диагностике аспирационных пневмонитов. И хотя признаков, отличающихся от обширных двухсторонних пневмоний чаще всего нет, рентгенологическая картина может быть разной в зависимости от положения тела больной на момент аспирации. Может также выявляться диффузное пятнистое затемнение с преимущественным поражением правого легкого: в него все-таки чаще попадает кислое желудочное содержимое. Аспирация твердым желудочным содержимым обычно проявляется полным или частичным ателектазом целого легкого либо его доли. Рентгенологические подтверждения аспирационного пневмонита были найдены в 38% случаев аспирации. Правосторонние поражения регистрировались чаще, чем левосторонние [24]. Более того, проявление этих изменений в ранние сроки после оперативного вмешательства сразу же должны насторожить врача в отношении имевшей место скрытой аспирации.
Как и всякое критическое состояние, аспирационный синдром не ограничивается только поражением дыхания. В связи с гипоксией довольно рано присоединяется нарушение реологических свойств крови, ведущее к гиповолемии, метаболическому ацидозу, коагулопатии. Среди причин отека легких может быть также высокая степень легочной гипертензии.