атрофия паренхимы поджелудочной железы что это такое
Атрофия поджелудочной железы
Атрофия поджелудочной железы – достаточно трудно поддающаяся своевременной диагностике патология, при которой поджелудочная железа значительно уменьшается в объёме. В норме масса поджелудочной железы составляет 60-90 г, при атрофии это значение снижается до 20 г и менее. Атрофические изменения в поджелудочной железе, как правило, развиваются годами, возникающий при этом дискомфорт пациент списывает на другие факторы.
Причины возникновения
Практически у каждого пациента с атрофией поджелудочной железы в прошлом был выявлен хронический панкреатит. Патология также может быть:
Симптомы
Поджелудочная железа – это орган, который функционирует в системе:
Проявления заболевания зависит от того, какие именно функции поражены. Если при атрофии поджелудочной железы сокращается выработка пищеварительных ферментов, наблюдаются симптомы, характерные для нарушения усваивания пищи:
При нарушении эндокринной функции поджелудочной железы появляются признаки нарушения углеводного обмена:
Диагностика и лечение
При подозрении на атрофию поджелудочной железы пациенту назначают:
Ранняя диагностика позволяет добиться максимального эффекта терапии. Врач назначает ферментные препараты для нормализации процессов пищеварения и инсулинотерапию для коррекции уровня сахара крови. При отсутствии положительного результата при лечении назначается хирургическое вмешательство.
Записаться на приём к гастроэнтерологу «Эммаклиник» для прохождения диагностики и терапии заболеваний поджелудочной железы можно по телефону +7 (495) 652-11-11 либо через онлайн-форму заявки на сайте.
Атрофия поджелудочной железы
Атрофия поджелудочной железы – это уменьшение объема органа, проявляющееся недостаточностью внешнесекреторной (продукция пищеварительных ферментов, бикарбоната) и внутрисекреторной (синтез инсулина, глюкагона) функции. Наиболее частыми причинами патологии являются хронический панкреатит, сахарный диабет, соматические заболевания с выраженным истощением, а также цирроз печени, нарушение кровоснабжения, сдавление опухолью. Диагностика основана на лабораторных данных, выявляющих дефицит ферментов и низкий уровень инсулина, УЗИ поджелудочной железы, результатах биопсии. Лечение заключается в назначении заместительной терапии: ферментных препаратов, инсулина; восстановлении кишечной флоры; коррекции дефицита нутриентов.
МКБ-10
Общие сведения
Атрофия поджелудочной железы – состояние, характеризующееся уменьшением размеров органа, уплотнением его структуры и недостаточностью функций. Данный процесс может развиваться вследствие физиологических возрастных изменений, а также заболеваний, сопровождающихся повреждением паренхимы, сдавлением, нарушением кровоснабжения, при длительно протекающих истощающих заболеваниях. При этом вес железы, который в норме составляет около 80-90 г, уменьшается до 30-40 и ниже.
Причины
Атрофия поджелудочной железы может быть физиологической, развивающейся в результате естественных процессов старения организма. Она сопровождает тяжелые истощающие заболевания (кахектическая форма). Также атрофия является исходом всех форм хронического панкреатита, при этом значительная часть стромы замещается фиброзной тканью, что сопровождается прогрессированием эндокринной и экзокринной недостаточности.
Своеобразным типом атрофии является липоматоз, при котором большая часть паренхимы органа замещена жировой тканью. Отдельное место занимает атрофия панкреас при сахарном диабете. К более редким случаям заболевания в гастроэнтерологии относится атрофия железы при циррозе печени, системной склеродермии, сдавлении опухолью, перекрытии выводных протоков конкрементами.
Патанатомия
Данная патология сопровождается существенным уменьшением размеров железы – до 20-18 г, консистенция значительно уплотнена, поверхность органа бугристая, капсула сращена с окружающей ее жировой тканью, а также соседними органами. Изменяется структура поджелудочной железы, характерно избыточное развитие соединительной ткани, которая может пролиферировать вокруг долек (перилобулярный склероз) либо диффузно (интралобулярный склероз). На микроскопическом уровне поражение характеризуется диффузным разрастанием фиброзной ткани (интраацинозный склероз), гибелью клеток железистой паренхимы.
При липоматозе, несмотря на то, что данное состояние характеризуется сохранением или даже увеличением размеров органа (псевдогипертрофия), его большая часть замещена жировой тканью, в которой находятся отдельные железистые участки. По наблюдениям специалистов в области клинической гастроэнтерологии и эндокринологии, большинстве случаев при данной патологии сохраняется островковый аппарат и эндокринная функция органа.
Симптомы атрофии
Клиническая картина атрофии поджелудочной железы определяется причиной ее развития (сахарный диабет, хронический панкреатит и другие). Однако в любом случае характерными симптомами являются экзокринная и эндокринная недостаточность. Экзокринная (внешнесекреторная) недостаточность железы характеризуется пониженной продукцией пищеварительных ферментов, а также бикарбонатов и других электролитов, которые нейтрализуют содержимое желудка, обеспечивая благоприятную для действия панкреатических ферментов среду. Типичными симптомами являются послабление стула, ухудшение аппетита, снижение веса.
Ранним симптомом недостаточности внешнесекреторной функции является стеаторея (повышенное выведение жиров с калом). Этот признак развивается при снижении секреции на 10% от нормы. Снижение веса происходит вследствие нарушения переваривания пищи, всасывания веществ в кишечнике, потери аппетита. При длительно существующей патологии развиваются признаки дефицита витаминов.
Эндокринная (внутрисекреторная) недостаточность проявляется нарушениями углеводного обмена, протекающими по типу гипергликемического синдрома. При этом симптомы сахарного диабета развиваются лишь у половины пациентов. Это объясняется тем, что инсулинпродуцирующие клетки обладают способностью лучше сохраняться при патологии в сравнении с ацинарными. Развивается дефицит инсулина, глюкагона. Пациента может беспокоить выраженная слабость, головокружение, жажда.
Диагностика
При обследовании пациента с атрофией поджелудочной железы определяется дефицит массы тела. Кожные покровы сухие, шелушащиеся. При уменьшении размеров железы пропальпировать ее не удается. Если причиной состояния стал панкреатит, возможна болезненность при прощупывании. Алгоритм диагностики включает:
Лечение атрофии поджелудочной железы
Консервативные мероприятия
При атрофии панкреас обязательно назначается диетотерапия. Питание должно быть с минимальным содержанием жиров. Достаточно внимания следует уделять белково-энергетическому дефициту, коррекции гиповитаминозов. Обязательным мероприятием является полное прекращение курения, поскольку никотин нарушает продукцию бикарбонатов поджелудочной железой, в следствие чего значительно повышается кислотность содержимого двенадцатиперстной кишки.
Основным направлением терапии данной патологии является замещение экзокринной и эндокринной секреции поджелудочной железы. Для компенсации нарушенных процессов полостного пищеварения врач-гастроэнтеролог назначает ферментные препараты. Для достижения клинического эффекта препараты должны обладать высокой активностью липазы, быть устойчивыми к действию желудочного сока, обеспечивать быстрое высвобождение ферментов в тонкой кишке, активно содействовать полостному пищеварению. Данным требованиям соответствуют ферменты в виде микрогранул.
Поскольку именно липаза из всех ферментов панкреаса быстрее всего теряет активность, коррекция производится с учетом ее концентрации в препарате и выраженности стеатореи. Эффективность лечения оценивается по содержанию эластазы в кале и степени уменьшения стеатореи. Действие ферментных препаратов направлено и на устранение болевого синдрома, уменьшение вторичного энтерита, создание условий для нормализации кишечного микробиоценоза, улучшение углеводного обмена.
Коррекция эндокринной недостаточности проводится путем инсулинотерапии. При атрофии поджелудочной железы частично сохраняются островки Лангерганса, поэтому инсулин в организме продуцируется, но в малых количествах. Дозировка и режим введения инсулина определяются индивидуально в зависимости от течения патологии, этиологического фактора, данных суточного мониторирования глюкозы крови. Назначение ферментных препаратов значительно улучшает функцию поджелудочной железы в целом и углеводный обмен в том числе. Поэтому режим инсулинотерапии определяется в зависимости от дозировки и эффективности заместительной ферментной терапии.
Важным условием эффективной коррекции пищеварительных функций является нормализация микробиоценоза кишечника, поскольку на фоне приема ферментов создаются благоприятные условия для заселения патогенной флоры. Применяются пробиотики, пребиотики. Обязательно назначается витаминотерапия инъекционно, а также препараты магния, цинка, меди.
Хирургическое лечение
Хирургическое лечение данной патологии проводится в специализированных центрах. Осуществляется трансплантация островков Лангерганса с последующим удалением железы и заместительной ферментной терапией. Однако, поскольку атрофия зачастую является следствием тяжелых заболеваний с выраженным нарушением общего состояния пациента, такое лечение проводится редко.
Прогноз и профилактика
Прогноз при атрофии поджелудочной железы определяется степенью поражения экзокринных и эндокринных структур органа. Поскольку островковый аппарат частично сохранен, существует и остаточный синтез инсулина. Ввиду этого редко развивается кетоацидоз, но часто возникают гипогликемические состояния. Определение этиологии заболевания, устранение основной патологии, своевременное начало лечения позволяют достичь хороших результатов.
Профилактика заключается в своевременном лечении заболеваний, которые могут стать причиной атрофии панкреас. При наличии хронического панкреатита обязателен полный отказ от алкоголя, соблюдение диеты, поддержание достаточного уровня ферментативной активности железы.
Другие уточненные болезни поджелудочной железы (K86.8)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
К данной подрубрике отнесены состояния, различающиеся как по морфологическим признакам, так и по этиологии и патогенезу. Чаще всего они связаны с острым или хроническим панкреатитом (включая алкогольный хронический панкреатит), но не ограничиваются ими.
* Образный термин, введенный в 1887 г. по визуальной аналогии поражения поджелудочной железы с циррозом печени.
** Термин «панкреатонекроз» является скорее патологоанатомическим, нежели клиническим, ввиду чего использовать его в качестве клинического диагноза не совсем верно. Под термином «тотально-субтотальный панкреонекроз» понимается деструкция поджелудочной железы с поражением всех отделов (головка, тело, хвост). Абсолютно тотальный панкреонекроз не встречается.
Этиология и патогенез
Атрофия поджелудочной железы является следствием (стадией) хронического панкреатита (в том числе обструктивного, некалькулезного и калькулезного хронического панкреатита). Атрофия может сочетаться с фиброзом ПЖ.
Также атрофия или фиброз ПЖ могут возникать вследствие следующих причин:
— атеросклероз;
— старческие изменения ПЖ;
— сахарный диабет;
— оперативные вмешательства на ПЖ;
— нарушения питания.
Патологическая и физиологическая атрофия отличаются по этиологии и качественным особенностям. В основе атрофии лежит преобладание процессов диссимиляции над процессами ассимиляции, что связано со снижением активности цитоплазматических ферментов.
Недоразвитие (инфантилизм) поджелудочной железы (клинический синдром Кларка-Хэдфилда) является врожденной формой недостаточности секреции гормонов ПЖ, включая инсулин. Этиология доподлинно неизвестна. Страдают дети младшего возраста.
Панкреонекроз протекает в нескольких видах:
Современные возможности терапии хронического панкреатита
Хронический панкреатит — длительно протекающее воспалительное заболевание поджелудочной железы, проявляющееся необратимыми морфологическими изменениями, которые вызывают боль и/или стойкое снижение функции поджелудочной железы. При хроническом панкреатит
Хронический панкреатит — длительно протекающее воспалительное заболевание поджелудочной железы, проявляющееся необратимыми морфологическими изменениями, которые вызывают боль и/или стойкое снижение функции поджелудочной железы. При хроническом панкреатите морфологические изменения поджелудочной железы сохраняются после прекращения воздействия этиологического агента. В настоящее время распространенность хронического панкреатита, по данным аутопсий, составляет от 0,01 до 5,4%, в среднем — 0,3-0,4%, при этом за последние 40 лет заболеваемость выросла примерно в два раза, что связывают с тем, что население стало употреблять больше алкогольных напитков, а также с воздействием вредных факторов окружающей среды (см. диаграмму 1).
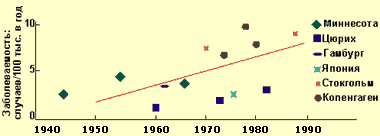 |
| Диаграмма 1. Заболеваемость ХП в 1945—1985 гг. (Worning H., 1990) |
В патогенезе хронического панкреатита важную роль играют несколько факторов. Одним из основных является обструкция главного панкреатического протока при конкрементах, воспалительном стенозе или опухолях. При алкогольном панкреатите повреждение поджелудочной железы связано с повышением содержания белка
в панкреатическом секрете, что приводит к возникновению белковых пробок и обструкции мелких протоков железы. Другим фактором, влияющим на патогенез алкогольного панкреатита, является изменение тонуса сфинктера Одди: его спазм вызывает внутрипротоковую гипертензию, а релаксация способствует рефлюксу дуоденального содержимого и внутрипротоковой активации панкреатических ферментов.
Разрушение экзокринной части поджелудочной железы вызывает прогрессирующее снижение секреции бикарбонатов и ферментов, однако клинические проявления нарушения переваривания пищи развиваются лишь при деструкции более 90% паренхимы органа. В первую очередь возникают проявления недостаточности липазы в виде нарушения всасывания жиров, жирорастворимых витаминов: A, D, E и K, что нечасто проявляется поражением костей, расстройствами свертывания крови. У 10–30% больных хроническим панкреатитом развивается сахарный диабет, обычно на поздних стадиях заболевания, нарушение толерантности в глюкозе наблюдается гораздо чаще. Для таких больных характерно развитие гипогликемических реакций на инсулин, недостаточное питание или злоупотребление алкоголем. Кетоацидоз развивается редко, что связано с одновременным снижением продукции инсулина и глюкагона.
Приступ хронического панкреатита проявляется иррадиирующими в спину болями в верхней половине живота, развивающимися после приема пищи, которые могут продолжаться в течение многих часов или нескольких дней. Нередко наблюдается тошнота, рвота, у 30–52% пациентов — снижение веса, у 16–33% — желтуха. Преходящая желтуха возникает вследствие отека железы при обострениях хронического панкреатита, постоянная — связана с обструкцией общего желчного протока вследствие фиброза головки поджелудочной железы. При разрывах протоков поджелудочной железы, на месте предыдущего некроза ткани происходит скопление секрета, что приводит к формированию псевдокист. Кисты могут быть бессимптомными или вызывать боли в верхней половине живота. При длительном течении заболевания, при уменьшении объема функционирующей паренхимы до 10% от нормы появляются признаки мальабсорбции (полифекалия, жирный стул, похудание).
В течении хронического панкреатита можно выделить несколько стадий (Lankisch P.G., Moessner Y.), умение различать которые важно для правильного подбора терапии. Так, на первой стадии заболевания клиническая симптоматика отсутствует: в этот период характерные для ХП изменения данных КТ или ЭРХПГ выявляются лишь при случайном обследовании.
На второй стадии возникают начальные проявления, характеризующиеся частыми эпизодами обострения ХП (которые могут быть ошибочно расценены как острый панкреатит). Заболевание видоизменяется от повторных приступов боли в животе до постоянных умеренных болей и похудания. С течением времени рецидивы становятся менее тяжелыми, но симптоматика сохраняется в периоды между приступами. На этой стадии может существенно ухудшаться качество жизни. Вторая стадия обычно продолжается на протяжении четырех—семи лет. Иногда заболевание быстро прогрессирует, развивается атрофия ПЖ, и нарушается функция органа.
У больных на третьей стадии постоянно присутствует симптоматика ХП, прежде всего — абдоминальная боль. Пациенты могут стать зависимыми от анальгетиков, значительно сокращают объем принимаемой пищи из-за опасения усиления боли. Появляются признаки экзокринной и эндокринной панкреатической недостаточности.
Особенность панкреатита на четвертой стадии — это атрофия ПЖ, развитие экзокринной и эндокринной недостаточности, что проявляется стеатореей, похуданием и сахарным диабетом. Снижается интенсивность боли, прекращаются острые приступы заболевания, могут развиваться тяжелые системные осложнения ХП и аденокарцинома поджелудочной железы.
Терапия панкреатита проводится по нескольким направлениям: отказ от употребления алкоголя; соблюдение диеты с низким содержанием жира (до 50–75 г/сут) и частым приемом небольших количеств пищи; купирование боли; ферментная заместительная терапия, борьба с витаминной недостаточностью; лечение эндокринных нарушений.
Лечение приступа хронического панкреатита, а также острого панкреатита проводиться по аналогичной схеме. Обязательные компоненты терапии: внутривенное введение растворов электролитов и коллоидов, голодная диета (полное голодание до двух дней) и анальгезия (например, меперидин). Рекомендуется введение свежезамороженной плазмы или альбумина. Диуретики не показаны большинству больных: олигурия разрешается при исчезновении гиповолемии и нормализации перфузии почек. Для облегчения рвоты, купирования пареза желудочно-кишечного тракта и уменьшения стимуляции поджелудочной железы может быть использована аспирация содержимого желудка через назогастральный зонд. Коагулопатия, возникающая при панкреатите, обычно требует назначения гепарина, свежей плазмы. В последние годы при остром панкреатите показана эффективность антагониста тромбоцит-активирующего фактора лексипафанта (60–100 мг/сут), однако его действие при хроническом панкреатите еще нуждается в уточнении.
Применение ингибиторов протеолитических ферментов (например, апротинина, габексата) является спорным. Исследования показывают, что при остром панкреатите не наблюдается дефицита ингибиторов протеаз, кроме того, проведенные клинические исследования не выявили преимуществ этих препаратов по сравнению с плацебо. Однако существуют данные, что габексат, низкомолекулярный ингибитор трипсина, эффективно используется для профилактики развития острого панкреатита, связанного с ЭРХПГ.
Ингибиторы секреции поджелудочной железы: глюкагон, соматостатин, кальцитонин, ингибиторы карбоангидразы, вазопрессин, изопреналин, также было предложено применять для лечения острого панкреатита, однако их эффективность к настоящему времени не получила достаточного подтверждения. Препараты пищеварительных ферментов можно использовать для лечения как в разгар заболевания с целью подавления панкреатической секреции, так и в период выздоровления, когда пациент снова получает возможность принимать пищу орально.
При билиарном обструктивном панкреатите должна быть проведена своевременная эндоскопическая декомпрессия желчных путей. Выполняется папиллосфинктеротомия, дилатация или стентирование панкреатического протока. Хирургическое лечение обструктивного панкреатита, безусловно, является основным методом, в то же время целесообразность проведения вмешательства в первые сутки после развития тяжелого приступа должна быть признана спорной. После стихания остроты воспаления целесообразно проведение холецистэктомии.
Схему длительной терапии при хроническом панкреатите можно разделить на две основные части, в соответствии с ведущими клиническими синдромами (см. диаграмму 2).
Боль могут облегчить большие дозы панкреатических ферментов. Попадание ферментов поджелудочной железы (прежде всего — трипсина) в двенадцатиперстную кишку по механизму отрицательной обратной связи вызывает снижение панкреатической секреции, снижение внутрипротокового давления и уменьшает боль. Традиционно для этой цели использовались порошок или таблетированные препараты панкреатина.
Если болевой синдром резистентен к терапии, при расширении главного протока более 8 мм, у 70–80% пациентов облегчение может принести латеральная панкреатоеюностомия. В случаях, когда панкреатический проток не расширен, показано проведение дистальной панкреатэктомии (при преимущественном поражении хвоста железы) или операция Уиппла (Whipple) (при поражении в основном головки железы). Альтернативой операции является чрезкожная денервация солнечного сплетения введением алкоголя, однако эффект этой процедуры сохраняется лишь в течение нескольких месяцев. Весьма перспективно эндоскопическое лечение под контролем эндоскопического УЗИ (дренирование псевдокист, невролиз солнечного сплетения).
Показаниями для заместительной терапии экзокринной панкреатической недостаточности являются исключительно клинические показатели: похудание, стеаторея, метеоризм. Классическая рекомендация, предусматривающая определение содержания жира в кале перед назначением лечения, в настоящее время потеряла свое значение из-за трудоемкости и низкой чувствительности данного метода. Для купирования внешнесекреторной панкреатической недостаточности используют различные препараты экстрактов поджелудочной железы (см. таблицу 1).
При выборе препарата для заместительной терапии следует учитывать следующие показатели:
Способность препарата активироваться только в щелочной среде — очень важное свойство, которое резко повышает эффективность ферментов; так, при использовании препарата, имеющего энтеросолюбильную оболочку, всасывание жиров повышается в среднем на 20% по сравнению с такой же дозой обычного средства. Однако при хроническом панкреатите происходит значительное снижение продукции бикарбонатов, что приводит к нарушению щелочной среды в двенадцатиперстной кишке. Это создает несколько проблем. Первая касается нарушения активации частиц ферментного препарата, покрытых энтеросолюбильной оболочкой. Вторая проблема заключается в том, что в кислой среде происходит преципитация желчных солей и нарушение эмульгации жира, что делает его малодоступным для расщепления липазой. Поэтому эффективность ферментной терапии (см. рисунок 1) может быть повышена благодаря одновременному назначению антацидов за 30 мин до и через 1 ч после еды или антисекреторных препаратов (Н2-блокаторы, омепразол), но необходимо помнить, что антациды, содержащие кальций или магний, ослабляют действие ферментных препаратов. Возможно использование препаратов, содержащих протеолитические ферменты растительного происхождения, которые сохраняют активность в гораздо более кислой среде, чем животные.
Значительное снижение качества жизни больного панкреатитом связано с такой проблемой, о которой обычно забывают, как стойкое вздутие живота. Нередко вздутие не купируется даже при приведении заместительной терапии высокими дозами ферментов. В этом случае к проводимой терапии необходимо добавить адсорбенты (симетикон, диметикон) или использовать комбинированные ферментные препараты, содержащие адсорбирующие вещества.
Разовая доза ферментов, которая рекомендуется для лечения внешнесекреторной панкреатической недостаточности, должна содержать не менее 20–40 тыс. ед. липазы. Обычно пациенту назначают две—четыре капсулы препарата (по 20—25 тыс. ед. липазы) при основных приемах пищи и по одной-две капсуле (по 8—10 тыс. ед. липазы) или таблетки панкреатина при употреблении небольшого количества пищи. При клинически выраженной панкреатической недостаточности обычно не удается полностью устранить стеаторею даже с помощью высоких доз препаратов, поэтому критериями адекватности подобранной дозы пищеварительных ферментов являются: прибавка веса, нормализация стула (менее трех раз в день), снижение вздутия живота.
Причины неэффективности заместительной терапии могут быть связаны как с неточной диагностикой заболевания, так и с неадекватным назначением терапии больному (см. рисунок 2).
Побочные эффекты ферментной терапии (см. рисунок 3) обычно не носят тяжелого характера, наиболее известный опасный побочный эффект — развитие фиброзирующей колопатии — возникает при длительном приеме очень высоких доз ферментов в виде микротаблеток: более 50 тыс. ед. липолитической активности на 1 кг веса тела в сутки.
Таким образом, терапия хронического панкреатита должна проводиться дифференцированно, в зависимости от ведущего клинического синдрома и стадии заболевания. Заболевание, которое удается обнаружить на первой стадии, как правило, не требует медикаментозной коррекции, в этом случае обычно достаточно изменения образа жизни и диетотерапии. Лечение ХП на второй стадии включает назначение таблетированного панкреатина, антисекреторных препаратов и спазмолитиков. Третья стадия обычно требует использования всего арсенала средств, которые имеются у врача для купирования панкреатической боли: микрогранулы панкреатина, антисекреторные препараты, октреотид, спазмолитики, мощные анальгетики, психотропные препараты. На последней, четвертой, стадии лечение основывается, прежде всего, на использовании микрогранул панкреатина в высокой дозе с целью проведения заместительной терапии.
По вопросам литературы обращайтесь в редакцию
А. В. Охлобыстин, кандидат медицинских наук
Э. Р. Буклис, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва

