ацетилхолинэстераза в нервно мышечном синапсе что делает
Ацетилхолинэстераза в нервно мышечном синапсе что делает
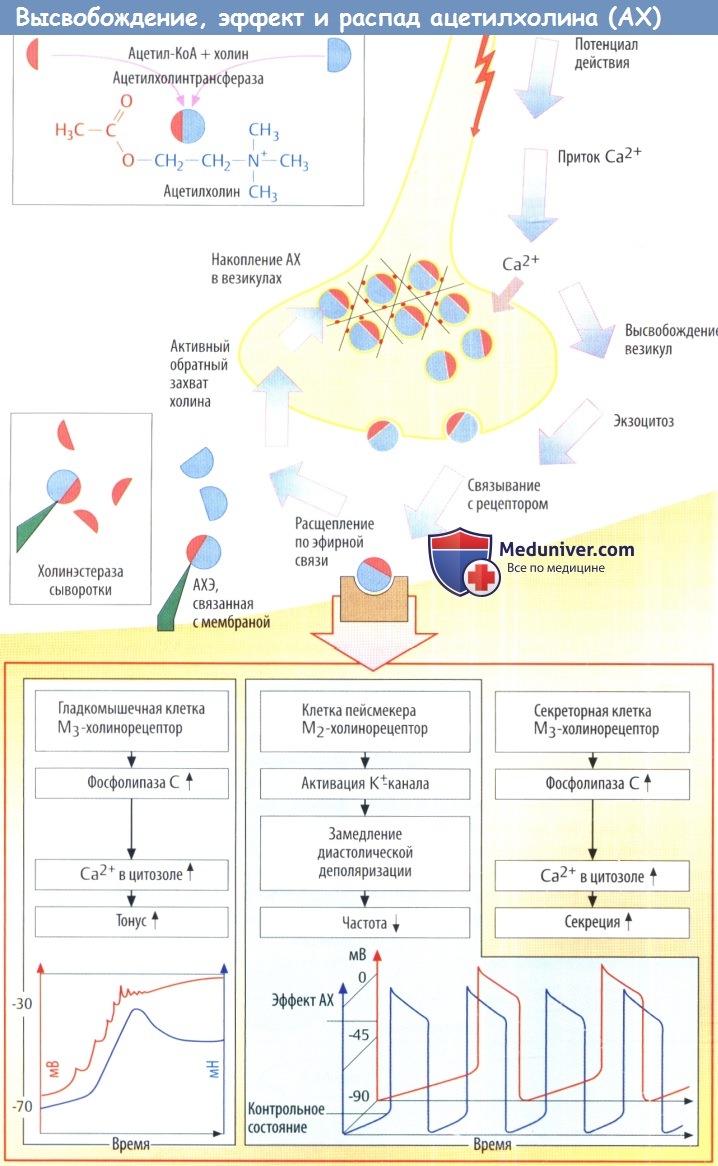
Ацетилхолин (АХ) служит медиатором постганглионарных синапсов окончаний парасимпатических нервов. Ацетилхолин (АХ) в высокой концентрации содержится в синаптических пузырьках (везикулах), плотно расположенных в аксоплазме пресинаптических окончаний. АХ образуется из холина и активированного ацетата (ацетилкоэнзима А); эту реакцию катализирует цитоплазматический фермент ацетилхолинтрансфераза.
Перенос высокополярного холина в аксоплазму осуществляет специфический холиновый переносчик, расположенный в мембранах окончаний холинергических аксонов и субпопуляции везикул. Во время непрерывной или интенсивной стимуляции этот переносчик обеспечивает стабильный синтез и высвобождение АХ. Образовавшийся АХ транспортируется в пузырьки везикулярным транспортером (переносчиком) АХ. Механизм высвобождения АХ до конца не изучен.
Заполненные ацетилхолина (АХ) везикулы прикрепляются к цитоскелету белком синапсином. Это обеспечивает группирование везикул вблизи пресинаптической мембраны, одновременно препятствуя их слиянию друг с другом. Предполагается, что во время активации мембраны нервного волокна ионы Са 2+ попадают в аксоплазму через потенциалзависимые каналы и активируют протеинкиназы, фосфорилирующие синапсин.
В итоге расположенные рядом с мембраной везикулы отделяются от цитоскелета и сливаются с пресинаптической мембраной. В результате слияния содержимое везикул попадает в синаптическую щель; одновременно с этим специфический холиновый переносчик встраивается в плазматическую мембрану. АХ быстро диффундирует через синаптическую щель (молекула АХ чуть больше 0,5 нм; размер синаптической щели составляет 20-30 нм). На постсинаптической мембране эффекторной клетки АХ связывается со своими рецепторами.
Эти рецепторы также активируются алкалоидом мускарином, поэтому их называют мускариновыми (М) холинорецепторами. Действие ацетилхолина (АХ) на ганглионарные рецепторы и рецепторы на двигательной концевой пластинке можно воспроизвести никотином; эти рецепторы называются никотиновыми (N)холинорецепторами
Выделившийся ацетилхолин (АХ) быстро подвергается гидролизу и инактивируется специфической ацетилхолинэстеразой (АХЭ), расположенной в пре- и постсинаптических мембранах (базальной пластинке двигательных концевых пластин), либо неспецифической сывороточной холинэстеразой (бутирилхолинэстеразой) — водорастворимым ферментом, который находится в сыворотке и интерстициальной жидкости.
М3-холинорецепторы отвечаютза регуляциютонуса гладкой мускулатуры. Например, в кишечнике и бронхахактивация этих рецепторов стимулирует фосфолипазу С, деполяризацию мембраны и повышает мышечный тонус. М3-холинорецепторы также находятся в железистом эпителии, в котором происходит активация фосфолипазы С и секреторной активности. В ЦНС представлены все подтипы М-холинорецепторов, где они отвечаютза различные процессы: от регуляции активности коры, процессов памяти и обучения, обработки болевой импульсации до двигательного контроля на уровне ствола мозга.
Ацетилхолин (АХ) расслабляет тонус мышц кровеносных сосудов. Действие это непрямое, оно обусловлено стимуляцией М3-холинорецепторов эндотелиальных клеток, которые в ответ высвобождают NO (оксид азота — эндотелиальный сосудорасширяющий фактор). Оксид азота диффундирует в гладкомышечные клетки, где вызывает расслабление тонуса, обусловленного их сокращением.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «фармакология»
Ацетилхолинэстераза в нервно мышечном синапсе что делает
Холинэстераза является ферментом, необходимым для нормальной работы нервной системы. Она бывает двух типов: ацетилхолинэстераза, которая играет роль в передаче нервных импульсов, и псевдохолинэстераза, которая находится в сыворотке и клетках некоторых внутренних органов и участвует в переработке и разложении химических веществ, попавших в организм.
Бутирилхолинэстераза, псевдохолинэстераза, BCHE, ацетилхолинэстераза.
Синонимы английские
CHS, AChE, RBC cholinesterase, red cell cholinesterase, BChE, plasma cholinesterase, pseudocholinesterase, PCHE, erythrocyte acetylcholinesterase, butyrylcholinesterase.
Кинетический колориметрический метод.
Ед/л (единица на литр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Холинэстераза является ферментом, необходимым для работы нервной системы.
В организме есть два типа холинэстеразы: ацетилхолинэстераза, присутствующая в эритроцитах, а также в легких, селезенке, нервных окончаниях и сером веществе мозга, и псевдохолинэстераза (бутирилхолинэстераза), содержащаяся в сыворотке крови, печени, мышцах, поджелудочной железе, сердце и белом веществе мозга. Ацетилхолинэстераза участвует в передаче нервных импульсов путем расщепления ацетилхолина – химического вещества, передающего сигналы через окончания нервных клеток. Понижение активности ацетилхолинэстеразы приводит к накоплению ацетилхолина в нервных окончаниях. Это, в свою очередь, ведет к сверхраздражению нервных клеток.
Псевдохолинэстераза необходима для расщепления и метаболизации токсинов и лекарственных веществ.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Референсные значения
При выявлении отравлений пестицидами
После отравления фосфорорганическими веществами активность ацетилхолинэстеразы и псевдохолинэстеразы может стать на 80 % меньше нормы, а уже при падении больше чем на 40 % симптомы становятся тяжелыми.
Значительное снижение активности холинэстеразы обычно свидетельствует о чрезмерном поглощении фосфорорганических веществ организмом.
При анализе на чувствительность к сукцинилхолину
У 3 % людей активность псевдохолинэстеразы понижена из-за наследственности, и в случае введения миорелаксанта сукцинилхолина они будут испытывать на себе его эффект более продолжительное время, чем нужно. У таких пациентов низкая активность псевдохолинэстеразы указывает на повышенный риск продолжительного действия миорелаксанта.
Кроме того, активность холинэстеразы может снижаться при хронических болезнях печени и недоедании, беременности, почечной недостаточности, шоковом состоянии и некоторых типах рака.
Лечение психических расстройств (ингибиторы холинэстеразы)
Ингибиторы холинэстеразы также имеют названия ингибиторов ацетилхолинэстеразы (AChE) или антихолинэстераз.Они представляют собой группу препаратов, которые блокируют нормальное расщепление ацетилхолина (АХ) на ацетат и холин и тем самым увеличивают как уровни, так и продолжительность действия ацетилхолина в центральной и периферической нервной системе. Ингибиторы ацетилхолинэстеразы чаще всего используют при лечении нейрогенеративных заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона и деменция тела Леви. Различные физиологические процессы при этих дегенеративных нарушениях разрушают клетки, которые продуцируют АХ, и тем самым снижают холинергическую передачу в разных областях мозга. Препараты, ингибирующие холинэстеразу, ингибируют активность AChE и поддерживают уровень ACh, уменьшая скорость его распада.
Кроме того, ингибиторы холинэстеразы часто используются у пациентов с миастенией. Повышенный уровень ацетилхолина в нервно-мышечном соединении, следовательно, приводит к повышенной активации рецепторов ACh, обнаруженных на постсинаптических мембранах, что приводит к улучшению мышечной активации, сокращения и силы. В конце терапии вводят ингибиторы холинэстеразы, чаще всего неостигмин, чтобы обратить вспять эффекты недеполяризующих мышечных агентов, таких как рокуроний.
Ингибиторы холинэстеразы также необходимы для применения при подозрении на антихолинергическое отравление. Симптомы антихолинергического отравления включают вазодилатацию, ангидроз, мидриаз, бред и задержку мочи. Другие менее распространенные показания к применению ингибиторов холинэстеразы включают лечение пациентов с диагнозом определенных психических расстройств, таких как шизофрения, и лечение глаукомы путем сброса давления водянистой влаги.
Ингибиторы холинэстеразы функционируют, подавляя холинэстеразу от гидролиза ацетилхолина до компонентов ацетата и холина, что позволяет увеличить доступность и продолжительность действия ацетилхолина в нервно-мышечных соединениях. Фермент холинэстераза имеет два активных сайта: анионный сайт, образованный триптофаном, и эстерактический сайт, образованный серином. Ингибиторы холинэстеразы, такие как органофосфаты, препятствуют расщеплению холинэстеразы ацетилхолином путем взаимодействия с сайтинэстерактическим сайтом. В результате ацетилхолин будет продолжать накапливать и активировать связанные рецепторы.
Ингибиторы холинэстеразы классифицируют как обратимые, необратимые или псевдообратные. Обратимые ингибиторы холинэстеразы обычно используются в терапевтических целях. Напротив, необратимые и псевдообратимые ингибиторы часто используются в пестицидах и для биологической войны (нервные агенты).
Ингибиторы холинэстеразы увеличивают общее количество доступного ацетилхолина. Таким образом, могут присутствовать симптомы чрезмерной стимуляции парасимпатической нервной системы, такие как повышенная гиперчувствительность, гиперсекреция, брадикардия, миоз, диарея и гипотония.
Из-за способности повышать тонус блуждающего нерва через активацию парасимпатической нервной системы необходимо соблюдать осторожность при назначении ингибиторов холинэстеразы лицам, страдающим брадикардией или заболеваниями сердечной проводимости, такими как синдром слабости синусового узла. Эти люди подвергаются риску обморока и падений. Осторожность также рекомендуется пациентам, принимающим антигипертензивные препараты в связи с возможностью развития тяжелой гипотонии. Кроме того, ингибиторы холинэстеразы также противопоказаны пациентам с язвой желудка из-за повышенного риска желудочно-кишечных кровотечений. Пациенты с задержкой мочи также не должны получать ингибиторы холинэстеразы из-за риска повышенной задержки. Этот эффект особенно заметен у пациентов, проходящих лечение от деменции и болезни Альцгеймера, поскольку недержание мочи является частой клинической особенностью у этих пациентов. Назначение пациентам с предшествующими аллергиями или повышенной чувствительностью к ингибиторам холинэстеразы и ее производным также противопоказано.
Современный опыт применения антихолинэстеразных препаратов в неврологии
Антихолинэстеразные средства в неврологической практике применяются для активации процессов регенерации и реиннервации при заболеваниях периферической и центральной нервной системы
Антихолинэстеразные средства в неврологической практике применяются для активации процессов регенерации и реиннервации при заболеваниях периферической и центральной нервной системы.
Долгие годы в лечебной практике широко используется препарат «Прозерин», обладающий выраженным действием на периферические холинергические синапсы.
В конце 80-х гг. 20 века было синтезировано лекарственное средство «Амиридин» с комбинированным антихолинэстеразным эффектом. С 2002 г. препарат выпускается под торговым наименованием «Нейромидин».
Фармакологические эффекты антихолинэстеразных препаратов приводят к усилению действия ацетилхолина. Выбор препарата из группы антихолинэстеразных средств определяется его фармакологическими свойствами, длительностью действия, активностью, способностью проникать через тканевые барьеры, а также побочными эффектами.
Прозерин — N-(мета-диметилкарбамоилоксифенил)-триметиламмонийметил-сульфат обладает сильной обратимой антихолинэстеразной активностью. Основой механизма его действия является ингибирование ацетилхолинэстеразы — фермента, гидролизующего медиатор ацетилхолин, которое сопровождается замедлением скорости его разрушения, накоплением и усилением действия в области холинергических синапсов с восстановлением нервно-мышечной проводимости.
В связи с наличием в молекуле Прозерина четвертичной аммониевой группы, препарат плохо проникает через гематоэнцефалический барьер и оказывает в основном влияние на периферические холинергические структуры.
Существенным отличием Нейромидина (ипидакрина) от Прозерина является способность Нейромидина блокировать калиевую проницаемость мембраны, что приводит к продлению реполяризационной фазы потенциала ее действия и повышению активности пресинаптического аксона. Этот процесс сопровождается увеличением входа ионов кальция в пресинаптическую терминаль и, как следствие, усилением выброса медиатора ацетилхолина в синаптическую щель во всех синапсах, способствуя усилению стимуляции постсинаптической клетки.
Кроме того, Нейромидин обладает эффектом обратимого ингибирования холинэстеразы в холинергических синапсах, что дополнительно увеличивает накопление нейромедиатора в синаптической щели и соответственно усиливает функциональную активность постсинаптической клетки. Однако торможение действия ацетилхолинэстеразы у Нейромидина менее выражено по сравнению с Прозерином.
Таким образом, Нейромидин стимулирует пресинаптическое нервное волокно, увеличивает выброс нейромедиатора в синаптическую щель, уменьшает разрушение медиатора ацетилхолина ферментом, повышает активность постсинаптической клетки прямым мембранным и опосредованным медиаторным воздействием, то есть действует на все звенья проведения возбуждения, в отличие от Прозерина, который уменьшает метаболизм медиатора только в холинергических синапсах.
М-холиномиметические эффекты Прозерина и Нейромидина схожи, однако активность воздействия на М-холинорецепторы у Прозерина выше.
Нейромидин обладает следующими фармакологическими эффектами: восстанавливает и стимулирует нервно-мышечную передачу, проводит импульс в периферической нервной системе, нарушенный вследствие воздействия различных факторов. Нейромидин увеличивает сократительную активность мышц под влиянием ацетилхолина и других медиаторов: адреналина, серотонина, гистамина и окситоцина, оказывая прямое воздействие на миофибриллы, в то время как Прозерин таким свойством не обладает.
Нейромидин, в отличие от Прозерина, стимулирует проведение нервного импульса не только в нервно-мышечном синапсе, но и в ЦНС, что объясняет положительное влияние этого препарата на мнестические процессы.
Следует обратить внимание на чрезвычайно важное, хотя и умеренно выраженное свойство Нейромидина — способность блокировать натриевую проницаемость мембраны. С этим эффектом связаны его седативные и анальгетические свойства. Кроме того, препарат обладает антиаритмическим эффектом.
Прозерин и Нейромидин метаболизируются в печени, а выводятся в основном за счет почечных механизмов. В неизмененном виде выделяется 50% Прозерина и 3,7% Нейромидина, что свидетельствует об ускоренном метаболизме Нейромидина. Начальный эффект от введения Прозерина отмечается, в среднем, через 10–15 минут, а от введения Нейромидина — через 15–20 минут. Продолжительность действия Нейромидина — 3–5 часов, что связано с длительной блокадой калиевой проницаемости мембраны, а Прозерин заканчивает свое действие через 2–3 часа после его введения.
Прозерин в результате воздействия на Н-холинорецепторы приводит к значительному повышению силы сокращения скелетных мышц и благодаря этому показан к применению в первую очередь у больных с миастенией и миастеническим кризом. Также препарат используется в неврологической практике при параличах, парезах, возникающих после механических травм, остаточных явлениях перенесенного менингита, полиомиелита, энцефалита и при невропатиях.
Благодаря мускариноподобным эффектам Прозерин используется для устранения послеоперационной атонии кишечника и мочевого пузыря, изредка при слабости родовой деятельности, иногда в офтальмологической практике при открытоугольной форме глаукомы.
В связи с тем что Прозерин облегчает передачу возбуждения в вегетативных ганглиях, он показан при отравлениях ганглиоблокаторами. Кроме того, Прозерин эффективен при передозировке миорелаксантов антидеполяризующего действия (мышечная слабость, угнетение дыхания).
Показания к применению Нейромидина шире, так как в его основе лежит биологически выгодная комбинация двух молекулярных эффектов (блокада калиевой проницаемости мембраны и ингибирование холинэстеразы) и он стимулирует структурные образования ЦНС. Это не только поражения периферической нервной системы: нейропатии, полинейропатии, миелополирадикулоневриты, миастения и миастенический синдром, рассеянный склероз и другие формы демиелинизирующих заболеваний нервной системы (в комплексной терапии), но и бульбарные параличи и парезы при органических поражениях ЦНС в восстановительном периоде, а также нарушения памяти, внимания, мотивации и инициативы различного генеза, дезориентация, эмоциональная лабильность при сенильной деменции, болезнь Альцгеймера и другие формы слабоумия позднего возраста, энцефалопатии травматического, сосудистого и другого генеза, сопровождающиеся не только нарушением памяти, но и двигательных функций.
Нейромидин, также как и Прозерин, используется при атонии кишечника и интоксикации антихолинергическими средствами.
Сопоставление клинического эффекта Нейромидина и Прозерина при миастении показало, что Прозерин по своему антихолинэстеразному действию значительно превосходит Нейромидин. Добиться полной компенсации двигательных расстройств у пациентов с миастенией можно, только используя Прозерин. Однако его применение ограничивает большое число побочных эффектов.
Вместе с тем отмечена эффективность Нейромидина в комплексном лечении больных миастенией и миастеническими синдромами, так как он дополняет действие Прозерина. Оба препарата улучшают передачу возбуждения в нервно-мышечном синапсе, и хотя Нейромидин слабее по антихолестеразной активности, но выигрывает в длительности действия.
Нейромидин приводит к урежению миастенических кризов, более быстрому наступлению и увеличению длительности ремиссий, повышению сократительной активности мышц, улучшению общего состояния больных.
По данным Российского миастенического центра Нейромидин продемонстрировал максимальную эффективность у пациентов с миастеническим синдромом Ламберта–Итона в отличие от Прозерина, при этом отмечено относительное снижение выраженности вегетативно-трофических нарушений.
И все же достоверным дифференциально-диагностическим тестом в диагностике острых состояний при миастении, а именно миастенических и холинергических кризах, является введение Прозерина. Проба с Прозерином при миастеническом кризе позитивная и проявляется в увеличении силы мышцы или ее полном восстановлении, а при холинергическом кризе — негативная.
Клинические исследования показали преимущества Нейромидина по сравнению с Прозерином в комплексной терапии нейропатии лицевого нерва, травматических невропатий и плексопатий. Лечение Нейромидином можно начать в дебюте заболевания, а Прозерин назначается спустя 10 дней, учитывая риск постпаралитической контрактуры. Восстановление функции мышц происходит быстрее при использовании Нейромидина. Отчетливый положительный эффект достигнут у 89,5% больных с поражением лицевой мускулатуры, у 80% пациентов с травматическими невропатиями и плексопатиями. Полное восстановление утраченной функции конечностей зарегистрировано у 40% больных. Причем активизация реиннервации больных подтверждается положительной динамикой показателей электромиографии (ЭМГ). Следует подчеркнуть, что признаков контрактуры конечностей или мимической мускулатуры ни у одного из наблюдаемых пациентов не отмечено. Несмотря на позднее назначение Прозерина, у нескольких пациентов все же наблюдалось появление патологических синкинезий на 16–22 день заболевания.
Нейромидин в лечении больных демиелинизирующими заболеваниями нервной системы (рассеянный склероз, боковой амиотрофический склероз) продемонстрировал положительный эффект на ранних стадиях заболевания у 40% больных. Конечно, лечебный эффект Нейромидина менее выражен, но он более длительный, чем у Прозерина. Под влиянием Нейромидина происходит восстановление проведения возбуждения в спинном мозге и периферической нервной системе, что проявляется уменьшением выраженности парезов и параличей, расстройств чувствительности, повышением силы в пораженных группах мышц.
Эффективное лечение сенсорных симптомов не зависимо от патогенеза поражения периферических нервов, обусловлено блокированием ионных каналов аксолеммы и нейрональных мембран, в основном калиевых и частично натриевых, что выгодно отличает Нейромидин от Прозерина.
Анальгетическое действие Нейромидина, блокирующего ионные каналы, достигается торможением эктопических разрядов и эфаптической передачи возбуждения в поврежденном нерве, в регенерирующих аксональных ветвлениях в результате коллатерального спраутинга, а также снижением возбудимости центральных нейронов.
Нейромидин входит в группу препаратов, используемых в качестве патогенетического лечения диабетической хронической дистальной симметричной сенсомоторной полинейропатии. Патогенетические механизмы диабетической полинейропатии приводят к прогрессивной потере миелинизированных волокон, в результате чего проведение нервного импульса замедляется, а во вновь образующихся в результате регенеративного спраутинга «новых» синапсах нервно-мышечная передача не эффективна. Исследование Нейромидина в лечении диабетической полинейропатии продемонстрировало уменьшение выраженности сенсорных симптомов, особенно парестезий, крампи, стреляющей боли с подтверждением результатами ЭМГ (увеличение амплитуды М-ответа).
Нейромидин в отличие от Прозерина, который фактически не проникает через гематоэнцефалический барьер, имеет способность стимулировать структурные образования ЦНС, в частности когнитивные процессы.
Когнитивные расстройства являются ведущими клиническими проявлениями хронической недостаточности мозгового кровообращения. Существует мнение, что мнестические расстройства связаны с центральным холинергическим дефицитом, а глютаматная экзайтотоксичность, возникающая при этом, является вторичной.
У пожилых людей нарушаются как пресинаптический, так и постсинаптический компоненты центральных холинергических синапсов, расположенных в коре больших полушарий и в гиппокампе, в результате чего уменьшается высвобождение ацетилхолина и снижается чувствительность к нему в пожилом возрасте.
После курса Нейромидина у пациентов с прогрессирующей сосудистой лейкоэнцефалопатией улучшалась кратковременная память, уменьшались проявления астенического синдрома, улучшались показатели когнитивных функций.
У больных сенильной деменцией альцгеймеровского типа и мультиинфарктной деменции, получавших Нейромидин, было выявлено уменьшение поведенческих нарушений, улучшение когнитивных функций, речи и социальной адаптации.
Независимым фактором нарушения когнитивных функций и развития деменций является сахарный диабет. Проведенные клинические исследования позволяют рассматривать Нейромидин как препарат первой линии лечения больных сахарным диабетом с умеренными когнитивными нарушениями и деменцией.
У больных с последствиями умеренного или легкого мозгового инсульта на фоне лечения Нейромидином возрастала физическая активность, интеллектуальные функции, увеличивался объем памяти. В восстановительном периоде ишемического инсульта средней тяжести у пациентов наблюдалось значительное уменьшение степени пареза конечностей без нарастания мышечного тонуса, бульбарных параличей и парезов, регресс расстройств чувствительности, вегетативно-трофических нарушений. У 70–80% больных с сосудистыми и другими органическими поражениями головного мозга в остром и отдаленном периодах отмечался быстрый регресс нарушений памяти, внимания, праксиса, шаткости при ходьбе, уменьшение астенических явлений, улучшение сна, повышение интеллектуальных возможностей больного и его работоспособности. Почти у всех больных с афазией отмечено улучшение речевых функций.
Оба препарата производятся в таблетированной (Прозерин по 15 мг, Нейромидин по 20 мг) и ампулированной форме по 1 мл (Прозерин 0,05%, в глазной практике используется 0,5% раствор, Нейромидин 1,5% и 0,5% раствор). Прозерин выпускается также в форме порошка, гранулах (для детей). Его применяют внутрь и подкожно. Взрослым Прозерин назначают внутрь за 30 мин до еды в порошках или таблетках по 10–15 мг 2–3 раза в день, подкожно вводят по 0,5 мг (1 мл 0,05% раствора) 1–2 раза в день, в глаза по 1–2 капли 0,5 % раствора 1–4 раза в сутки.
При развитии миастенического криза у взрослых Прозерин вводят внутривенно — 0,5–1 мл 0,05% раствора, затем подкожно в дозе 1,5–2,5 мл в зависимости от веса больного. Лечение миастении Прозерином проводят длительно. При других заболеваниях курс лечения продолжается 25–30 дней; при необходимости его повторяют после 3–4-недельного перерыва.
Нейромидин используют внутрь независимо от приема пищи, подкожно и внутримышечно. При поражениях периферической нервной системы — по 20 мг 2–3 раза в день в течение 30–40 дней. Курсы лечения повторяют с перерывом 1–2 месяца. При острых невритах используют по 10–20 мг в день в течение 10–15 дней, при хронических невропатиях длительность лечения увеличивают до 20–30 дней. При необходимости курсы повторяют 2–3 раза с интервалом 2–4 недели до достижения максимального эффекта.
При миастении, миастенических синдромах, демиелинизирующих поражениях нервной системы дозу Нейромидина можно увеличить до 20–40 мг 5–6 раз в сутки. Максимальная суточная доза — 180–200 мг. Купирование миастенического криза — по 5–15 мг 1–2 раза в сутки подкожно или внутримышечно.
Наибольший эффект для стимулирования когнитивных процессов получен при использовании средних (50–60 мг/сут) и высоких доз (80–120 мг/сут) Нейромидина.
При болезни Альцгеймера и других формах слабоумия требуется индивидуальный подбор режима дозирования Нейромидина. Максимальная суточная доза может достигать 200 мг; длительность курса терапии — от 4 месяцев до 1 года. При необходимости применения высоких доз целесообразно применение 4–5 раз в сутки с интервалом 2–3 ч.
В восстановительном периоде ишемического инсульта легкой и средней тяжести используют 1,5% раствор Нейромидина внутримышечно в течение 14 дней по 1 мл в день.
При черепно-мозговой травме Нейромидин назначают от 40 мг до 120–160 мг в сутки. Курс лечения составляет 30–40 дней, 4 раза в год с интервалом месяц.
Для лечения и профилактики атонии кишечника — по 15–20 мг 2–3 раза в сутки в течение 1–2 нед.
Противопоказаниями к применению Прозерина и Нейромидина являются: гиперчувствительность, эпилепсия, экстрапирамидные нарушения с гиперкинезами, бронхиальная астма, стенокардия, выраженная брадикардия, беременность и период лактации.
Число противопоказаний и побочных эффектов у Прозерина больше по сравнению с Нейромидином, что связано с его сильной антихолинэстеразной активностью. Прозерин нельзя использовать при выраженном атеросклерозе, органических заболеваниях сердца и сосудов, тиреотоксикозе, язвенной болезни желудка и двенадцатиперстной кишки, перитоните, воспалительных процессах в брюшной полости, механической обструкции желудочно-кишечного тракта и мочевыводящих путей, аденоме предстательной железы, периоде острого заболевания, интоксикации.
Следует соблюдать осторожность при использовании нейромидина у пациентов с заболеваниями сердечно-сосудистой системы, тиреотоксикозом, язвенной болезнью желудка, однако эти состояния не являются противопоказаниями к его применению.
При применении Прозерина возможно появление гиперсаливации, обильного потоотделения, спастического сокращения и усиления перистальтики кишечника, тошноты, рвоты, метеоризма, диареи, учащенного мочеиспускания. Кроме того, могут развиться головная боль, головокружение, слабость, потеря сознания, сонливость, миоз, нарушения зрения, артралгии, аллергические реакции вплоть до анафилаксии. Со стороны сердечно-сосудистой системы: замедление сердечного ритма, аритмии, AV-блокада, неспецифические изменения на ЭКГ, снижение артериального давления, остановка сердца. Со стороны дыхательной системы: одышка, бронхоспазм, угнетение дыхания до остановки. Благодаря никотиноподобным эффектам Прозерин может вызвать тремор, спазмы и подергивание скелетной мускулатуры, включая фасцикуляции мышц языка, дизартрию, судороги.
Для снятия побочных явлений уменьшают дозу Прозерина или прекращают его прием, при необходимости вводят холинолитические препараты.
При парентеральном введении больших доз Прозерина необходимо предварительное или одновременное назначение атропина для нивелирования побочных мускариновых эффектов. При развившихся судорогах используют Сибазон.
Нейромидин, в сравнении с Прозерином, хорошо переносим, побочные эффекты возникают редко, слабо выражены и, как правило, не требуют отмены препарата, в связи со слабой антихолестеразной активностью и быстрым выведением, что препятствует кумуляции и возникновению побочных эффектов.
Кроме того, при приеме Нейромидина, в отличие от Прозерина, не наблюдается побочных эффектов, обусловленных действием на Н-холинергические синапсы, — фасцикуляции, крампи. Побочные эффекты Нейромидина связаны с активацией М-холинергических синапсов. В основном это диспептические явления (тошнота, усиление перистальтики, учащение частоты стула без диареи), которые самостоятельно регрессируют и не требуют прекращения лечения.
Появление других побочных явлений, таких как головокружение, гиперсаливация и брадикардия, кожно-аллергические реакции, требует коррекции дозы или короткого 1–2-дневного перерыва в лечении.
Для предотвращения побочных нежелательных явлений необходимо титровать препарат до лечебной дозы, чтобы организм адаптировался к усилению холинергической активности.
В связи с тем что Нейромидин может оказывать седативное действие, во время лечения необходимо воздерживаться от занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания, в том числе и вождения автотранспорта. На время лечения следует исключить прием этанола, так как возможно усиление неблагоприятных побочных действий.
Нейромидин и прозерин, несмотря на общее антихолинэстеразное действие, являются препаратами, обладающими неоднородными фармакологическими свойствами, что обуславливает их круг применения. В связи с высокой антихолинэстеразной активностью, Прозерин обладает рядом выраженных побочных эффектов и остается препаратом выбора при миастении, миастенических кризах и демиелинизирующих заболеваниях. Нейромидин обладает более широким спектром фармакологической активности, в том числе и стимулирующим действием на структурные образования ЦНС, поэтому с успехом применяется как при лечении заболеваний периферической нервной системы, так и при органических поражениях ЦНС. Несомненным достоинством является хорошая переносимость и отсутствие выраженных побочных эффектов, что позволяет его длительно применять у пожилого контингента пациентов, страдающих многочисленными сопутствующими заболеваниями.
По вопросам литературы обращайтесь в редакцию.
З. А. Суслина, доктор медицинских наук, профессор, академик РАМН
М. Н. Шаров, доктор медицинских наук, профессор
О. А. Степанченко, кандидат медицинских наук
МГМСУ, Москва