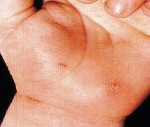
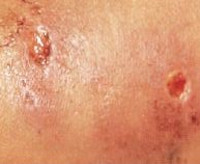
бартонеллез кошек что это такое
Гемобартонеллёз кошек
Гемобартонеллез – кровепаразитарное заболевание кошек, по клиническим признакам схожее с пироплазмозом у собак.
Распространенность заболевания зависит от климатических условий. Страны с прохладным климатом имеют 0-1% инфицированных животных, в теплом климате – до 60-80%, в России распространенность гемобартенеллеза составляет в среднем 4-5%.
Возбудителем инфекционной анемии являются внутриклеточные грамотрицательные бактерии рода Bartonella. Они требовательны к питательной среде, поэтому паразитируют в эритроцитах, эндотелиальных клетках, создавая длительную бактериемию. У млекопитающих выделено 34 вида бартонелл, 6 видов паразитируют у кошек (B.henselae, B.clarridgeiae, B.koehlerae, B.quintana, B.bovis, B.vinsonii supsp berkhoffii). Наиболее часто распространены B.henselae и B.clarridgeiae, которые являются возбудителями у человека болезни «кошачьих царапин» (доброкачественный лимфоретикулез).
Основные пути передачи
Другие предположительные пути передачи (трансплацентарный, при содержании зараженных животных со здоровыми) подвергнуты сомнениям. Экспериментальное изучение путей передачи гемобартонеллеза не подтвердило перекрестное заражение при отсутствии переносчика. Иными словами, человек не может заразиться бартонеллами от инфицированной кошки, если нет блох и их фекалий на когтях.
| Вид бартонеллы | Природный резервуар | Переносчик | Случайный хозяин |
|---|---|---|---|
| Bartonella henselae | кошка | Ctenocephalides felis | человек, собака |
| Bartonella clarridgeiae | кошка | Ctenocephalides felis | человек, собака |
| Bartonella koehlerae | домашние и дикие кошачьи | Ctenocephalides felis | человек, собака |
| Bartonella quintana | человек | Pediculus humanus | кошка, собака, обезьяна |
| Bartonella bovis | домашний скот | кровососущие мухи, клещи | кошка, собака, человек |
| Bartonella vinsonii supsp berkhoffii | койот, лиса, собака | Rhipicefalus sanquineus | человек, собака |
Патогенез гемобартонеллёза
Переносчик заражается бартонеллами при укусе инфицированного животного. В кишечнике блохи (клеща) происходит их размножение, выделяются с фекалиями в окружающую среду (в том числе на шерсть кошки). При травмах, царапинах бартонеллы попадают под кожу, где предположительно заглатываются тканевыми макрофагами (моноциты), размножаются в них и мигрируют в кровеносное русло. Часть бартонелл проникает в эндотелиальные клетки внутренней поверхности сосудов, часть – в эритроциты, где происходит дальнейшее размножение. Цикл повторяется, когда инфицированную кошку вновь кусает переносчик.
Бартонеллы имеют ряд особенностей и приспособлений, которые позволяют избежать выраженного иммунного ответа у животного. Во-первых, локализуются внутри эритроцитов, не вызывая гемолиз, что не дает обнаружить их антигены лимфоцитами. Во-вторых, они способны изменять и скрывать патоген-ассоциированный белковый паттерн на поверхности своей мембраны, что осложняет их распознование дендритными клетками. Последние участвуют в распозновании чужеродных антигенов. В-третьих, бартонеллы секретируют интерлейкин-10, который угнетае выработку Т-лимфоцитов (хелперов), моноцитов, дендритных клеток. Как результат, снижение выработки защитных иммунных клеток приводит к длительной и выраженной бактериемии (2 года и более).
Бартонеллез
Бартонеллезы – это группа заболеваний, вызываемых бактериями из рода Bartonella, протекающих с преимущественным поражением эндотелиальных клеток и эритроцитов. Клинические проявления могут быть различными: от легких и местных (сыпь, лимфаденопатия, конъюнктивит) до распространенных системных нарушений (лихорадка, анемия, септическая бактериемия, эндокардит, менингит, миелит). Диагностика бартонеллеза основана на обнаружении самого возбудителя, а также его антигенов и антител в крови пациента. Терапия проводится антибактериальными препаратами (тетрациклины, макролиды, фторхинолоны), по показаниям дополняется симптоматическим лечением (жаропонижающие средства, дезинтоксикационная терапия).
МКБ-10
Общие сведения
Группа бартонеллезов включает в себя фелиноз, траншейную лихорадку, болезнь Карриона, бациллярный ангиоматоз, бартонеллезный синдром с бактериемией и эндокардит, пелиозный гепатит /спленит, хроническую лимфаденопатию. Хронологически первой среди всего многообразия клинических вариантов инфекции была изучена болезнь Карриона, поэтому бартонеллез обычно отождествляется именно с ней. Эндемичными районами для заболевания являются северо-западные территории Южной Америки. Это связано с ареалом обитания переносчика бактерии – москитов флеботомусов. Пик заболеваемости бартонеллезом приходится на сезон дождей, когда комары особенно активны. Другие формы инфекции не имеют четкой географической локации, что объясняется повсеместной распространенностью бартонелл на планете.
Причины
Бартонеллы являются грамотрицательными аэробными палочками. Способны вызывать бактериемию, в организме хозяина персистируют внутри эритроцитов. Быстро погибают под воздействием обычных дезинфицирующих средств. Возбудитель болезни Карриона – B. bacilliformis. Кроме этого, патогенными для человека являются B. henselae (вызывает фелиноз, бациллярный ангиоматоз), B. quitana (обусловливает развитие траншейной лихорадки, бациллярного ангиоматоза, бактериемии и эндокардита), B. vinsonii и B. elizabethae (являются причиной бактериемии, эндокардита), B.grahamii (вызывает нейроретинит), B. washoesis (способствует развитию миокардита).
В организм человека бактерии проникают через укусы комаров, клещей, вшей или микроповреждения кожи. Резервуаром инфекции является человек, больной острыми формами, либо бессимптомный бактерионоситель. Частота бессимптомной бактериемии у носителей инфекции достигает 50%. Восприимчивость к бартонеллезу у жителей эндемичных районов высокая. Антисанитарные условия, скученность людей способствуют увеличению частоты инфицирования.
Патогенез
В месте проникновения возбудителя образуется первичный аффект – папула, везикула или пустула. Далее с током лимфы возбудитель проникает в лимфатические узлы – развивается лимфаденопатия. При преодолении лимфатического барьера патоген поступает в кровь – наступает бактериемия. Наиболее чувствительными к бартонеллам являются эритроциты и эндотелиальные клетки сосудов, костный мозг, клапаны сердца. Активное размножение возбудителя в эритроцитах и их разрушение вызывает развитие гемолитической анемии.
При острых процессах в клетках эндотелия преобладают некротические изменения, стенка сосудов инфильтрируется лейкоцитами и макрофагами с образованием гранулем, явления пролиферации выражены незначительно. В слизистых оболочках, коже появляются мелкие кровоизлияния. Для хронического течения бартонеллеза характерно образование новых мелких сосудов с формированием ангиоэндотелиом. При состоятельности системы иммунитета образуются антитела с последующей элиминацией возбудителя. В случае иммунодефицитных состояний происходит хронизация процесса с длительной персистенцией бартонелл в крови. Отсутствие лечения в такой ситуации может привести к летальному исходу. У выздоровевших пациентов формируется стойкий иммунитет.
Классификация
Бартонеллез представляет собой группу разноплановых заболеваний. Единой классификации нозологий нет, поскольку бартонеллы остаются не до конца изученными бактериями, появляются новые сведения о вызываемых ими поражениях; кроме того, одни формы могут перетекать в другие. На сегодняшний день известны следующие заболевания, вызываемые бартонеллами:
Симптомы бартонеллеза
Болезнь Карриона является стадийным процессом. Может протекать в виде острой (лихорадка Оройя) или хронической фазы (перуанская бородавка). Возможно одновременное развитие клиники обеих стадий. В классическом варианте хроническая стадия сменяет острую через 1-2 мес.
Инкубационный период бартонеллеза от 10 до 120 дней (в среднем около 2-х месяцев). При развертывании клинической картины появляется лихорадка неправильного типа, подъем температуры до 39–40°С сопровождается ознобом, а снижение – потливостью, напоминая малярию. Пациенты жалуются на головные боли, недомогание, боли в животе, суставах, мышцах. Характерна выраженная бледность за счет анемии. Могут появляться различные симптомы нарушения неврологического статуса вплоть до развития комы. На коже, слизистых оболочках возникают мелкие кровоизлияния. Увеличивается печень, селезенка, лимфатические узлы. При благоприятном исходе заболевания человек выздоравливает, однако без лечения летальность составляет от 40 до 90%.
При сохранении возбудителя в организме бартонеллез переходит в латентную стадию с последующей реактивацией и развитием хронической фазы ‒ перуанской бородавки. Вновь повышается температура. На теле появляется папулезная сыпь, которая со временем трансформируется в узелки от 3 мм до нескольких сантиметров в диаметре. Чаще всего высыпания локализуются на лице, шее, конечностях. Наблюдается поражение слизистых оболочек рта, влагалища, желудочно-кишечного тракта и др. Узлы могут кровоточить и изъязвляться с присоединением вторичной инфекции. При благоприятном течении через 1-2 мес. наступает выздоровление, узлы разрешаются без рубца.
Осложнения
Наиболее распространенным осложнением является присоединение вторичной сальмонеллезной инфекции. В случае развития септической формы заболевания резко увеличивается летальность. Кроме того, возможно инфицирование изъязвлений высыпаний при перуанской бородавке, в таком случае раны заживают с рубцом. При поражении слизистых возникают кровотечения. Бактериемия и полиорганные поражения способствуют развитию сепсиса, который обычно сопровождается ДВС-синдромом. Регургитация высокой степени на сердечных клапанах ведет к несостоятельности компенсаторных возможностей сердца, что требует хирургической замены клапана. Поражения ЦНС приводят к неврологическому дефициту, бациллярный ангиоматоз способствует угнетению функций печени.
Диагностика
При подозрении на бартонеллез необходима консультация терапевта, инфекциониста, дерматолога, в случае поражения нервной системы – невролога, развития гнойных осложнений – хирурга. Во время физикального обследования отмечается бледность, на коже – первичный аффект с регионарной лимфаденопатией, при пальпации – увеличенная печень, селезенка. В диагностике используются следующие лабораторно-инструментальные методы:
Дифференциальная диагностика бартонеллеза проводится с кожной формой туберкулеза, ангиосаркомой, опухолью кожи, в частности миеломой. Более распространенную нозологию – фелиноз – стоит разграничивать с атипичным микобактериозом, сифилисом, туляремией, лимфомой. Дифдиагностику бациллярного ангиоматоза необходимо проводить с саркомой Капоши, ангиомой, плоскоклеточным и базальноклеточным раком. Эндокардит и бактериемию необходимо различать с аналогичными заболеваниями, вызываемыми другими патогенами.
Лечение бартонеллеза
Лечение осуществляется в инфекционном стационаре. Необходимо соблюдение постельного режима. Проводится этиотропная терапия антибактериальными препаратами. Поскольку возможно последующее вторичное присоединение сальмонеллеза, рационально использовать ципрофлоксацин или хлорамфинекол в сочетании с β-лактамным антибиотиком. Препаратами резерва являются макролиды, тетрациклины, рифампицин. При необходимости назначается симптоматическое лечение (дезинтоксикационная терапия, жаропонижающие препараты, гепатопротекторы, переливание эритроцитарной массы). На инфицированные кожные элементы после промывания антисептиками накладывают повязки с антибактериальными мазями.
Прогноз и профилактика
В острой фазе при отсутствии сопутствующей патологии и своевременно начатом лечении прогноз благоприятный. Однако при иммуносупрессии с массивной бактериемией возможно развитие бациллярного ангиоматоза, поражений нервной системы, декомпенсации сердечной деятельности за счет поражения клапанов. В стадии перуанской бородавки летальные случаи практически не описаны, смертность связана с присоединением инфекции. Специфическая профилактика бартонеллеза не разработана. Индивидуальные меры защиты предусматривают применение репеллентов, антимоскитных сеток.
БОЛЕЗНЬ КОШАЧЬЕЙ ЦАРАПИНЫ
Несмотря на то что первое клиническое описание болезни кошачьей царапины (БКЦ) было дано R. Debre и соавт. более 50 лет назад, до сих пор вопрос об этиологии этого заболевания остается предметом дискуссий и специальных исследований.
Несмотря на то что первое клиническое описание болезни кошачьей царапины (БКЦ) было дано R. Debre и соавт. более 50 лет назад, до сих пор вопрос об этиологии этого заболевания остается предметом дискуссий и специальных исследований. Поскольку выделить возбудитель от больных не удавалось в течение длительного времени, первоначально предполагалась вирусная или хламидийная этиология заболевания. Первые убедительные сведения об идентификации возбудителя БКЦ были получены только в 1983 г., когда исследователи, используя метод окраски по Warthin-Starry (метод серебрения), обнаружили в ткани пораженных лимфатических узлов у 29 из 34 больных БКЦ мелкие полиморфные грамотрицательные бациллы, которые удалось культивировать лишь в 1988 г. Именно этот микроорганизм первоначально был признан возбудителем БКЦ и получил название Alipia felis.
Тем не менее многочисленные последующие исследования не подтвердили четкой взаимосвязи развития БКЦ с A. felis: в большинстве случаев у больных в пораженных тканях не только не обнаруживался указанный возбудитель, но и в сыворотке крови не выявлялись антитела к нему. Более того, из ткани пораженных лимфоузлов был изолирован еще один возбудитель — Bartonella henselae. Методом ПЦР с применением специфических праймеров к Bartonella spp. и A. felis у больных, у которых кожный тест на БКЦ оказался положительным, было установлено, что в 96% случаев у них обнаруживалась ДНК Bartonella, тогда как ДНК A. felis не выявлялась ни в одном случае (A. Bergmans et al., 1995). Сходные данные, подтверждающие ключевую роль B. henselae в развитии БКЦ, были получены и другими исследователями при использовании непрямой реакции флюоресцирующих антител.
В то же время первоначальный факт обнаружения A. felis в пораженных лимфатических узлах игнорироваться не должен. На сегодняшний день некоторые исследователи допускают, что A. felis способен вызывать заболевание, которое по своей клинической картине может напоминать БКЦ.
Болезнь кошачьей царапины (лимфоретикулез доброкачественный) относится к группе бартонеллезов и характеризуется как нетяжелое самокупирующееся заболевание с развитием одностороннего лимфаденита, регионарного по отношению к месту инокуляции возбудителя, и только в редких случаях возможна диссеминация возбудителя с поражением центральной нервной системы и висцеральных органов.
B. henselae характеризуется как небольшая плеоморфная, грамотрицательная бацилла, весьма требовательная к условиям культивирования (растет только на средах с 5% кровяного агара при температуре от 35 до 37°С, с 5—10% углекислого газа и 40-процентной влажностью). Кроме этого, колонии первичной культуры растут медленно и становятся видимыми только после 9—15 дней роста. При последующем пассаже рост колоний ускоряется. Идентификация выделенного возбудителя проводится с использованием специфических антисывороток, определением профиля жирных кислот клеточной стенки или молекулярно-генетическим методом. С помощью этого метода было идентифицировано два генотипа B. henselae, хотя до сих пор четкой зависимости между генотипами возбудителя и особенностями клинического течения вызываемых ими заболеваний не установлено.
B. henselae на сегодняшний день рассматривается как основной возбудитель БКЦ, однако у 5—15% больных с диагнозом, установленным на основании клинико-эпидемиологических данных, даже с помощью существующих современных методов лабораторной диагностики этиологическое значение B. henselae в развитии заболевания не подтверждается.
Один из необъяснимых парадоксов, связанных с B. henselae: в последние годы установлено, что данный возбудитель ответственен за развитие не только БКЦ, но и некоторых других заболеваний.
БКЦ имеет широкое географическое распространение и встречается практически повсеместно. Основным естественным резервуаром B. henselae являются кошки, инфицированность которых в значительной степени определяет распространенность БКЦ (K. M. Zangwill et al., 1993). По данным некоторых исследователей, у более чем 50% домашних и диких кошек обнаруживается бактериемия, обусловленная B. henselae. В ходе исследования, проведенного в США, установлено, что наиболее высокий процент инфицированности кошек и, соответственно, заболеваемости БКЦ среди людей регистрируется в южных штатах. Большинство исследователей подчеркивают особую роль котят в передаче возбудителя, указывая, что у взрослых кошек редко выявляется бактериемия B. henselae за счет наличия у них специфических антител, свидетельствующих о длительности их инфицирования. Особенностью течения бартонеллеза у кошек является его продолжительность (месяцы, годы) и бессимптомность (даже в случае подтверждаемой бактериемии).
В циркуляции B. henselae среди кошек исключительную роль играют блохи (Ctenocephalides felis). Экспериментальным путем было установлено, что при отсутствии блох инфицирования здоровых кошек не происходит.
B. henselae обнаруживается в кишечнике блох и их испражнениях в течение 9 дней после инфицирования, что свидетельствует о его репликации и персистенции в организме блох. Кроме этого, экспериментально была установлена возможность инфицирования кошек путем внутрикожной инокуляции инфицированных испражнений блох, в то же время оральное введение кошкам инфицированных блох и их испражнений к сероконверсии не приводило. Роль блох в передаче возбудителя от кошек к человеку в настоящее время категорически не отрицается. В последние годы исследователями в США и Италии (Y. O. Sanogo et al., 2003) молекулярно-генетическими методами было продемонстрировано, что ДНК B. henselae может обнаруживаться в иксодовых клещах, хотя их роль в качестве вектора передачи возбудителя БКЦ по-прежнему не изучена.
«Травматический» контакт с кошками (царапины, укусы) весьма характерен для БКЦ и отмечается более чем у 90% заболевших. Установлено, что «резервуаром» B. henselae могут быть и собаки, однако достоверно подтвержденных случаев заражения от них людей пока не описано.
Эпидемиологические исследования показывают, что в сыворотке крови около 20% владельцев кошек и 3–4% общей популяции людей обнаруживаются антитела к B. henselae. Семейные случаи заболевания БКЦ не столь типичны и регистрируются менее чем у 5% пациентов. Хотя БКЦ может развиваться в любом возрасте, чаще заболевают молодые люди (до 18 лет).
Передача возбудителя БКЦ реализуется главным образом контактным путем через царапины, укусы или слюну инфицированных кошек. Подъем заболеваемости, как правило, отмечается с конца лета, что объясняется особенностями жизненного цикла у кошек и блох.
Поскольку возбудитель БКЦ был идентифицирован относительно недавно, многие аспекты, касающиеся патогенеза заболевания, до сих пор недостаточно изучены. Характер развивающегося инфекционного процесса, обусловленного действием B. henselae, в значительной степени зависит от иммунного статуса человека: в тех случаях, когда заболевание развивается у иммунокомпетентных пациентов, диссеминация возбудителя отсутствует, и процесс преимущественно ограничивается локальными или регионарными поражениями. В частности, БКЦ в большинстве случаев проявляется развитием регионарной лимфаденопатии. Поражение висцеральных органов описано только в отдельных случаях (Dunn et al., 1997), а бактериемия у иммунокомпетентных пациентов регистрируется исключительно редко (Slater et al., 1990). Напротив, у иммунокомпрометированных пациентов для инфекции B. henselae типично развитие бактериемии и других системных поражений, включая бациллярный ангиоматоз и бациллярный пелиозный гепатит, а у лиц с врожденными и приобретенными аномалиями клапанов сердца — эндокардит (Raoult et al., 1996).
Гистологические изменения в пораженных лимфатических узлах характеризуются пролиферацией гистиоцитов и B-лимфоцитов, приводящей к образованию гранулем с последующей нейтрофильной инфильтрацией и развитием центрального или звездчатого некроза.
Хотя B. henselae и считается одним из наиболее вероятных возбудителей БКЦ, тем не менее, согласно современным наблюдениям, данный возбудитель ответственен за развитие ряда других патологических состояний человека (табл. 1). При этом иммунный статус больных рассматривается как ключевой фактор, определяющий характер формирующегося заболевания, хотя известны случаи, когда даже у лиц с ВИЧ-инфекцией в стадии СПИДа БКЦ протекала в типичной форме.
 |
| Таблица 1. Заболевания человека, вызываемые B. henselae |
Инкубационный период у больных с БКЦ может варьировать в достаточно широких пределах — от 3 до 20 дней и более, составляя в среднем 1–2 нед. Хотя общепринятой клинической классификации БКЦ нет, чаще всего выделяют типичную и атипичные формы заболевания (табл. 2), что определяется по доминирующему в клинической картине болезни синдромокомплексу.
В типичных случаях БКЦ проявляется развитием первичного аффекта и регионарного (к месту входных ворот инфекции) лимфаденита. Локализация первичного аффекта определяется местом первичной инокуляции возбудителя, а именно местом нанесения кошкой царапин и укусов. По истечении нескольких дней (от 3 до 10), когда нанесенные кошкой повреждения кожи уже заживают, в месте входных ворот формируется папула, которая, как правило, трансформируется в везикулу и далее в пустулу, а после вскрытия — в язвочку, покрытую корочкой. В некоторых случаях пустула может подсыхать без образования язвочки. В диаметре размер формирующейся папулы, как правило, составляет от 1–2 до 5 мм. Частота выявления первичного аффекта у больных БКЦ, по данным различных исследователей, может колебаться от 25 до 94%. Кожные проявления сохраняются в течение 1—3 нед и спонтанно разрешаются.
Регионарный лимфаденит является одним из наиболее постоянных и характерных клинических признаков БКЦ (табл. 3) и сохраняется в течение длительного времени: от 7 до 60 дней, а в отдельных случаях до 1 года и даже 3 лет. В большинстве случаев лимфаденит разрешается в течение 1—4 мес. Нередко он оказывается практически единственным проявлением БКЦ. В большинстве случаев (85%) у больных выявляются одиночные лимфатические узлы, реже множественные, в границах одной анатомической области. Несмотря на то что у больных регистрируется увеличение лимфатических узлов, осуществляющих дренаж места первичной инокуляции возбудителя, развитие лимфангоита не характерно для БКЦ. У 1/3 пациентов могут определяться увеличенные лимфатические узлы разных анатомических областей, хотя генерализованная лимфаденопатия встречается достаточно редко. Размером увеличенные лимфатические узлы чаще бывают от 1 до 5 см, в некоторых случаях до 8—10 см. При пальпации лимфатические узлы умеренно болезненные. Хотя они и не спаяны с окружающими тканями, нередко определяется гиперемия кожных покровов над ними. В 10—50% случаев у больных БКЦ развивается нагноение пораженных лимфатических узлов с образованием густого желто-зеленого гноя. В отдельных случаях при посеве гноя на питательные среды удается получить рост стафилококков и другой флоры, хотя роль условно-патогенной флоры (суперинфекция) в нагноении пораженных лимфатических узлов пока не установлена.
Общее состояние больных в большинстве случаев остается удовлетворительным. Только в трети случаев у больных отмечается повышение температуры тела свыше 38,3°С, которое сохраняется около недели и лишь иногда может затягиваться до месяца и более. Среди других клинических проявлений БКЦ могут отмечаться: слабость и недомогание (30%), головная боль (14%), тошнота и рвота (15%), спленомегалия (11%). В случае длительного течения заболевания у больных может наблюдаться потеря веса. Нередко заболевание приобретает волнообразное течение.
Поражение глаз (глазной вариант) при БКЦ регистрируется в том случае, когда местом инокуляции возбудителя служит слизистая оболочка глаз. Клинические проявления заболевания в этом случае будут включать развитие одностороннего поражения в виде язвенно-гранулематозного конъюнктивита, отека век и преаурикулярной лимфаденопатии (синдром Парино). Одновременно у больных могут определяться умеренно увеличенные и болезненные околоушные и шейные лимфатические узлы. К числу других глазных проявлений БКЦ относятся нейроретинит, неврит зрительного нерва и папиллит. Для нейроретинита типично одностороннее острое нарушение остроты зрения, развивающееся на фоне умеренно выраженных явлений интоксикации. При осмотре глазного дна могут выявляться геморрагии, множественные дискретные повреждения, ватоподобные образования, отек и экссудация соска зрительного нерва (симптом «макулярной звезды») (J. B. Reed et al., 1998).
Поражение нервной системы (неврологический вариант) у больных БКЦ выявляется редко (
2% случаев), хотя диапазон клинических проявлений весьма разнообразен: у больных могут выявляться радикулиты, полиневриты, миелит, энцефалопатия, энцефалит, менингит и церебральная атаксия. Характерным признаком поражения нервной системы при БКЦ является то, что они развиваются спустя 1—6 нед (чаще 2–3 нед) от момента появления лимфаденопатии. Для развития энцефалита и менингита типично внезапно возникающее ухудшение состояния больного, сопровождающееся лихорадкой, головной болью, спутанностью сознания и дезориентацией. В некоторых случаях состояние может прогрессивно ухудшаться, вплоть до развития комы. В ликворе у таких больных определяется мононуклеарный плеоцитоз. Только в отдельных случаях у больных после перенесенного энцефалита могут отмечаться резидуальные явления.
Некоторые авторы (P. M. Delahoussaye, B. M. Osborne, 1990), указывая на возможность поражения печени и селезенки при БКЦ, выделяют висцеральный вариант заболевания, для которого характерны длительная волнообразная лихорадка, увеличение размеров печени и селезенки, повышение в сыворотке крови уровней аминотрансфераз, с определением при УЗИ и компьютерной томографии множественных, диффузных, гипоэхогенных дефектов. Довольно часто у таких больных отмечается генерализованная лимфаденопатия.
Кроме этого, в более редких случаях у больных БКЦ могут выявляться абсцесс селезенки, плеврит, эндокардит, пневмония, узловатая эритема, тромбоцитопеническая пурпура, остеомиелит (B. Dzelalija et al., 2001, C. V. Hulzebos et al., 1999).
В типичных случаях первичная диагностика БКЦ не представляет больших сложностей, поскольку основывается на характерных клинико-эпидемиологических данных (табл. 4).
Определенные сложности имеются при лабораторной верификации диагноза, что связано с отсутствием соответствующей лабораторной базы. В зарубежной практике длительное время в качестве основного диагностического критерия БКЦ использовался кожный тест, в котором в качестве аллергена применялся термоинактивированный пунктат, полученный из лимфоузлов больных с установленным (в соответствии с принятыми критериями) диагнозом БКЦ. По данным многих авторов, результативность такого теста достигала 95—98%, однако из-за риска передачи гемоконтактных инфекций использование данного теста ограничено, а кожного теста с использованием очищенных антигенов B. henselae пока не описано.
Микробиологические исследования в широкой практике не применяются ввиду длительности (от 2 до 6 нед) и сложности проведения анализа.
Достаточно информативным способом установления диагноза является биопсия папул и/или пораженных лимфатических узлов с последующим гистологическим исследованием (окрашивание срезов гематоксилин-эозином и серебром — метод Warthin-Starry), позволяющим выявить характерные гистологические признаки поражения и скопление мелких плеоморфных бактерий.
В последние годы большое внимание уделяется разработке специфических иммунологических (ИФА) и молекулярно-генетических (идентификация гена 16S рибосомальной РНК B. henselae) методов обнаружения возбудителя БКЦ в биопсийном материале больного, хотя пока для широкой практики они по-прежнему недоступны.
Дифференциальный диагноз необходимо проводить с заболеваниями, сопровождающимися развитием лимфаденопатии (табл. 5).
Несмотря на то что в редких случаях отмечаются варианты тяжелого течения БКЦ, у иммунокомпетентных лиц прогноз заболевания благоприятный. Повторных случаев и летальных исходов не описано.
Многочисленные клинические наблюдения показывают, что в большинстве случаев БКЦ протекает как самокупирующаяся инфекция, и применение антибактериальной терапии не оказывает существенного влияния на ее течение. Традиционные рекомендации по применению эритромицина (эритромицин-тева, зинерит) и доксициклина (юнидокс солютаб, медомицин, вибрамицин, тетрадокс) основаны на эффективности этих препаратов у больных с ВИЧ-инфекцией при развитии бациллярного ангиоматоза, вызываемого Bartonella quintana, тогда как у больных БКЦ терапевтическая эффективность указанных препаратов не подтверждена ни в одном исследовании. Весьма противоречивыми остаются данные по соответствию чувствительности in vitro возбудителя БКЦ к антибактериальным препаратам и их клинической эффективности. Единственным антибактериальным препаратом, клиническая эффективность которого была установлена в ходе рандомизированного плацебо-контролируемого исследования, является азитромицин (сумамед, хемомицин, азивок, сумазид), назначаемый в течение 5—10 дней. В неконтролируемых исследованиях (A. M. Margileth, 1992) из 18 антимикробных препаратов клиническая эффективность была установлена только при применении рифампицина (бенемицин, р-цин), ципрофлоксацина (ципросан, цифран, ципрова), гентамицина (гентамицин К, гентамицина сульфат) и триметопримсульфаметоксазола (бактрим, септрин). Антибактериальные препараты при БКЦ следует применять у иммунокомпрометированных лиц и при тяжелом течении заболевания, сопровождающегося поражением нервной системы и висцеральных органов.
В случае выявления флуктуации в пораженном лимфатическом узле требуется его пункция и аспирация гноя, что ускоряет последующий процесс склерозирования и рубцевания ткани лимфатического узла и влияет в конечном итоге на выздоровление пациента.
По вопросам литературы обращайтесь в редакцию.
В. А. Малов, доктор медицинских наук, профессор
А. Н. Горобченко, кандидат медицинских наук, доцент
ММА им. И. М. Сеченова, Москва