ишемия мозга лечение у ребенка
Церебральная ишемия головного мозга у новорожденных
Церебральная ишемия – это заболевание, характеризующееся недостаточным поступлением в головной мозг кислорода вместе с кровью по причине закупорки одного или нескольких сосудов. Из-за этого мозг новорожденного не может формироваться нормально. При несвоевременном медицинском вмешательстве в тканях могут возникать кровотечения и развиваться патологические изменения. Именно своевременность играет важную роль при лечении ишемии головного мозга у новорожденных.
Признаки и симптомы ишемии головного мозга у новорожденных
Заболевание проявляет себя явными симптомами, которые обращают на себя внимание.
Как возникает церебральная ишемия?
В 70% случаев ишемия возникает у плода еще в утробе матери и связана с образованием тромба в одном из сосудов, питающих головной мозг, или с недостаточным развитием сосуда. Чаще всего заболевание диагностируют у недоношенных детей, у которых сосудистая система еще не полностью сформирована.
В результате в жизненно важный орган поступает недостаточное количество крови, а вместе с ней – кислорода. Промедление с оказанием медицинской помощи ведет к поражению более крупных участков головного мозга, кровоизлиянию в мозг и другим тяжелым последствиям.
Причины
В подавляющем большинстве случаев причины церебральной ишемии у новорожденных заключаются в различных нарушениях вынашивания плода в последние недели, а также в нестандартных ситуациях при родах.
Факторы риска
Различные сосудистые и неврологические патологии, проблемы с артериальным давлением (особенно наследственные) у матери должны насторожить врача, который ведет беременность. Также факторами риска возникновения у ребенка церебральной ишемии являются:
Диагностика
В основном заболевание диагностируют в течение первых нескольких часов.
О наличии патологии свидетельствуют отклонения при проверке рефлексов, общем анализе крови. Обычно анализ показывает повышенное содержание в организме углекислого газа.
При обнаружении явных симптомов тяжелого заболевания проводят магнитно-резонансную томографию, а также электроэнцефалографию, выявляющие скрытые судороги и др. отклонения в работе головного мозга.
Степени ишемии
Церебральная ишемия 1 степени
Легкая форма, характеризующаяся наличием слабо выраженных признаков в первые 3-5 дней после рождения. В основном, проявляется в виде:
За ребенком ведет наблюдение врач, а симптомы постепенно проходят без осложнений.
Церебральная ишемия 2 степени
Опасная форма заболевания. Для нее характерны:
Чаще всего ишемия 2 степени проявляет себя в первые сутки жизни новорожденного, а симптомы могут наблюдаться в течение 2-4 недель. В это время за ребенком тщательно наблюдают врачи, он проходит курс терапии. При необходимости проводят хирургическую операцию по удалению тромба.
Церебральная ишемия 3 степени
Наиболее тяжелая форма, при которой:
Опытный врач уже в первые 5 минут жизни новорожденного может определить наличие признаков и симптомов церебральной ишемии 3 степени. В этом случае ребенка отправляют в реанимацию, при необходимости подключают к аппарату искусственной вентиляции легких.
Лечение церебральной ишемии у новорожденных
Цель лечения – восстановить нормальное кровообращение в тканях головного мозга, не допустить патологических изменений и устранить последствия ишемии. Для болезни 1-й степени лечение обычно заключается в назначении массажа для улучшения кровообращения.
При заболеваниях 2-ой и 3-ей степени применяют медикаментозную терапию и хирургическое вмешательство для удаления тромба в сосуде и восстановления структуры сосудистого русла. В сложных случаях младенец проходит восстановительный курс интенсивной терапии.
Прогноз и последствия церебральной ишемии
Гораздо эффективнее ликвидировать саму ишемию после рождения младенца, нежели лечить ее осложнения. Среди последствий церебральной ишемии 2 степени:
Если же все действия по устранению ишемии были проведены врачами своевременно, то симптомы проходят в течение реабилитационного периода, длящегося обычно 6-12 месяцев.
Церебральная ишемия у новорожденных детей
Церебральная ишемия у новорожденных детей
Церебральная ишемия — диагноз, который могут поставить врачи новорожденным малышам в роддоме, при котором необходимо наблюдение невролога, остеопата, а так же может потребоваться курс лекарственных препаратов.
ЦЕРЕБРАЛЬНАЯ ИШЕМИЯ — диагноз, который могут поставить врачи новорожденным малышам в роддоме. Возникает она из-за недостаточного снабжения клеток головного мозга кислородом. Причина, способствующая этой нехватке, может появиться как во время беременности мамы, так и во время рождения ребенка.
Одним из первых тестов, которыми пользуются врачи сразу после рождения малыша — является всем известная оценка ребенка по шкале Апгар. По количеству баллов судят о состоянии малыша. Чем ниже балл, тем тяжелее состояние ребенка, тем больше вероятность данного диагноза. Диагноз церебральная ишемия новорожденных используют врачи в первый месяц жизни ребенка и делят патологию по тяжести на три степени. От степени тяжести зависит лечение ребенка.
Самая легкая – это 1 степень, как правило, отмечается легкая неврологическая симптоматика, например, в виде повышенной возбудимости ребенка и малыш не нуждается в стационарном лечении. А вот при второй, особенно третей степени решается вопрос о госпитализации малыша в специализированное отделение стационара. Первый месяц — это острое состояние. Со второго месяца жизни до достижения 1 года идет период восстановления пострадавшей от ишемии нервной системы, и невролог в диагнозе гипоксически-ишемическое поражение цнс выделяет ведущие синдромы и лечение подбирает в соответствии с этим. Одно из тяжелых последствие церебральной ишемии – это детский церебральный паралич, делающий ребенка инвалидом детства.
Что же требуется от родителей?
Какие изменения после лечения у остеопата наблюдают родители у ребенка? Чаще всего это улучшение сна, уменьшение немотивированного плача, срыгиваний, положительные сдвиги в предречевом и моторном развитии. Невролог наблюдает положительную динамику при неврологическом осмотре, у него появляется возможность уменьшить лекарственную нагрузку на ребенка.
Гипоксически-ишемическая энцефалопатия
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «03» октября 2019 года
Протокол №74
Гипоксически-ишемическая энцефалопатия – это острое повреждение головного мозга плода и новорожденного после перенесенной перинатальной асфиксии, вызванное дефицитом кислорода в крови (гипоксемия) и слабой перфузией (ишемия) достаточной силы и продолжительности, чтобы привести к функциональным и биохимическим изменениям (активация анаэробного гликолиза, развитие лактатацидоза) и тяжелым нарушениям энергетического обмена [1].
Перинатальная асфиксия – критическая кислородная недостаточность плода во время родов, приводящая к тяжелому метаболическому ацидозу, депрессии дыхания и нарушению адаптации кровообращения сразу после рождения [2].
Название протокола: Гипоксически-ишемическая энцефалопатия
Код(ы) МКБ-10:
| Код | Название |
| Р91.0 | Другие нарушения церебрального статуса у новорожденного |
| Р91.0 | Ишемия мозга |
Дата разработки/пересмотра протокола: 2014 год (пересмотр 2018 г.)
Сокращения, используемые в протоколе:
| аЭЭГ | – | Амплитудно-интегрированная электроэнцефалография |
| ГИЭ | – | гипоксически-ишемическая энцефалопатия |
| ИВЛ | – | искусственная вентиляция легких |
| УЗИ | – | ультразвуковое исследование |
| МРТ | – | магнитно-резонансная томография |
Пользователи протокола: врачи-неонатологи.
Категория пациентов: новорожденные дети.
Шкала уровня доказательности:
Соотношение между степенью убедительности доказательств и видом научных исследований
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследование случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное, или исследование случай-контроль, или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
| 1-ая степень (легкое поражение) | 2-ая степень умеренное поражение) | 3-я степень (тяжелое поражение) | |
| 1 | 2 | 3 | 4 |
| Уровень сознания | Повышенная раздражимость | Апатичность или заторможенность (снижена реакция на раздражитель) | Ступор, кома (отсутствует реакция на раздражитель) |
| Нейромышечный контроль | |||
| Мышечный тонус | Нормальный | Легкая гипотония | Вялый |
| Поза | Легкая дистальная флексия | Выраженная дистальная флексия в | Интермиттирующая децеребрация |
| Периостальные рефлексы | Повышены | Повышены | Снижены или отсутствуют |
| Сегментарный миоклонус | Присутствует | Присутствует | Отсутствует |
| Сложные рефлексы | Норма | Угнетение | Отсутствуют |
| Сосательный рефлекс | Слабый | Слабый или отсутствует | Отсутствует |
| Рефлекс Моро | Повышен с низким порогом | Ослаблен, неполный; высокий порог | Отсутствует |
| Окуловестибу-лярный рефлекс | Нормальный | Повышен | Ослаблен или отсутствует |
| Шейный тонический рефлекс | Легкий | Выраженный | Отсутствует |
| Вегетативные функции | Преобладает симпатическая | Преобладает парасимпатическая | Угнетение обеих систем |
| Зрачки | Мидриаз | Миоз | Непостоянный размер, часто асимметрия, недостаточная реакция на свет |
| Дыхание | Спонтанное | Спонтанное, иногда апноэ | Периодическое, апноэ |
| Частота сердечных сокращений | Тахикардия | Брадикардия | Варьирующая |
| Секреция бронхиальных желез | Скудная | Обильная | Варьирующая |
| Перистальтика кишечника | Нормальная или сниженная | Усилена, диарея | Варьирующая |
| Судороги | Нет | Частые, фокальные или мультифокальные | Редкие (за исключением децеребрации) |
| Результаты ЭЭГ | Норма (бодрствование) | Ранние: низкий вольтаж с непрерывными дельта- и тетра-волнами. Поздние: периодический | Ранние: периодический паттерн с изопотенциальными фазами. |
| ЭЭГ | паттерн (бодрствование); фокальные или многоочаговые судороги; «пик-волна» от 1,0 до 1,5 Гц | Поздние: тотальная изопотенциальность | |
| Продолжитель-ность | 2–14 дней | От нескольких часов до нескольких недель | |
| Исход | Около 100% ─ нормальный | В 80% случаев нормальный; патология, если симптомы персистируют более 5–7 дней | Около 50% умирают; у остальных – тяжелые последствия |
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии:
Для подтверждения тяжести перенесенной гипоксии в течение первых 30 минут после рождения у новорожденного проводится забор крови из пережатой артерии пуповины для определения ее газового состава (стабильность газового состава забранной крови сохраняется в пластиковом шприце в течение 30 минут!).
Критерии острой перинатальной асфиксии, которые могут быть причиной ГИЭ [4]:
Обязательные критерии (должны присутствовать все 4):
Помимо повреждения нервной системы, признаком тяжелой асфиксии является полиорганная недостаточность:
Тяжелое угнетение дыхательной и сердечной деятельности:
выражающаяся такими признаками, как олигурия и, в восстановительном периоде – полиурия, что приводит к значительному водно-электролитному дисбалансу.
Повреждения со стороны кишечника в первые несколько дней жизни могут не проявлять себя. Обычными являются вялая перистальтика кишечника и замедленное опорожнение желудка. В редких случаях развивается некротизирующий энтероколит.
Лабораторные исследования:
Цель всех лабораторных методов – оценить степень тяжести повреждения мозга и
контролировать функциональное состояние жизненно-важных систем.
Набор исследований зависит от развития симптомов. результаты дополнительных исследований должны интерпретироваться в комплексе с клиническим анамнезом и результатами объективного исследования (смотрите алгоритм дифференциальной диагностики).
Ранними изменениями являются общее снижение амплитуды фонового ритма с наличием различных степеней судорожной активности.
Особенно угрожающий признак – разрывное подавление паттерна (т.е изоэлектрическая ЭЭГ). Если этот образец ЭЭГ соответствует клинике – обычно он расценивается, как свидетельство необратимого повреждения, тождественного юридическому определению смерти мозга.
Дифференциальный диагноз
Дифференциальная диагностика неонатальных энцефалопатий:
Неонатальная энцефалопатия – это неспецифическая реакция ГМ на различные повреждения вследствие множества процессов. Диагноз ГИЭ выставляется только в тех случаях, когда точно установлено, что гипоксия и ишемия привели к клиническому состоянию новорожденного, что будет способствовать проведению специфических методов лечения и помощи в прогнозировании.
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза ГИЭ |
| 1 | 2 | 3 | 4 |
| Наследственные болезни обмена | Однотипная с ГИЭ симптоматика неврологических нарушений: •синдром угнетения, либо гипервозбуди-мости; •неонатальные судороги/кома | 1. Анализ семейного анамнеза: •близкородственный брак; •смерть предыдущих детей от: — сепсиса с неустановленным возбудите-лем; -синдром внезапной смерти; -неустановленная причина смерти. 2. Анализ особенностей внутриутробного развития плода: -ЗВУР; -наличие дисморфий; -гепатолиенальный синдром; -асцит плода; -неиммунная водянка плода. 3. Лабораторные исследования • в крови: аммиак, КОС, мочевина, триглицериды, спектр аминокислот и ацилкарнитинов; галактоза и активность фермента галактозо-1-фосфат-уридилтрансферазы. • в моче: кетоновые тела, рН, спектр органических кислот, сукцинил ацетон, запах и цвет. | Положительные специфические реакции на наследственные болезни обмена, специфический запах мочи и тела: • аммиак повышен, респираторный алкалоз, реакция на кетоновые тела отрицательная ‒ нарушение цикла мочевины, транзиторная гипераммо-ниемия; • аммиак повышен, рН в норме, кетоновые тела +, сладкий запах мочи (кленового сиропа, карамели) ― лейциноз; при запахе «вареной капусты» ‒ тирозинемия; • аммиак в норме или повышен, метаболический ацидоз, кетоновые тела +, запах «потных ног», «сыра» ‒ изовалериановая ацидемия; или запах • «кошачей мочи» ― 3-ОН- изовалериановая ацидурия; • высокий уровень фенилаланина, «мышиный» ― фенилкетонурия. Для уточнения диагноза НБО ‒ генетическое обследование. |
•С-реактивный белок;
•Бактериологическое исследование крови;
•Рентгенография органов грудной клетки;
Для ТБИ характерно появление через 8-12 и 24 часа после рождения лейкоцитоза/лейкопении, нейтрофилеза/нейтропении, повышение лейкоцитарного индекса ≥0,2, СОЭ ≥10 мм/час на 1- й неделе жизни и уровня С-реактивного белка ≥ 10 мг/л, положительный результат бактериологического исследования крови, на рентгенограмме при пневмонии характерны очаговые изменения
(БЭН)
Все перечисленные тесты не характерны для ГИЭ
Лечение (амбулатория)
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Карта наблюдения пациента, маршрутизация пациента (схемы, алгоритмы):
Немедикаментозное лечение:
Единственным методом немедикаментозного лечения, относительно широко используемым у детей, перенесших среднетяжелую и тяжелую асфиксию в родах, является контролируемая лечебная гипотермия. Суть методики заключается в создании гипотермического воздействия, позволяющего прервать вторую фазу гипоксически-ишемического повреждения и снизить количество погибших нервных клеток в результате вторичного энергетического дефицита/апоптоза 12.
Режимы охлаждения при гипотермии новорожденных.
| Cool Cap [9] | Системная гипотермия [10] | |
| Способ охлаждения | Голова и тело | Тело |
| Оборудование | Охлаждающая шапочка и источник лучистого тепла | Охлаждающее одеяло |
| Главная цель: температура | 33,0-34,0 0 С | 33,5 0 С |
| Главная цель: место | Прямая кишка | Пищевод |
| Контроль температуры на месте наложения | Сервоконтроль температуры кожи живота* | Сервоконтроль температуры пищевода |
| Возраст начала охлаждения | Менее 6 час | 5±1,1 час |
| Время достижения целевой температуры после начала охлаждения | 2 часа | ≈1,5 час** |
| Длительность охлаждения | 72 часа | 72 часа |
| Скорость согревания | 0,5 0 С/час | 0,5 0 С/час |
Перечень основных лекарственных средств (имеющих 100% вероятность применения)
Хирургическое вмешательство: нет.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе: снижение летальности и тяжелой психоневрологической инвалидизации.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации в родовспомогательный стационар: для новорожденного нет.
Показания для экстренной госпитализации в родовспомогательный стационар для новорожденного: нет.
NB! Тип госпитализации в родовспомогательный стационар определяется состоянием беременной женщины (матери новорожденного с ГИЭ).
Информация
Источники и литература
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков протокола с указанием квалификационных данных:
Рецензенты:
Ишемия мозга лечение у ребенка
Цереброваскулярная окклюзия может поражать как артерии, так и синусы черепа или мозговые вены. Это может быть связано с тромбозом или миграцией эмбола, чаще всего сердечного происхождения. В большинстве случаев окклюзия сосуда происходит внезапно или, по меньшей мере, вызывает быстро развивающиеся клинические проявления. Понятие «инсульт», который может быть геморрагическим или ишемическим, определяется как клинический синдром быстро развивающихся клинических симптомов очаговых или общих расстройств функции мозга, продолжительностью более 24 часов или приводящих к смерти без очевидных причин, несосудистого генеза. В этой статье на сайте будет рассматриваться только ишемический инсульт. Похожие случаи, длящиеся менее 24 часов, называются транзиторной ишемической атакой.
Ежегодная заболеваемость инсультами в детском возрасте составляет приблизительно 1,2-3:100000 человек. Schoenberg et al. (1978) сообщали о ежегодной заболеваемости на уровне 2,52 случая на 100000 детей в Рочестере, Миннесоте, что соразмерно примерно половине случаев опухолей мозга у детей в США. Геморрагические инсульты в этих исследованиях встречались несколько чаще (55%), чем ишемические. Сходная картина наблюдалась в Швеции (Eeg-Olofsson и Ringheim, 1983), тогда как Giroud et al. (1997) в обследовании 54 детей выявили, что ишемический инсульт более типичен (57% против 43% соответственно).
Blom et al. (2003) зарегистрировали уровень встречаемости 1,5-3,0:100000.
Неонатальный инсульт более распространен, чем считалось раньше, что будет обсуждаться ниже.
а) Механизм и патология ишемического инсульта у ребенка. Артериальная окклюзия может быть результатом церебральной эмболии или тромбоза. Независимо от причины возникает ишемический инсульт. Когда в процесс вовлекается одна из крупных мозговых артерий, инфаркт может затрагивать как кору, так и подлежащее белое вещество. При геморрагическом инфаркте пораженная область переполнена кровью и усеяна точечными кровоизлияниями. На границе инфаркта ткань выглядит бледной, обычно со значительным отеком. В центре области инфаркта определяется массивный некроз всех тканевых компонентов, в то время как по направлению к периферии инфаркта повреждение становится все менее тяжелым. На протяжении первых часов острой ишемии повреждение в периферической части (так называемая «пенумбра») является обратимым с восстановлением кровотока. Поэтому в этот момент требуется неотложная терапия. Область пенумбры не определяется на КТ или стандартном МРТ, но дает высокий сигнал при выполнении диффузионной МРТ.
Через несколько часов обнаруживается полиморфно-ядерная инфильтрация, сменяющаяся в течение 4-5 дней мононуклеарными фагоцитами. В конце концов, пролиферируют астроциты и развивается волокнистая сеть, что является причиной ретракции и склероза коркового вещества (улегирия). В область максимального повреждения может сформироваться киста, оставляя в мозге полость, нередко ошибочно именуемую «порэнцефалией».
Уязвимость мозга даже при кратковременной ишемии хорошо известна. Отек ткани мозга может увеличить объем поражения путем сдавления капилляров, предотвращая таким образом реваскуляризацию коллатеральными путями с «явлением отсутствия кровотока», в который вовлечены комплексные факторы. В отличие от ишемии, в области инфаркта отмечается повышенный кровоток вокруг повреждения, так называемая «излишняя перфузия», которая выявляется при нейровизуализации и сканировании мозга. Роль молочной кислоты и других патологических метаболитов в последовательности событий, которые приводят к ишемии и инфаркту, широко обсуждается (Plum, 1983).
Причины тромбоза или эмболии значительно варьируют, и во многих случаях они остаются неопределенными.
б) Клинические проявления. Клинические особенности в большинстве случаев не отличаются, независимо от развития инфаркта в результате тромбоза или эмболии. В целом у ишемического инсульта тромботического происхождения начало менее острое, чем у инсульта геморрагического типа, более продолжительное развитие и иногда упреждающее проявление сходных регрессирующих эпизодов. В некоторых случаях этиология или условия возникновения позволяют предположить конкретный механизм. К примеру, наличие бактериального эндокардита или порока клапанов сердца способствует эмболии, в то время как «прерывистое» начало клинических проявлений более напоминает тромбоз. Анамнез шейной травмы наводит на мысль о разрыве сонных или позвоночных артерий (Garg et al., 1993; Garg и DeMyer, 1995).
По сути окклюзия сосудов проявляется внезапным развитием неврологического дефицита в бассейне одного из крупных мозговых сосудов, наиболее часто в виде острого начала гемиплегии (Lanska et al., 1991). У некоторых пациентов — в 23% случаев в исследовании Abram et al. (1996) — ишемическим инсультам обычно примерно за неделю предшествуют эпизоды транзиторной гемиплегии, продолжающиеся от одного до нескольких часов, которые могут сопровождаться другими явлениями дефицита, такими как дефекты полей зрения, патологические движения или афазия. Симптомы и признаки внутричерепной гипертензии могут быть представлены большими приступами и могут потребоваться экстренные меры. Дисфазия присутствует при правосторонней гемиплегии, когда поражается кора (Cranberg et al., 1987), что также наблюдалось в некоторых случаях с инфарктами, ограниченными областью внутренней капсулы, скорлупы, хвостатого ядра (Ferro et al., 1982; Dusser et al, 1986).
Дисфазия наиболее выражена у детей в возрасте до 8-10 лет. Однако афазия не характерна для младших детей и а в случаях до двух лет часто проявляется как немота. Определение острая гемиплегия детского возраста иногда используется для обозначения только тех случаев, когда полное обследование не выявляет этиологии. Область переднего кровообращения на сегодняшний день является наиболее поражаемой, поэтому типична картина ишемического инсульта у детей в виде острой гемиплегии, но случаи гемиплегии сосудистого происхождения распространены среди всех возрастных групп детей и подростков, тогда как гемиплегия после судорог чаще встречается у детей первых трех лет жизни. Начало в любом возрасте, наиболее часто до шести лет.
В одном из крупных исследований приобретенных гемиплегий (Aicardi et al., 1969), в 27% случаев отсутствовали предшествующие судорожные припадки, а большинство из них предположительно было сосудистого происхождения. Напротив, лишь редкие случаи с признаками окклюзии сосудов предварялись эпистатусом, хотя изолированные приступы могут возникать в более четверти случаев инфарктов мозга в бассейне средней мозговой артерии при начале гемиплегии. Yang et al. (1995) обнаружили, что 36 из 56 пациентов с инсультом перенесли по меньшей мере один приступ с рецидивом в 21 случае. Однако судороги были редкими при отсутствии поражения коры мозга по данным нейровизуализации. Различия между многочисленными исследованиями, вероятно, являются результатом гетерогенности случаев, обследованных в разных центрах.
Сосудистой гемиплегии может предшествовать лихорадка, хотя она более характерна в случаях после-судорожной гемиплегии. Выявление таких продромальных симптомов как головная боль, боль в области шеи, ипсилатеральный синдром Горнера или транзиторные ишемические эпизоды в анамнезе, предшествующие гемиплегии, поможет яснее определить причины таких явлений как расслоение.
При всех приобретенных гемиплегиях слабость является максимальной сразу после начала заболевания и, как правило, сопровождается вялостью (Isler, 1984). Мышечная спастичность и симптомы пирамидального тракта возникают позже. Степень восстановления значительно варьирует. Существенное восстановление может ожидаться на протяжение первых двух или трех недель, а дальнейший медленный прогресс может длиться нескольких месяцев. Непроизвольные движения атетоидного типа или явные расстройства являются редкими.
Топография инфарктов, вызывающих приобретенную гемиплегию, является различной. В таблице ниже перечислены вовлекаемые артерии, соответствующие областям инфарктов, и основные клинические особенности. Тем не менее, топография и объем инфаркта зависят, помимо пораженных сосудов, от разных факторов, таких как качество коллатерального и системного кровообращения и индивидуальных анатомических особенностей. Локализация инфаркта может также различаться в зависимости от этиологии. Ишемические инсульты в базальных ядрах наиболее часто являются идиопатическими, чем поверхностные инсульты (Dusser et al, 1986; Kappelle et al., 1989). Инсульты могут возникнуть в любом артериальном бассейне. Вовлечение внутренней капсулы и чечевицеобразного ядра можно назвать редким, но фактически они участвуют приблизительно в половине случаев (Dusser et al., 1986). Результаты ангиографии иногда трудно интерпретировать, но они могут быть даже нормальными при инсультах в области капсулы и скорлупы.
Поражение задней мозговой артерии развивается намного реже, чем в сонных артериях и их ветвях. Echenne et al. (1983) наблюдали 36 случаев, и в дальнейшем добавилось лишь несколько случаев. Многие случаи вертебрально-базилярной недостаточности были связаны с травмой, вызвавшей разрыв (Garg et al., 1993), который также может возникнуть спонтанно (Sturzenegger, 1995; Khurana et al., 1996) при аномалиях шейного отдела позвоночника (Ross et al., 1987; Phillips et al., 1988) или сосудистых мальформациях. Все причины инсульта можно обнаружить, но достаточно часты «идиопатические» случаи. Более ограниченные окклюзии поражают только мозжечковую артерию (Chatkupt et al, 1987), приводя к мозжечковому инфаркту. Однако латеральный медуллярный синдром наблюдался при тромбозе позвоночной артерии (Klein et al., 1976). Таламический инфаркт может быть результатом проксимальной обструкции позвоночной артерии в области шеи (Garg et al., 1993; Garg и DeMyer, 1995; Garg и Edwards-Brown, 1995).
Клиническая картина вертебробазилярной окклюзии включает тошноту, атаксию, тремор, гемиплегию, головокружение, паралич глазодвигательных мышц, тетраплегию, дизартрию, нистагм и вовлечение нижних черепных нервов (Mehler, 1988). Имеются сообщения о нарушении сознания, кризах опистотонуса и дыхательной недостаточности (Echenne et al., 1983). Хотя в некоторых сообщениях упоминается о встречаемости клонико-тонических атак, они, вероятно, не являются истинными эпилептическими припадками (Ropper, 1988). Более ограниченные инфаркты могут привести к изолированной атаксии и патологической подвижности глаз или расстройствам сознания и речи. Двусторонний таламический инфаркт может быть связан с обструкцией одной таламоперфорирующей артерии (Garg и DeMyer, 1995). После инсульта может развиваться деменция в области среднего и промежуточного мозга. Окклюзионным повреждениям в задней мозговой артерии часто предшествуют повторные эпизоды вертебрально-базилярной недостаточности за дни, недели или даже месяцы до окончательной атаки.
Сдавление позвоночной артерии при повороте головы может вызывать транзиторные ишемические приступы (Garg и Edwards-Brown, 1995).
г) Особенности нейровизуализации. Нейровизуализационная картина артериальной окклюзии зависит как от размера инфаркта, так и от продолжительности периода между началом инсульта и обследованием (Raybaud et al., 1985). КТ и даже МРТ сканирование, выполненное в течение первых 10-24 часов, указывает на норму, но диффузионная тензорная визуализация при МРТ может продемонстрировать существенный патологический сигнал, регрессирируемый частично или полностью (Warach et al., 1995). Позднее появляется область со сниженным ослаблением с плохо различимыми границами, которые расширяются, становятся лучше видными и достигают максимума через следующие несколько дней. Этот участок низкой плотности сопровождается варьирующим масс-эффектом, с максимумом проявления на 2-3 день.
Большинство инфарктов не увеличивается при введении контраста в течение первой недели. Однако у детей раннее увеличение не является редкостью даже через 24-48 часов. При увеличении в большинстве случаев вовлекается кортикальное серое вещество, которое выглядит как волнистая лента под извилинами мозга. Позднее инфаркт проявляется в виде вдавленного треугольного рубца.
Малые лакунарные инфаркты часто не увеличиваются при введении контрастного вещества и могут оставаться необнаруженными на КТ, но обычно видны в Т2-режиме МРТ (Inagaki et al., 1992). Самые большие лакуны, поражающие область скорлупы или бледного шара, могут иногда накапливать контраст. Кровоизлияния в пределах участка инфаркта могут возникать на протяжении первой недели заболевания.
На МРТ выявляются даже небольшие ишемические очаги, которые дают сигнал низкой интенсивности на Т1-взвешенной последовательности и интенсивный сигнал вероятно отечного характера на Т2-взвешенной последовательности. Кровоизлияние лучше всего определяется на Т1-взвешенной МРТ по периферии инфаркта.
С появлением современных методов нейровизуализации традиционная ангиография в большинстве случаев для диагностики инфаркта не требуется. Действительно, лакунарные инфаркты, как правило, не сопровождаются видимыми сосудистыми патологиями, поскольку вовлеченные сосуды слишком небольшого размера и слишком разные по внешнему виду на ангиографии, чтобы определить окончательный диагноз (Kappelle et al., 1989). Для пациентов с необъяснимыми инсультами, ангиография, на мой взгляд, до сих пор показана для контроля внутренней сосудистой патологии, такой как фиброзно-мышечная дисплазия и разрыв, и для распознавания случаев с множественными сосудистыми повреждениями типа моямоя. Это важно для прогностических и терапевтических целей. МРА может быть неадекватным для этой цели, поскольку дает информацию скорее о кровотоке, чем о сосудистой структуре.
С другой стороны, она дает некоторую информацию об изменении тканевой перфузии. Реперфузия тромбированных сосудов может возникать уже через два дня после инсульта (Isler, 1984), что может объяснить частоту нормальных ангиограмм при детских инсультах. Недавние технические достижения в МРА были описаны Husson et al. (2002) и Husson и Lasjaunias (2004). Parker et al. (1998) рассмотрели результаты и специфические симптомы при различных методах визуализации. МРА позволяет больше оценить поток, чем сосудистые стенки. Это исследование не является достаточно точным, чтобы продемонстрировать тонкие сосудистые аномалии, такие как артериальный стеноз или неровность стенок сосудов. Новые методы КТ ангиографии (спиральная КТ) является перспективной. Цифровая субтракционная внутривенная ангиография может быть достаточной для определения относительно большой группы множественных повреждений, но точный анализ все же требует использования артериального доступа.
МРТ может точно показать разрыв шейных и внутричерепных артерий как причину инфаркта (Zuber et al., 1993). Водно-диффузионная МРТ и перфузионно-взвешенная МРТ в настоящее время обеспечивают раннюю диагностику инфаркта и оценку области инфаркта и пенумбры, таким образом позволяя уточнить диагноз и более точно определить прогноз (Sakoh et al., 2001). Для аналогичных целей также применялась спектроскопия, использующая 1H-MR (Imamura et al., 2004).
Транскраниальная доплерография является неинвазивным и ценным методом, позволяющим визуализировать артериальные аномалии и с помощью усовершенствованной методики оценить функциональные характеристики кровообращения в сосуде (Sturzenegger, 1995).
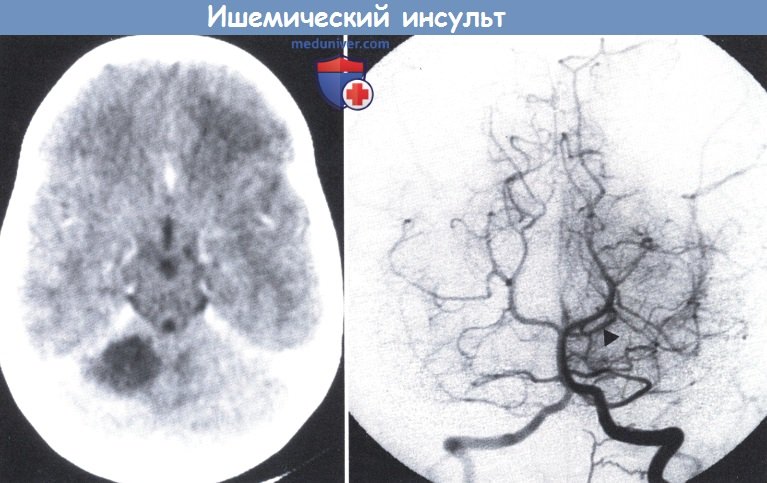
Ангиография позвоночника (справа): отсутствие контраста в правой верхней мозжечковой артерии.
Маркером указана противоположная верхняя артерия мозжечка (15-летний мальчик с внезапным развитием правостороннего мозжечкового синдрома, прогрессивно убывающего в последующие месяцы).
д) Дифференциальный диагноз. Приобретенную сосудистую гемиплегию необходимо отличать от других многочисленных причин острой гемиплегии. Дифференцировка от острой постсудорожной гемиплегии (ГГЭ синдром), которая редко возникает в связи с сосудистым тромбозом, обычно не составляет трудностей. На КТ и МРТ изображения совершенно разные, так как они показывают первоначальный отек и сниженную плотность целого полушария без преимущественного вовлечения любого сосудистого бассейна, с последующей позднее гемиатрофией мозга (Kataoka et al., 1988). Гемиплегическая мигрень бывает трудно отличимой от артериальной, в редких случаях становясь причиной инсульта. У пациентов с сердечно-сосудистыми заболеваниями, приобретенная гемиплегия может также быть результатом венозного тромбоза или мозгового абсцесса, последний только после возраста 2-3 лет.
В сомнительных случаях, разумнее всем таким детям назначить антибактериальную терапию, которая может быть отменена через неделю, если абсцесс исключен. Опухоли, особенно ствола мозга, могут привести к быстрому развитию приобретенной гемиплегии. В отличие от них, некоторые инфаркты развиваются постепенно и могут имитировать объемные поражения (Chatkupt et al., 1987). Эпилептические припадки и другие пароксизмальные состояния могут вызывать транзиторную гемиплегию, которую, как правило, нетрудно отличить от сосудистой гемиплегии, за исключением начальной стадии. Геморрагический инсульт обсуждался выше.
Транзиторные ишемические нарушения нехарактерны для детей, но могут встречаться у пациентов с артериальным стенозом любого генеза или как продромальное состояние в случае разрыва или тромбоза. Они характеризуются краткосрочной гемиплегией, гемианопией или гемисенсорным дефицитом. Острые, но преходящие приступы гемипареза, которые встречаются у детей с инсулинозависимым сахарным диабетом (глава 22), могут представлять диагностическую проблему. Нейровизуализация не демонстрирует инфаркт, и гемиплегия разрешается через 24-48 часов. Такие атаки отличаются от настоящих инсультов, которые могут развиваться у молодых пациентов с диабетом во время эпизодов кетоацидоза. Окклюзия задней мозговой артерии, возникшая у восьмилетней девочки, страдающей диабетом, с выраженным отеком мозга в результате неправильного лечения кетоацидоза, вероятно, была связана со сдавлением артерии краем намета мозжечка (личный случай).
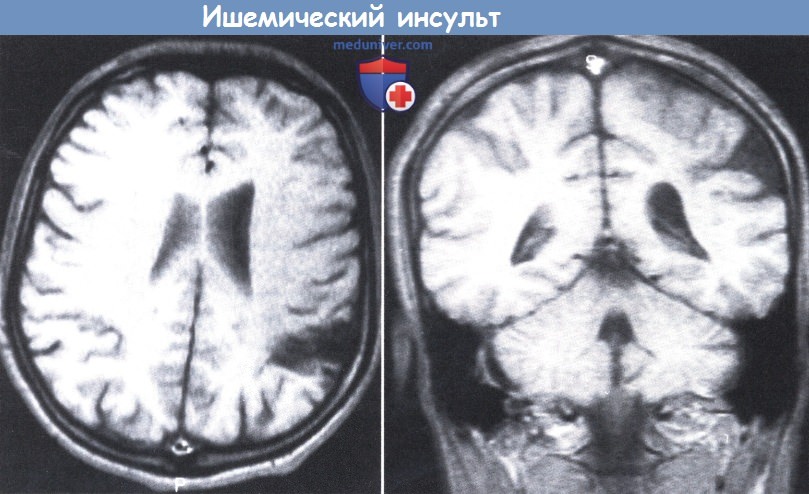
у которого внезапно развилась правосторонняя гемиплегия в возрасте 20 месяцев при заболевании с гипертермией (имелся минимальный остаточный гемипарез).
MPT, Т1-режим: дефект треугольной формы в теменной коре, проникающий в белое вещество. Обратите внимание на относительно небольшой дефект в полушарии. 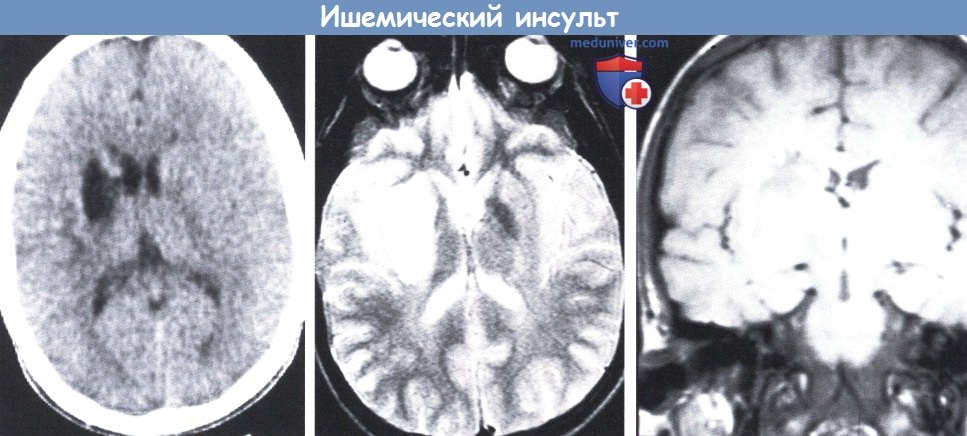
КТ (слева): лакуна в правом хвостатом ядре и внутренней капсуле.
MPT, Т1-режим (в центре): обширный участок интенсивного сигнала, вероятно связанный с отеком.
MPT, Т2-режим (справа): обширная область низкого сигнала в правом полушарии, четко отграниченная зоной интенсивного сигнала, вероятно, в связи с небольшим кровотечением.
е) Исход и прогноз. Исход приобретенной окклюзии зависит в большей степени от причины сосудистого расстройства. Прогноз должен быть осторожным, если обнаруживаются расстройства в крупных сосудах мозга, такие как болезнь моямоя или фиброзно-мышечная дисплазия. В Швейцарии 80 детей наблюдались в течение двух лет (Steinlin et al., 2005), четверо из них умерло в течение шести месяцев, но общий уровень смертности был относительно низким. Однако нейрофизиологические проблемы были выявлены при последующем наблюдении у 25 из 33 детей и 6 детей имели IQ
Редактор: Искандер Милевски. Дата публикации: 2.1.2019