какие клетки красного костного мозга могут в норме попадать в кровь
Какие клетки красного костного мозга могут в норме попадать в кровь
Сосудистая сеть костного мозга начинается от артерии, проникающей в кроветворную ткань через костный канал. Ответвления артерии формируют элементарную морфофункциональную единицу костного мозга — «синусоидальное дерево». Стенка синусоидов состоит из эндотелиальных клеток и лежащих на них со стороны гемопоэтической ткани широких мононукле-арных адвентициальных клеток. Гемопоэтическая ткань распространяется между синусоидами. Созревающие эритроидные и гранулоцитарные клетки, мегакариоциты и макрофаги прилегают к наружной поверхности сосудистых синусов.
Зрелые клетки из костного мозга попадают в кровь через отверстия между эндотелиальными клетками костно-мозговых синусоидов. Диаметр этих отверстий — 2,3 мкм, т. е. много меньше проходящих через них в кровь клеток. Поэтому мигрирующие клетки должны обладать хорошей деформируемостью, чтобы преодолеть барьер и выйти в кровь. Плохо деформирующиеся ригидные ядра эритробластов, миелоцитов, промиелоци-тов не позволяют им мигрировать через отверстия в синусоиде. Напротив, хорошо деформирующиеся ядра зрелых гранулоцитов, моноцитов и лимфоцитов дают им возможность пересекать эндотелий.
Важным условием миграции клеток в кровь является способность ретикулоцитов и клеток белой крови к движению. Они пересекают узкие отверстия синусоидов, выпуская в них сначала цитоплазматические отростки—псевдоподии. В костномозговых синусоидах края эндотелиальных клеток тесно прилегают друг к другу и не позволяют клеткам проходить через отверстия между ними. Однако миграция клеток через них облегчается ритмичными расслаблениями синусоидов, которые уменьшают перекрытие этими клетками пор. Поверхность эндотелиальных клеток частично покрыта адвентициальными клетками, которые легко скользят по ней благодаря сократительному аппарату, имеющемуся у адвентициальных клеток. Сокращаясь, адвентициальные клетки уменьшают покрываемую ими поверхность костномозговых синусоидов и увеличивают возможность миграции клеток через стенку синусоидов в кровоток.
Выход клеток в просвет синусоида возрастает под влиянием молекулярных регуляторов гемопоэза. Эритропоэтин стимулирует быстрый выход ретикулоцитов, КСФ и бактериальный эндотоксин — нейтрофилов. Эритропоэтин ускоряет «сборку» цитоскелета ретикулоцитов, находящихся в костном мозге, увеличивает их деформабельность, что облегчает их выход через отверстия стенки синусоидов в кровь. Регуляторы облегчают формирование отверстий в эндотелии, уменьшая внешнюю поверхность эндотелия костномозгового синуса, покрытого адвентициальными клетками. Например, инъекция животному эритропоэтина резко уменьшает его адвентициальный покров и ретикулоциты легко пересекают стенку синусоида.
В норме небольшая часть клеток не достигает стадии созревания, погибает в костном мозге и подвергается фагоцитозу макрофагами, располагающимися на наружной поверхности костномозговых синусоидов. Применительно к эритроидному ряду это явление называется неэффективным эритропоэзом, применительно к гранулоцитарному — неэффективным гранулопоэзом. Неэффективный гемопоэз охватывает от 2 до 10 % эритробла-стов и от 10 до 15 % костномозговых гранулоцитов. Их мембраны теряют сиаловые кислоты, в результате уменьшается отрицательный заряд мембраны и макрофаги легко фагоцитируют эти клетки. Неполноценные клетки в кровоток не поступают.
Публикации в СМИ
Лейкоз острый
Острый лейкоз — злокачественное заболевание кроветворной системы; морфологический субстрат — бластные клетки.
Частота. 13,2 случаев на 100 000 населения среди мужчин и 7,7 случаев на 100 000 населения среди женщин.
КЛАССИФИКАЦИЯ
FAB классификация (франко американо британская) основана на морфологии лейкемических клеток (строение ядра, соотношение размеров ядра и цитоплазмы) • Острый миелобластный (нелимфобластный) лейкоз (ОМЛ) •• М0 — без созревания клеток, миелогенная дифференцировка доказывается только иммунологически •• М1 — без созревания клеток •• М2 — ОМЛ с дифференцировкой клеток, •• М3 — промиелоцитарный •• М4 — миеломоноцитарный •• М5 — монобластный лейкоз •• М6 — эритролейкоз •• М7 — мегакариобластный лейкоз • Острый лимфобластный лейкоз (ОЛЛ): •• L1 — без дифференцировки клеток (морфологически гомогенные клетки) •• L2 — с дифференцировкой клеток (морфологически гетерогенная популяция клеток) •• L3 — беркеттоподобные лейкозы • Недифференцируемый лейкоз — к этой категории относят лейкозы, клетки которых невозможно идентифицировать как миелобластные или лимфобластные (ни химическими, ни иммунологическими методами) • Миелопоэтическая дисплазия •• Рефрактерная анемия без бластоза (в костном мозге бласты и промиелоциты
Код вставки на сайт
Лейкоз острый
Острый лейкоз — злокачественное заболевание кроветворной системы; морфологический субстрат — бластные клетки.
Частота. 13,2 случаев на 100 000 населения среди мужчин и 7,7 случаев на 100 000 населения среди женщин.
КЛАССИФИКАЦИЯ
FAB классификация (франко американо британская) основана на морфологии лейкемических клеток (строение ядра, соотношение размеров ядра и цитоплазмы) • Острый миелобластный (нелимфобластный) лейкоз (ОМЛ) •• М0 — без созревания клеток, миелогенная дифференцировка доказывается только иммунологически •• М1 — без созревания клеток •• М2 — ОМЛ с дифференцировкой клеток, •• М3 — промиелоцитарный •• М4 — миеломоноцитарный •• М5 — монобластный лейкоз •• М6 — эритролейкоз •• М7 — мегакариобластный лейкоз • Острый лимфобластный лейкоз (ОЛЛ): •• L1 — без дифференцировки клеток (морфологически гомогенные клетки) •• L2 — с дифференцировкой клеток (морфологически гетерогенная популяция клеток) •• L3 — беркеттоподобные лейкозы • Недифференцируемый лейкоз — к этой категории относят лейкозы, клетки которых невозможно идентифицировать как миелобластные или лимфобластные (ни химическими, ни иммунологическими методами) • Миелопоэтическая дисплазия •• Рефрактерная анемия без бластоза (в костном мозге бласты и промиелоциты Copy
Какие клетки красного костного мозга могут в норме попадать в кровь
Цель исследования: оценка особенностей миелограммы из костного мозга трубчатых костей
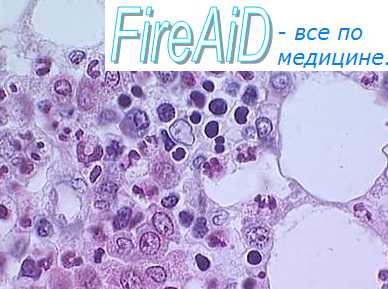
Результаты исследования: Было исследовано 15 образцов костного мозга трубчатых костей, полученного при ампутации конечности. Высохшие на воздухе мазки фиксировались с использованием фиксатора Майн-Грюнвальда, далее фиксированные мазки окрашивались азур-эозином по Романовскому. Окрашенные препараты микроскопировали с иммерсией при увеличении х 1000 используя микроскоп Olympus CX 41 (окуляр на 10, объектив на 100). Следует отметить, что состояние костного мозга во всех случаях разное. Консистенция костного мозга варьирует от жидкого, как вода до густого типа желе, но это состояние не связано с клеточным составом и не влияет на результаты миелограмм. Также характерен цвет костного мозга трубчатых костей, чаще он желтоватый из-за жирового компонента, который является необходимым составляющим компонентом для жизнеобеспечения костного мозга. Утверждение, что костный мозг трубчатых костей перерождается в жировую ткань, является сомнительным, так как в процессе исследования костного мозга пациентов различного возраста, выявлено, что даже у 25-летнего больного, которому произведена ампутация конечности в связи с отморожением стопы, костный мозг имеет такой же процент жировой ткани, как и пожилые пациенты старше 70 лет. При исследовании костного мозга определяется неоднородность по наличию «островков кроветворения». В одних случаях их нет вообще, у других присутствуют единичные. Костный мозг трубчатых костей крайне редко бывает красноватого цвета, что позволяет предположить низкий уровень кроветворной функции. При подсчете миелограммы желтого костного мозга следует отметить следующее: недифференцированные бласты, миелобласты и промиелоциты в пределах от 0,1% до 1,4%. Содержание миелоцитов возрастает от 8,0% до 31,4%. Количество метамиелоцитов, палочкоядерных и сегментоядерных нейтрофилов в пределах нормы. В целом клетки нейтрофильного ряда количественно составляют от 64,0% до 78,6%. Крайне низкое число клеток эозинофильного ряда от 0,1% до 3,0%. Содержание клеток эритроидного ряда незначительно снижено от 7,0% до 18,0%. Лейко-эритробластное соотношение имеет свои особенности и равно от 5:1 до 10:1. Индекс созревания эритробластов равен 1,0. Отмечается полное отсутствие тромбоцитов и мегакариоцитов. Во всех исследованных образцах (10) отмечалась нормальная клеточность костномозгового материала и в 2 случаях клеточность была снижена. Состав костного мозга полиморфный. Тип эритропоэза нормобластический. Гранулоцитарный росток в норме или расширен. Созревание нейтрофилов не нарушено. Эритроидный росток во всех случаях угнетен. Белый росток гиперплазирован.
Заключение: Полученные данные следует считать нормой для желтого костного мозга. Исследование особенностей желтого костного мозга, взятого из бедренной кости (в случае ампутации конечности) может быть использовано для более полного понимания процессов иммуногенеза, происходящих в организме. В последнее десятилетие резко повысился интерес к изучению стволовых клеток, что невозможно без тонкого изучения костного мозга, как красного, так и желтого в целом. Понимание процессов происходящих в микроокружении стволовых клеток, находящихся в костном мозге, даст нам возможность влиять на функциональное состояние этих клеток и управлять ими.
Данная работа выполнена при поддержке Красноярского краевого фонда поддержки научной и научно-технической деятельности.
Рецензенты:
Сухоруков А.М., д.м.н., проф. ФГБНУ «НИИ МПС» г. Красноярск;
Черданцев Д.В., д.м.н., проф., заведующий кафедрой и клиникой хирургических болезней им. проф. А.М. Дыхно с курсом эндоскопии и эндохирургии КрасГМУ, г. Красноярск.
Система кровообращения
Кровообращением называют движение крови в организме человека. Оно состоит из трех основных частей: крови, кровеносных сосудов (артерий, вен, капилляров) и сердца.
Мы решили подготовить ознакомительный материал, чтобы каждый из вас был осведомлен обо всех нюансах работы сердечнососудистой системы. Это важно, чтобы вы вовремя могли понять, с какой проблемой могли или можете столкнуться в дальнейшем, а также, чтобы терминологические выражения нашего специалиста на очной консультации не казались вам иностранным языком.
Сердце – основа системы кровообращения
Сердце представляет собой мышечный орган размером с человеческий кулак, который располагается в левой части грудной клетки, чуть спереди легких. Этот орган фактически является мощным двойным насосом с четырьмя камерами, перекачивающим кровь и поддерживающим ее движение по всему телу.
Правая часть сердца состоит из верхней (предсердие) и нижней (желудочек) камер. Предсердие принимает переработанную венозную кровь, насыщенную углекислым газом, после чего направляет ее к желудочку. Из него она попадает в легочные артерии, где вновь насыщается кислородом. «Свежая» кровь циркулирует к левой верхней камере (атриуму), откуда попадает в аорту и начинает обновленную транспортировку по всему организму.
Сердечная мышца совершает более 3 миллиардов ударов в течение жизни.
Кровеносные сосуды
Кровеносные сосуды имеют разную форму, структуру и объем, в зависимости от их роли в организме.
1. Артерии являются самыми прочными сосудами в теле человека. Их стенки плотны и эластичны, состоят из трех слоев – эндотелия, волокон гладкой мускулатуры и фиброзной ткани. Задача артерий обстоит в насыщении всех органов и тканей кровью, обогащенной кислородом и питательными веществами. Исключением являются артерии малого круга кровообращения, по которым венозная кровь течет от сердца к легким. Самым крупным артериальным сосудом является аорта.
3. Капилляры – тончайшие сосуды, схожие по объему с человеческим волосом. Они являются ответвлениями крупных периферических артерий. Именно через них ткани и органы снабжаются кислородом и нутриентами. Они также обладают коммуникацией с венами, чтобы отдавать им клеточные отходы. Следовательно, эти крошечные сосуды одновременно являются кормильцами и санитарами нашего организма.
Нормальную циркуляцию крови внутри сосудистой системы обеспечивает артериальное давление.
Клеточное строение крови
Кровь состоит из двух компонентов: плазмы (50-60%) и взвешенных форменных элементов (40-50%).
Ко второй категории относятся:
· Эритроциты (красные кровяные тельца) – самые многочисленные из форменных элементов. Согласно данным официальных исследований, одна капля крови содержит порядка 5 миллионов эритроцитов. Красные кровяные тельца отвечают за транспорт газов – кислорода и диоксида углерода. Содержат в себе белок гемоглобин, обеспечивающий связывание молекул кислорода в легких. Эритроциты доставляют кислород ко всем тканям и органам, после чего вбирают в себя углекислый газ и несут его к легким. Он удаляется из организма в процессе дыхания.
· Лейкоциты (белые клетки крови) – элементы, защищающие наш организм от чужеродных тел и соединений, являются частью иммунной системы. Белые клетки крови распознают и атакуют патогенные микроорганизмы посредством вырабатываемых антител и макрофагов. Когда в организм проникает инфекция, продукция лейкоцитов существенно усиливается. В норме их количество уступает концентрации в крови других форменных элементов.
· Тромбоциты (кровяные пластинки) – клетки, обеспечивающие коагуляцию (свертывание) крови, вытекающей из поврежденного сосуда, и предохраняющие организм от обильных кровопотерь. Они приклеиваются к отверстию в поврежденном сосуде, формируя «запечатывающую» пробку для остановки кровотечения. Именно тромбоциты могут склеиваться между собой и образовать патологические сгустки крови внутри сосудов, называемые тромбами.
Все форменные элементы синтезируются костным мозгом и распространяются при помощи плазмы – жидкой части крови.
Распространенные проблемы с кровообращением
К категории самых распространенных заболеваний кровеносной системы следует отнести:
1. Атеросклероз – хроническая патология, характеризующаяся отложением холестерина и других липидов на стенках артериальных сосудов, которая приводит к нарушению тока крови и окклюзии артерии;
2. Аневризма – выпячивание части артериальной стенки на фоне неудовлетворительной регуляции тонуса сосуда (его растяжения или истончения);
3. Инфаркт миокарда – некроз части миокарда, обусловленный полной или частичной недостаточностью его кровоснабжения на фоне истончения местных сосудов;
4. Артериальная гипертензия (гипертония) – устойчивое повышение кровяного давления, обусловленное нарушением регуляторных факторов деятельности сердечнососудистой системы;
5. Варикозное расширение вен – хроническое заболевание, обусловленное необратимой деформацией вен, связанное с недостаточностью венозных клапанов и нарушением венозного тока крови.
Нормальное кровообращение является важнейшей составляющей здорового организма. Если вы отмечаете у себя характерные признаки того или иного заболевания сердечнососудистой системы, не медлите с обращением к сосудистому хирургу или флебологу. Помните, что игнорирование симптомов в данном случае может стоить вам жизни.
β-2 микроглобулин (лимфома, множественная миелома) (кровь) в Сердобску
Анализ уровня β2-микроглобулина является важным исследованием при диагностике миеломной болезни и лимфомы.
Приём и исследование биоматериала
Когда нужно сдавать анализ β-2 микроглобулин (лимфома, множественная миелома) (кровь)?
При установленной множественной миеломе и лимфоме для определения стадии, степени тяжести и прогноза заболевания.
Подробное описание исследования
На поверхности большинства ядросодержащих клеток расположены большие белки, называемые антигенами класса I, или главным комплексом гистосовместимости (МНС I). Благодаря этому комплексу иммунная система человеческого организма способна идентифицировать опухолевые клетки, а также бактерии, вирусы и другие патологические микроорганизмы. Антигены класса I экспрессируются в основном на лимфоцитах и в меньшей степени в тканях легких, почек и печени; еще реже — в скелетных мышцах и головном мозге.
Главный комплекс гистосовместимости I состоит из двух белковых субъединиц, т.н. тяжелой и легкой цепей. В свою очередь, тяжелая цепь состоит из полиморфной α-субъединицы, кодируемой одним из генов класса I локуса МНС, а легкая цепь химически связана с ней. Эта легкая цепь и представляет собой микроглобулин β2.
β2 (бета-2) микроглобулин — это белок, представленный во всех биологических жидкостях организма: моче, крови, спинномозговой жидкости и др. Он синтезируется практически всеми клетками, в норме его можно обнаружить в кровотоке в небольших концентрациях. Из организма β2М выводится через органы мочевыделительной системы. В почках происходит его фильтрация и реабсорбция, то есть обратное всасывание в кровь.
Изначально в мочу поступает малый объем бета-2 протеина. Следовательно, избыточное количество β2-микроглобулина в моче может быть плохим прогностическим симптомом, это может свидетельствовать о нарушении фильтрационной функции почек — почечной недостаточности — и быть причиной болезни отложений — амилоидоза — у пациентов на гемодиализе.
В наибольшем количестве β2М представлен на лимфоцитах, его концентрация в крови отражает их деление и размножение. Помимо этого, бета-2 микроглобулин участвует в апоптозе, или запрограммированной гибели, клетки и может запускать образование молекул воспаления — интерлейкинов 6, 8 и 10. Из дополнительных функций β2М известно, что этот протеин участвует в реакциях взаимодействия интерлейкинов с их рецепторами, а также регулирует образование факторов роста клеток. В связи с этим его повышение в крови/моче может признаком воспалительных заболеваний, в том числе аутоиммунных и инфекционных.
Однако основной причиной повышения концентрации β2М к крови, как правило, является развитие онкологических заболеваний кроветворной системы организма. К ним относятся такие лимфопролиферативные патологии, как: лимфома и множественная миелома.
Оба заболевания имеют опухолевую природу. Лимфома развивается в органах с лимфоидной тканью (лимфатические узлы, селезенка и др.) и может распространяться — метастазировать — по всему организму. Миеломная болезнь связана со злокачественным перерождением B-лимфоцитов, которые начинают бесконтрольно производить антитела одного класса. Заболевание имеет системный характер и чаще всего поражает кости, костный мозг и почки.
Тем не менее бета-2 микроглобулин нельзя назвать полноценным онкомаркером. Скорее он используется как вспомогательный метод диагностики, который даёт врачу дополнительную информацию о вероятном прогнозе заболевания, его степени тяжести и распространенности, а также эффективности терапии. Также β2-микроглобулин используют при оценке безрецидивной выживаемости.
