кальцинаты в головном мозге у новорожденного последствия
Кальцинаты в головном мозге у новорожденного последствия
Иногда на рентгенограммах можно обнаружить обызвествления и инородные тела. Обызвествления в черепе детей могут быть физиологическими и патологическими. Физиологические располагаются на уровне сосудистых сплетений боковых желудочков, в шишковидной железе, серповидном отростке. У детей раннего возраста они встречаются редко и появляются постепенно с возрастом.
К патологическим обызвествлениям относятся опухолевые и неопухолевые. Из опухолей часто обызвествляются краниофарингиомы (70—85%), тератомы, хордомы, дермоиды; из глиальных опухолей — олигодендроглиомы, пинеаломы. При краниофарингиомах известковые массы находятся выше турецкого седла и несколько кзади. Локализация очень типична и не вызывает диагностических затруднений.
К неопухолевым относятся посттравматические, постинфекционные, паразитарные и дизонтогенетические обызвествления.
Дизонтогенетические обызвествления наблюдаются при внутричерепных ангиомах, энцефалотригеминальном ангиоматозе, туберозном склерозе. Ангиоматозные сосуды выглядят как нежные червеобразные обызвествления. При энцефалотригеминальном ангиоматозе обнаруживаются двуконтурные линейные тени обызвествлений, располагающиеся по ходу мозговых извилин, преимущественно в заднетеменных и затылочных областях мозга. Множественные, округлые и тяжистые обызвествления в поверхностных отделах мозга наблюдаются при туберозном склерозе.
К посттравматическим обызвествлениям у новорожденных и грудных детей относятся кефалогематомы. По верхнему контуру кефалогематомы обызвествляется твердая мозговая оболочка в виде тонкой полоски-скорлупы, позже известь можно найти и в толще бывшей гематомы. Иногда кефалогематома оссифицируется и имеет вид костной опухоли.
При эпидуральных гематомах наряду с участками обызвествления наблюдаются истончения внутренней костной пластинки, а иногда — образование участков рассасывания кости. Если ребенок перенес тяжелую черепно-мозговую травму, протекавшую с субдуральным или внутримозговым кровоизлиянием, то при возникновении гематом могут образоваться обширные обызвествления, плоские в виде серпа или полулуния. Субдуральная гематома представляет собой инкапсулированное скопление крови в субдуральном пространстве. Гематома плоская и чаще всего односторонняя. При внутримозговых гематомах наблюдаются единичные множественные «коралловые» петрификаты.
Черепно-мозговая травма, перенесенная в раннем детском возрасте, при которой были отмечены переломы костей и подоболочечные гематомы, может привести к образованию участков рассасывания кости.
Подобные изменения можно наблюдать уже через 3—4 нед после травмы. Костные дефекты в результате рассасывания костей образуются, если травма произошла в возрасте до 3 лет. Это объясняется особенностями кровоснабжения костей черепа в этом возрасте.
К постинфекционным относятся обызвествления у детей раннего возраста после менингоэнцефалита, туберкулезного менингита, абсцесса мозга. Они могут быть единичные и групповые, крапчатого пли кораллового строения.
Паразитарные обызвествления у детей раннего возраста встречаются при токсоплазмозе и цитомегалии. Известковые включения в черепе при токсоплазмозе обнаруживаются у 40—50% больных, а при микроскопическом исследовании — у 85%. Петрификаты бывают множественные, полиморфные и располагаются в разных отделах мозга: теменно-затылочной, височно-лобной, мозжечке, сосудистых сплетениях. Размеры их колеблются от 2 до 10 мм в диаметре, форма — в виде узелков, палочек, черточек, гроздей. В связи с тем что при токсоплазмозе часто поражается орган зрения, кальцификаты можно обнаружить и в пораженном глазу. При цитомегалии обызвествления такие же, как при токсоплазмозе.
У новорожденных иногда можно обнаружить так называемый лакунарный череп. На краниограммах в области костей свода видны крупные овальные истончения, разделенные костными перегородками, напоминающие лакуны.
Лакунарный череп возникает в результате повышения внутричерепного давления или глубоких расстройств костеобразования во внутриутробный период. После рождения процесс не прогрессирует.
Лакунарный череп следует отличать от лакунарного остеопороза. Последний встречается у здоровых новорожденных и в клинике известен как «мягкий череп». Кости свода черепа при пальпации податливы, голова не увеличена в размерах. На краниограммах выражены ячеистые просветления на фоне нормальной картины свода черепа, рисунок костных перегородок между лакунами отсутствует. В возрасте 2—3 мес очаги лакунарного остеопороза исчезают.
Органическое поражение мозга
Понятие «органическое поражение мозга у детей» не имеет четкого и однозначного определения.
Но принято считать, что это – целый комплекс нарушений, связанных со структурными патологическими изменениями в тканях головного мозга.
Они могут быть как диффузными (например, появиться вследствие энцефалопатии) так и локализованными (возникнуть в результате опухоли или травмы головного мозга)
У таких детей нарушены функции многих тканей в мозгу и не только, нужно немало времени, чтобы они поменялись на другие или здоровые, которые будут выполнять свои функции правильно.
В современной педиатрии такое явление, к сожалению, это не редкость.
Головной мозг детей подвержен целому ряду негативных воздействий
Более того, невропатологи утверждают, что диагноз «органическое повреждение головного мозга» сегодня можно ставить 9 из 10 пациентов любого возраста.
Просто большая часть таких поражений не дает о себе знать.
Симптомы ОПМ ярко проявляются тогда, когда изменением подверглись от 20 до 50% органа.
Если же повреждение охватило больше половины мозга, тогда стоит говорить о серьезных признаках болезни, носящих стойкий патологический характер.
Но есть и другая сторона медали: часто не слишком квалифицированные специалисты просто злоупотребляют данным диагнозом, не желая глубоко анализировать характер неврологической патологии у ребенка.
В медицине существует классификация недугов, которые можно объединить под термином ОПМ (органическое поражение мозга).
Заболевания, относящиеся к органическим поражениям головного мозга:
Гидроцефалии
Врожденные аномалии развития головного мозга
Детский церебральный паралич ДЦП
Нарушения, вызванные внутриутробными инфекциями
Группа заболеваний, вызванных поражением центральной нервной системы (ЦНС)
Каждый недуг, входящий в эту группу, характеризуется множеством нюансов – имеет свою природу и развивается особым образом
От причины развития болезни во многом зависит и характер его лечения
Существует несколько основных причин возникновения органического поражения головного мозга у детей
Гипокальциемии у детей. Клиническое наблюдение
Опубликовано в журнале:
«ПРАКТИКА ПЕДИАТРА»; сентябрь-октябрь; 2018; стр. 32-42.
Е.В. Тозлиян, к.м.н., педиатр-эндокринолог, генетик, ОСП «НИКИ педиатрии им. академика Ю.Е. Вельтищева» ФГБОУ ВО РНИМУ имени Н.И. Пирогова МЗ РФ, г. Москва
Ключевые слова: дети, гипокальциемия, витамин D
Keywords: children, hypocalcemia, vitamin D
В детском возрасте (особенно на первом году жизни) заболевания (или состояния), связанные с нарушением фосфорно-кальциевого обмена, встречаются довольно часто.
Физиология фосфорнокальциевого обмена
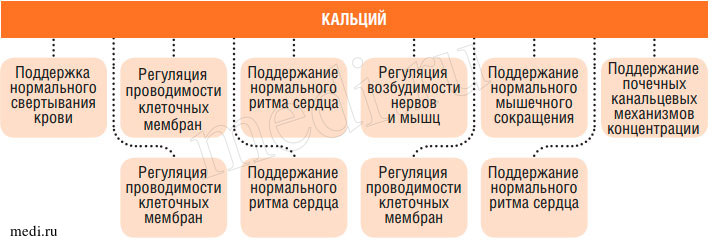
Ионы кальция регулируют ряд важнейших физиологических и биохимических процессов, в частности, нейромышечное возбуждение, свертывание крови, поддержание целостности мембран и транспорт через мембраны, многие ферментативные реакции, внутриклеточное функционирование гормонов и нейромедиаторов (рис. 1).
Рис. 1. Роль кальция в организме
В сыворотке крови кальций в трех формах:
Роль фосфора в организме не менее важная.
Фосфор выполняет важную роль в транспорте кислорода, энергетическом обмене, обеспечении целостности скелета, мышечной сократимости. Концентрации кальция и фосфора во внеклеточной жидкости взаимосвязаны: любые изменения внеклеточной концентрации одного из ионов приводят к обратному изменению концентрации другого.
Также нельзя забывать о роли магния в организме:
Магний выполняет важную роль в построении ряда энзимов, кофактор биохимических реакций, в активации секреции паратгормона, в костном метаболизме и обмене кальция, мышечной сократимости.
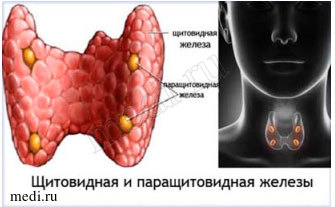
Рис. 2. Регуляция фосфорно-кальциевого обмена (анатомическое расположение щитовидной и околощитовидных желез)
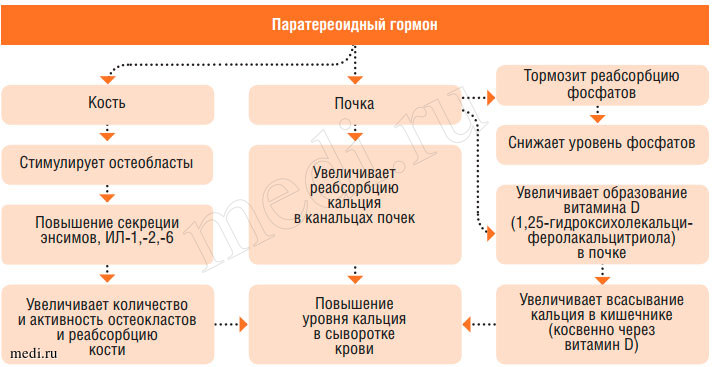
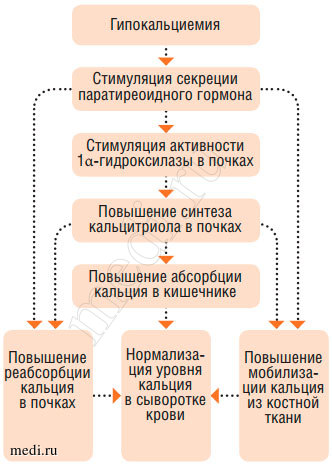
Рис. 3. Регуляция фосфорно-кальциевого обмена (эффекты паратиреоидного гормона)
Рис. 4. Регуляция фосфорно-кальциевого обмена (эффекты паратиреоидного гормона)
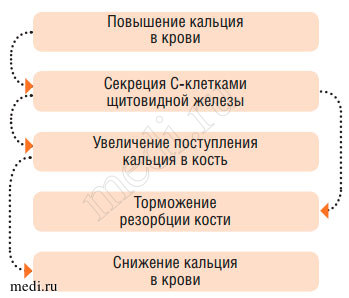
Рис. 5. Регуляция фосфорно-кальциевого обмена (эффекты кальцитонина)
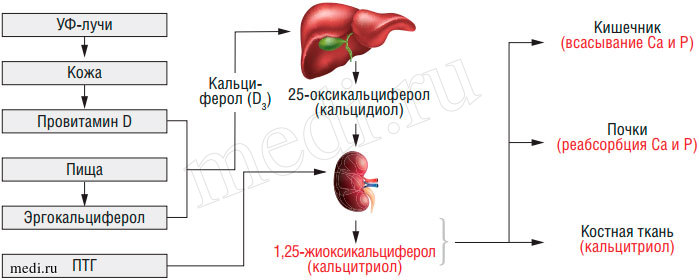
Рис. 6. Метаболизм витамина D3 в организме
Механизм всасывания кальция в кишечнике связан с синтезом энтероцитами кальций-связывающего белка (СаСБ), одна молекула которого транспортирует 4 атома кальция. Синтез СаСБ индуцируется кальцитриолом через генетический аппарат клеток, т. е. по механизму действия 1,25(OH)2D3 аналогичен гормонам. В условиях гипокальциемии витамин D временно увеличивает резорбцию костной ткани, усиливает всасывание кальция в кишечнике и реабсорбцию его в почках, повышая тем самым уровень кальция в крови. При нормокальциемии он активирует деятельность остеобластов, снижает резорбцию кости и ее кортикальную порозность. В последние годы показано, что клетки многих органов имеют рецепторы к кальцитриолу (активному метаболиту витамина D), который тем самым участвует в универсальной регуляции ферментных внутриклеточных систем. Активация соответствующих рецепторов через аденилатциклазу и цАМФ мобилизует кальций и его связь с белком-кальмодулином, что способствует передаче сигнала и усиливает функцию клетки, и соответственно, всего органа.
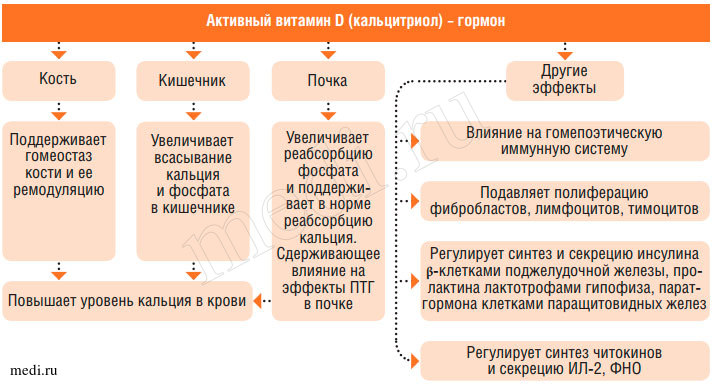
Витамин D стимулирует реакцию пируват-цитрат в цикле Кребса, обладает иммуномодулирующим действием, регулирует уровень секреции тиреотропного гормона гипофиза, прямо или опосредованно (через кальциемию) влияет на выработку инсулина поджелудочной железой (рис. 7).
Рис. 7. Эффекты активного метаболита витамина D (кальцитриола) в организме
На гомеостаз кальция и фосфора, кроме трех вышеописанных (витамин D, паратгормон, кальцитонин), оказывает влияние множество других факторов:
Болезнь Фара
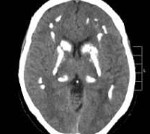
Болезнь Фара — идиопатическая симметричная кальцификация церебральных структур: подкорковых ганглиев, коры полушарий, мозжечка. Может протекать бессимптомно, клинически проявляется экстрапирамидными расстройствами (гиперкинезами, паркинсонизмом), мозжечковыми нарушениями, интеллектуальным снижением. Диагностируется по данным церебральной КТ при исключении вторичного характера кальцинированных очагов по результатам биохимических, ультразвуковых, ПЦР исследований. Лечение симптоматическое с применением средств, улучшающих тканевый обмен, цитопротекторов, препаратов леводопы, антиконвульсантов.
МКБ-10
Общие сведения
Болезнь Фара включает случаи первичного идиопатического отложения кальция в мозговых структурах, вторичные формы церебрального кальциноза в рамках данной патологии не рассматриваются. Первые подробные описания заболевания сделаны в 1930 году немецким невропатологом К.Т. Фаром. Болезнь Фара является редкой нозологией, распространённость составляет менее 1 случая на 1 млн. населения. Гендерные различия в заболеваемости выражаются соотношением мужчин и женщин 2:1. Патология проявляется в любом возрастном периоде, чаще в 30-60 лет. Прижизненно выявляется лишь в 1-2% случаев, что объясняется наличием бессимптомных вариантов течения, диагностикой заболевания под видом иных нейродегенеративных процессов (болезни Паркинсона, сенильной хореи).
Причины болезни Фара
Патогенез
Формирующие болезнь патогенетические механизмы окончательно не определены. Предполагаются генетически детерминированные сдвиги церебрального метаболизма, становящиеся причиной отложения в мозговых тканях избытков кальция. Выраженная кальцификация подкорковых образований становится причиной дезорганизации лобно-субкортикальной системы, регулирующей произвольные движения и обеспечивающей когнитивные функции (память, мышление, внимание).
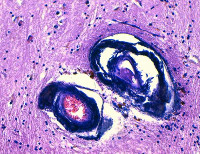
Морфологически кальцификаты обнаруживаются симметрично в различных структурах: коре мозга, белом веществе, подкорковых ганглиях, внутренней капсуле, мозжечке, стенках мелких артерий, реже вен. Характерно наличие периваскулярных мелких кальциевых конгломератов. Наиболее массивная кальцификация выявляется в подкорковых отделах. Микроскопически кальцификаты отличаются типичной структурой, представленной нитями толщиной 140-400 мкм. Они зачастую содержат минеральные комплексы с включениями железа, меди, алюминия, фосфора, свинца, цинка, кобальта.
Классификация
В практической неврологии болезнь Фара подразделяется на две клинические формы, отличающиеся возрастом манифестации, типом преобладающей симптоматики:
Симптомы болезни Фара
В типичных случаях болезнь дебютирует появлением утомляемости, неуклюжести движений, шаткости ходьбы, изменений речи, непроизвольных двигательных актов или ночных мышечных спазмов. Основу клинических проявлений составляют экстрапирамидные нарушения. В молодом возрасте это различные гиперкинезы: атетоз — непроизвольные червеобразные движения в пальцах кистей, хореоатетоз — сочетание атетоза с быстрыми насильственными движениями в конечностях, торсионная дистония — тонические мышечные спазмы, придающие телу неестественные позы. У взрослых наблюдается вторичный паркинсонизм: амимия лица, брадикинезия, замедленные скованные движения, шаркающая походка, постуральный тремор.
Симптоматика паркинсонизма зачастую сочетается с мозжечковой атаксией (дискоординация, несоразмерность движений, нистагм), пирамидной недостаточностью (слабость в конечностях, повышенные сухожильные рефлексы, патологические стопные знаки). Возможна дизартрия, дисфагия, недержание мочи. Эпилептические пароксизмы более характерны для ювенильной формы заболевания, могут отмечаться у взрослых.
Сопровождающие болезнь Фара когнитивные нарушения характеризуются снижением памяти на текущие и прошлые события, замедленным мышлением, неустойчивым вниманием, угасанием способности к аналитической и синтетической интеллектуальной деятельности. Прогрессирование расстройств когнитивной сферы у детей приводит к олигофрении, во взрослом возрасте — к развитию корково-подкорковой деменции с элементами агнозии, апраксии, алексии. Однако часть больных ювенильной формой остаются интеллектуально сохранными.
Диагностика
Основным диагностическим методом, позволяющим неврологу достоверно установить наличие очагов кальциноза в мозговых тканях, является КТ головного мозга. Интенсивность очагов на томограммах отражает уровень концентрации кальция. МРТ головного мозга значительно хуже визуализирует кальцификаты, но позволяет оценить сопутствующие дегенеративные процессы. С целью подтверждения идиопатического характера патологии проводится целый ряд дополнительных обследований:
Диагноз болезнь Фара правомочен после исключения вторичного характера церебральной кальцификации, наблюдающейся при эндокринных (гипопаратиреоз, псевдогипопаратиреоз, гипотиреоз), сосудистых (атеросклероз, амилоидоз сосудов), инфекционных (краснуха, цистицеркоз, токсоплазмоз, цитомегалия) заболеваниях. Дифференциальная диагностика проводится также с болезнью Галлервордена-Шпатца, туберозным склерозом.
Лечение болезни Фара
Поскольку патогенез заболевания остаётся неясным, терапия имеет преимущественно симптоматический характер. С целью улучшения обменных процессов применяются стимуляторы тканевого метаболизма (ацетилкарнитин, глютаминовая кислота, комплекс L-цитруллин+малат, никотинамид), цитопротекторы (рибофлавин, янтарная кислота, мельдоний). При симптомах паркинсонизма предпочтительно назначение фармпрепаратов леводопы, при гиперкинезах — холинолитиков, бензодиазепинов. Наличие эпилептических приступов служит показанием к лечению современными антиконвульсантами (леветирацетамом). В комплексной терапии применяется лечебная физкультура, водолечение, когнитивные тренинги.
Прогноз и профилактика
Клинически проявленная болезнь Фара рассматривается как хроническое нейродегенеративное заболевание. Прогноз выздоровления неблагоприятный, однако, при должном уровне поддерживающей симптоматической терапии состояние пациентов длительное время остаётся удовлетворительным. Субклинический вариант не сказывается на здоровье и когнитивных способностях больного, может быть случайной находкой при проведении компьютерной томографии. Специфические меры, позволяющие предупредить развитие болезни, не разработаны.
Гидроцефалия у детей: только факты
В лекции рассматриваются определение, варианты классификаций, этиология, патогенез, клиническая синдромология гидроцефалии (врожденной и приобретенной) у детей, а также современные подходы к диагностике, методы лечения (фармакологического и нейрохирургиче
Definition, classification variants, etiology, pathogenesis and clinical syndromology of hydrocephalus (congenital and acquired) in pediatric patients are considered, as well as contemporary approaches to diagnostics, methods of management (pharmacological and neurosurgical) and prevention for this type of central nervous system pathology.
Гидроцефалия — болезнь, возникающая вследствие избыточной выработки и чрезмерного накопления ликвора в подоболочечных пространствах и/или желудочках головного мозга (в субарахноидальном или субдуральном пространстве), приводящих к истончению (атрофии) мозгового вещества и расхождению костей черепа [1–4].
В МКБ-10 предусмотрены следующие коды для различных видов гидроцефалии: G91 (G91.0 — сообщающаяся гидроцефалия, G91.1 — обструктивная гидроцефалия, G91.2 — гидроцефалия нормального давления, G91.3 — посттравматическая гидроцефалия неуточненная, G91.8 — другие виды гидроцефалии, G91.9 — гидроцефалия неуточненная).
Классификация гидроцефалии
Существуют несколько вариантов классификации гидроцефалии. Прежде всего, различают врожденную и приобретенную гидроцефалию.
Врожденная гидроцефалия имеется к моменту рождения ребенка и является результатом воспалительных заболеваний центральной нервной системы (ЦНС), пороков развития мозга, а также внутричерепной (родовой) травмы, кровоизлияний в головной мозг.
Приобретенная гидроцефалия развивается после рождения вследствие этиологически и патогенетически разнообразной патологии (нейроинфекции, опухолевые процессы, сосудистые заболевания, черепно-мозговые травмы и т. д.).
Болезнь бывает активной и пассивной. В первом случае имеется повышение внутричерепного давления при наличии дилатации желудочков и субарахноидальных пространств. При пассивной гидроцефалии предполагается, что описываемые изменения отмечаются в отсутствие внутричерепной гипертензии.
Выделяют открытую и закрытую формы гидроцефалии. Открытая (сообщающаяся) гидроцефалия диагностируется при отсутствии нарушений связи желудочковой системы мозга с субарахноидальным пространством, а закрытая (окклюзионная или несообщающаяся) — когда это сообщение нарушено.
Наружная и внутренняя формы гидроцефалии определяются локализацией аккумуляции спинномозговой жидкости (СМЖ); наружная гидроцефалия — скопление СМЖ в подоболочечных пространствах головного мозга, внутренняя гидроцефалия — скопление СМЖ в желудочках головного мозга.
Патогенетическая классификация гидроцефалии: 1) гиперсекреторные формы (избыточное образование СМЖ); 2) арезорбтивные формы (нарушение процессов всасывания СМЖ); 3) окклюзионные формы (наличие препятствия на пути движения СМЖ от источника ее образования к областям ее резорбции).
В зависимости от имеющегося уровня окклюзии ликворных путей рассматривают пять вариантов гидроцефалии: 1) окклюзия одного или обоих отверстий Монро; 2) блокада полости III желудочка; 3) стеноз или окклюзия сильвиева водопровода; 4) окклюзия или нераскрытие отверстий IV желудочка; 5) нарушения проходимости субарахноидальных пространств.
В зависимости от достигнутого уровня контроля над внутричерепной гипертензией принято различать компенсированную, субкомпенсированную или декомпенсированную гидроцефалию.
Отдельный вариант болезни — гидроцефалия нормального давления («симптоматическая»). При ней изначально отмечается повышение внутричерепного давления (следствие избыточного скопления СМЖ в желудочках мозга) — с вентрикуломегалией или без таковой, которое постепенно снижается, но остается умеренно повышенным (150–200 мм водн. ст.). Существуют две разновидности гидроцефалии нормального давления — идиопатическая (причина неизвестна) и вторичная (следствие субарахноидального кровоизлияния, травмы, опухоли и/или инфекции ЦНС, осложнение нейрохирургического вмешательства и т. д.) [1–4].
S. Oi (2010) предложил «мультикатегориальную классификацию гидроцефалии», отражающую современные представления об этой болезни (табл.) [5, 6].
Этиология и патогенез гидроцефалии
Важнейший этиологический фактор гидроцефалии — интра- и перинатальная патология ЦНС. В качестве этиологических причин врожденной гидроцефалии рассматриваются патология беременности, кислородное голодание церебральной ткани; интранатальные факторы, приводящие к гипоксически-ишемическим и/или травматическим повреждениям головного мозга; гестационная незрелость мозговых структур, наиболее подверженных описываемым повреждениям.
К развитию гидроцефалии приводят воспалительные заболевания мозга и его оболочек, а также внутриутробные и нейроинфекции, врожденные пороки развития ЦНС, патология сосудов, опухоли головного и спинного мозга, травматические повреждения (включая внутричерепные родовые травмы), генетические факторы и др.
Описаны случаи гидроцефалии, ассоциированные с дисгенезиями головного мозга, бруцеллезом, паротитной и другими инфекциями, диффузной гиперплазией ворсинок хориоидального сплетения, сосудистыми аномалиями, внутричерепными кровоизлияниями и т. д.
Гидроцефалия посттравматическая (прогрессирующее избыточное накопление СМЖ в ликворных пространствах и веществе головного мозга вследствие черепно-мозговой травмы) обусловлена нарушениями циркуляции и резорбции СМЖ [1–4, 7].
По данным C. Schrander-Stumple и J. P. Fryns (1998) наследственная Х-сцепленная (врожденная) гидроцефалия встречается в 4% всех зарегистрированных случаев болезни (по другим данным в 5–15% наблюдений), до 40% случаев гидроцефалии этиогенетически обусловлены [8]. Гидроцефалия встречается при синдроме Дэнди–Уокера, синдроме Арнольда–Киари и др. Описано не менее 43 мутаций/локусов, связанных с гередитарными формами гидроцефалии (у человека и лабораторных животных); в экспериментальных условиях обнаружены 9 генов, ассоциированных с этой церебральной патологией, а у людей всего один [1–4].
Прогрессирование гидроцефалии сопровождается структурно-морфологическими изменениями головного мозга различной выраженности: 1) истончение коры и белого вещества (вплоть до полной его ликвидации); 2) атрофия сосудистых сплетений; 3) атрофия/субатрофия базальных ганглиев, ствола, мозжечка; 4) выраженные расстройства капиллярного кровотока; 5) утолщение и/или сращение мозговых оболочек; 6) избыточный рост (гипертрофия) глиозной ткани. В тяжелых случаях возможно формирование гидроанэнцефалии, когда имеются только эпендима и тонкий слой мягкой мозговой оболочки.
Наиболее интенсивно функционирующая и высоковаскуляризованная перивентрикулярная область максимально страдает от гипоксии. Следствием атрофии перивентрикулярного белого вещества мозга является пассивное расширение желудочковой системы с формированием вентрикуломегалии.
При посттравматической гидроцефалии патологические процессы в головном мозге морфологически характеризуются расширением желудочковой системы, перивентрикулярным отеком и облитерацией субарахноидальных щелей. Облитерация путей ликворотока определяется следующими патогенетическими факторами: субарахноидальное кровоизлияние, внутричерепные гематомы, очаговые и/или диффузные повреждения мозга, рубцово-спаечные и атрофические процессы (в том числе после обширных краниотомии и резекционных трепанаций), менингоэнцефалиты и вентрикулиты. Сроки развития посттравматической гидроцефалии (нормотензивной, гипертензивной или окклюзионной) обычно варьируют от 1 месяца до 1 года [1–4, 7].
Клиническая синдромология гидроцефалии
Основная симптоматика при гидроцефалии (врожденной и приобретенной) определяется двумя группами факторов: 1) причинами возникновения болезни; 2) непосредственно гидроцефальным синдромом.
К первой группе преимущественно относятся очаговые проявления (чаще в виде спастических парезов восходящего типа в нижних и/или верхних конечностях). Выраженность симптомов группы 2 зависит от формы, стадии и степени прогрессирования гидроцефалии. При врожденной форме болезни признаки гидроцефалии могут присутствовать как при рождении ребенка, так и проявляться позже — к возрасту 3–6 мес.
Чаще первым признаком болезни служит непропорционально быстрый прирост окружности головы. Для ее оценки у детей пользуются специальными таблицами (центильными).
У детей первого года жизни может возникать преобладание «мозговых» отделов черепа над «лицевым» (как следствие — вынужденное положение с запрокидыванием головы назад), усиление венозного рисунка и полнокровие подкожных вен головы, напряжение большого и других родничков, расхождение костей черепа, симптом Грефе. Эти симптомы сопровождаются отставанием в психомоторном развитии (различной выраженности), реже — в физическом. Атрофия сосков зрительных нервов — тяжелое осложнение не леченной или не поддающейся терапии прогрессирующей гидроцефалии.
Цефалгический синдром в большей степени свойственен приобретенной гидроцефалии у детей старше 1 года (когда роднички и черепные швы уже закрыты).
Клинические проявления посттравматической гидроцефалии характеризуются неврологическими и психическими нарушениями, вызванными первичной травмой головного мозга. Частично они являются отражением не столько самой гидроцефалии, сколько следствием перенесенной черепно-мозговой травмы (ЧМТ) или преморбидной патологии.
А. П. Коновалов и соавт. (1999) выделяют три варианта посттравматической гидроцефалии: 1) на фоне разрешившейся или негрубой остаточной симптоматики тяжелой ЧМТ, с доминированием в клинике какого-либо определенного симптомокомплекса; 2) на фоне медленно разрешающейся грубой симптоматики тяжелой ЧМТ с присоединением к ней интеллектуально-мнестических и атактических синдромов; 3) на фоне вегетативного состояния (что препятствует выходу из него). Для гипертензивной и окклюзионной посттравматической гидроцефалии (исключая нормотензивную) характерны головная боль, рвота, головокружение. У всех пациентов выявляется психопатологическая симптоматика (интеллектуально-мнестические расстройства, эйфория или заторможенность, аспонтанность, акинетический мутизм и др.); а также нарушения походки и атаксия (с характерным «прилипанием стоп к полу»), нарушения функций тазовых органов.
При гидроцефалии нормального давления обычно не отмечается классических симптомов, свойственных врожденной или приобретенной гидроцефалии, но, поскольку вентрикуломегалия оказывает негативный эффект на смежные участки корковой ткани, болезнь имеет свои особенности (классическая триада: нарушения походки, недержание мочи, снижение интеллекта различной степени выраженности) [1–4].
Диагностика и методы обследования
Установление диагноза гидроцефалии (помимо физикальных данных) основывается на данных нейровизуализации (нейросонография — при открытом большом родничке, компьютерная и магнитно-резонансная томография головного мозга — КТ и МРТ), которые рассматриваются в совокупности с описанными выше симптомами болезни. Указанные методы нейровизуализации вытеснили используемую ранее рентгенографию черепа. К ней прибегают лишь в редких случаях; обзорная рентгенография черепа позволяет косвенно судить о вторичных изменениях костей черепа (при отсутствии КТ и МРТ).
Особенно важно наблюдение за адекватным функционированием шунтов, установленных в ходе нейрохирургического вмешательства. При малейшем подозрении на несостоятельность шунтов пациент должен быть направлен к нейрохирургу.
Изотопная цистернография с введением радиоактивного изотопа (в ходе люмбальной пункции) и последующим наблюдением за выведением СМЖ из мозга позволяет установить диагноз нормотензивной гидроцефалии.
От диафаноскопии (трансиллюминация черепа) в настоящее время практически отказались. Люмбальная пункция — традиционный метод исследования, позволяющий оценить давление и провести анализ СМЖ. Усиление эхо-пульсации до 70–80% при проведении ультразвукового исследования мозга не является диагностическим признаком гидроцефалии.
Исследование слуховых вызванных потенциалов нередко обнаруживает их нарушения, что указывает на особую чувствительность ствола головного мозга к внутричерепной гипертензии.
Офтальмологический осмотр глазного дна позволяет выявить изменения, характерные для гидроцефалии (застойные явления на глазном дне, атрофические процессы, признаки воспаления, а также кровоизлияния, изменения тонуса и калибра сосудов и пр.), что дает возможность оценить течение патологического процесса.
При подозрении на наличие врожденной инфекции (внутриутробного инфицирования) оправдано проведение серологических и вирусологических исследований.
За рубежом используется метод неинвазивного мониторирования внутричерепного давления через большой родничок у детей первого года жизни, основанный на принципе аппланации. Измерение производится при помощи специального прибора (фонтанометр), а само исследование получило название «фонтограммы» или «фонтанометрии» [1–4, 7].
Дифференциальная диагностика
Гидроцефалию дифференцируют от следующих основных патологических состояний: субдуральные внутричерепные кровоизлияния, мегалэнцефалия (первичная), гидроанэнцефалия, менингит, опухоли головного мозга, семейная (конституциональная) макроцефалия, витамин D-дефицитный рахит, рахит недоношенных детей и др.
Реже встречаются другие виды патологии, от которых необходимо дифференцировать гидроцефалию: ахондроплазия, синдром Сото (церебральный гигантизм), многочисленные так называемые «нейрокожные» синдромы, группа лейкодистрофий (болезнь Александера, Канавана, глобоидная и метохроматическая формы лейкодистрофий), ганглиозидозы, мукополисахаридоз (болезни Тея–Сакса и Сандхоффа), болезнь мочи с запахом кленового сиропа и др. [1–4, 7].
Лечение
Лечебные мероприятия при прогрессирующей гидроцефалии подразделяются на оперативные и терапевтические (медикаментозные и немедикаментозные).
При наличии признаков текущего воспалительного процесса в ЦНС детям показана соответствующая терапия (антибактериальными средствами, специфическими препаратами, а также глюкокортикостероидами и человеческими внутривенными иммуноглобулинами — по показаниям).
Прогрессирующие формы гидроцефалии (окклюзионные), как более серьезный вариант патологии, требуют своевременного нейрохирургического вмешательства (проведение шунтирующей операции). Целью оперативного вмешательства является создание адекватного оттока СМЖ при помощи специальных шунтов (дренирующих систем из синтетических материалов). Различают шунты, отводящие СМЖ из желудочков мозга в различные локусы организма (вентрикулоперитонеальные, люмбоперитонеальные, вентрикулоатриальные). Так, одни шунты транспортируют избыточное скопление ликвора в перитонеальную полость, другие — в правый желудочек сердца. Вентрикулоперитонеальное шунтирование — основной метод нейрохирургического лечения гидроцефалии в РФ и за рубежом.
Существует метод хирургического лечения, получивший название «эндоскопической третьей вентрикулостомии» (перфорация нижней части III желудочка головного мозга для устранения блокирования потока СМЖ и увеличения ее оттока); другое название метода «эндоскопическая вентрикулоцистерностомия дна III желудочка». Целью описываемой операции является создание путей оттока СМЖ из III желудочка в цистерны головного мозга, через пути которых происходит резорбция ликвора.
Другими разновидностями эндоскопического лечения гидроцефалии в различных клинических ситуациях являются акведуктопластика, вентрикулокистоцистерностомия, септостомия, эндоскопическое удаление внутрижелудочковой опухоли, а также эндоскопическая установка шунтирующей системы.
Из нейрохирургических манипуляций у детей грудного возраста может применяться вентрикулярная пункция (выведение СМЖ из желудочков головного мозга через большой родничок). Эта наружная дренирующая манипуляция используется крайне редко, так как может сопровождаться большим числом осложнений (инфицирование и т. д.).
Имеются отдельные сообщения о применении интрадуральной спинальной эндоскопии при лечении гидроцефалии и ассоциированных с ней состояний у детей.
При остром возникновении внутричерепной гипертензии используют препараты, обладающие мочегонным действием. К ним относятся: фуросемид (внутримышечно) — иногда в сочетании с раствором сульфата магния, глицерол (per os), маннитол (внутривенно капельно).
При необходимости в длительном лечении гидроцефалии в первую очередь назначается ацетазоламид (Диакарб) — диуретик из группы ингибиторов карбоангидразы (фермент, катализирующий обратимую реакцию гидратации диоксида углерода и последующую диссоциацию угольной кислоты). Действие ацетазоламида связано с супрессией карбоангидразы в сплетениях желудочков головного мозга и со снижением продукции СМЖ (гиполикворное действие). Побочные эффекты ацетазоламида (ацидоз и одышка) систематически корригируют назначением бикарбоната натрия (0,5 г 3 раза в день).
Пациентам с гидроцефалией в возрасте до 3 лет необходимо назначение препаратов витамина D и кальция. Помимо кальция, из минеральных веществ на фоне терапии ацетазоламидом абсолютно необходима дотация препаратов калия и магния (Аспаркам, Панангин).
Симптоматическое лечение при гидроцефалии определяется индивидуальными показаниями и обычно включает: массаж, лечебную физкультуру, различные виды физиотерапии, метод биологической обратной связи, а также стимулирующую терапию (ноотропные, метаболические, сосудистые препараты и пр.) и т. д. Противосудорожные средства детям с гидроцефалией назначают при наличии соответствующих показаний (симптоматическая эпилепсия и пр.).
Нейродиетологические мероприятия должны быть направлены на поддержание состояния питания, адекватное потребление жидкости, дотацию витаминов и минеральных веществ, при необходимости — питательная поддержка (клиническое питание: энтеральное и/или парентеральное) [2–4].
Профилактика
Поскольку в значительном числе случаев гидроцефалия может быть установлена еще в периоде внутриутробного развития, рекомендуется сонографическое исследование плодов (начиная с 17-й недели гестации). В ряде случаев показано МРТ-исследование, хотя P. Peruzzi и соавт. (2010) указывают, что оно не имеет выраженных диагностических преимуществ по сравнению с ультразвуковыми методами [9].
В целях профилактики гидроцефалии у детей необходимо своевременное выявление и лечение внутриутробных инфекций у их матерей. Необходимо осуществление в полной мере профилактики детского травматизма и нейроинфекций. Для предотвращения миеломенингоцеле показан превентивный прием препаратов фолиевой кислоты [1–4, 7].
Прогноз
Гидроцефалия — церебральная патология, сопряженная со значительным неврологическим дефицитом, потенциальной инвалидизацией и снижением качества жизни. Существует риск формирования необратимых изменений в нервной системе и снижения интеллекта (вплоть до умственной отсталости).
При врожденной и приобретенной гидроцефалии прогноз определяется ранним началом и адекватностью лечения (фармакологического или нейрохирургического).
Серьезным осложнением гидроцефалии может явиться эпилепсия, индуцированная как самой гидроцефалией (структурно-морфологическими изменениями структур мозга), так и установкой дренирующего шунта [1–4, 7].
По данным M. Mataro и соавт. (2001), средние значения IQ у пациентов с гидроцефалией снижены по ряду вербальных и невербальных функций. Среди получавших адекватную терапию пациентов в 40–65% случаев отмечаются нормальные показатели интеллектуальных функций [10].
Литература
В. М. Студеникин, доктор медицинских наук, профессор, академик РАЕ
ООО НПСМЦ «Дрим Клиник», Москва
Гидроцефалия у детей: только факты/ В. М. Студеникин
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 66-69
Теги: цефалгия, головной мозг, ликвор, внутричерепная гипертензия
.gif)