костный мозг как поддерживать
Когда нужна пересадка костного мозга?
Пересадка костного мозга — это метод лечения, который используется при различных заболеваниях крови, преимущественно онкологического характера. Его актуальность постоянно растет, поскольку, согласно данным ВОЗ, только лейкемией и лимфомой заболевают до 600 тыс. человек ежегодно. На сегодняшний день количество трансплантаций, выполненных в мире, приближается к 2 млн.
Что такое костный мозг?
Он представляет собой мягкую губчатую ткань внутри костей. В костном мозге из стволовых клеток производится большая часть клеток крови. На самом раннем этапе развития стволовые клетки называются плюрипотентными — они способны превратиться в любую другую клетку нашего организма. Суть пересадки костного мозга как раз и состоит в том, чтобы у человека появились новые, здоровые плюрипотентные стволовые клетки взамен поврежденных.
Что такое пересадка костного мозга?
Первая успешная трансплантация такого рода была проведена еще в 1968 году. С тех пор процедура многократно совершенствовалась. Сегодня в ней выделяют три этапа:
Зачем нужна трансплантация?
Костный мозг пациента может быть поврежден из-за воздействия многих факторов. Наиболее частым из них становится онкологическое заболевание, которое поражает стволовые клетки, в результате чего они теряют способность дифференцироваться и превращаться в зрелые, функционально полноценные клетки крови.
Иногда ткани костного мозга могут необратимо повреждаться под действием длительной химиотерапии или интенсивного лучевого лечения других типов злокачественных опухолей. Соответственно, пересадка может использоваться для:
Важно понимать, что операция по пересадке костного мозга — крайне сложная медицинская манипуляция. Применять ее следует только при наличии строгих показаний. В каждом отдельном случае риски и преимущества такого лечения должны быть тщательно взвешены в ходе обсуждения с лечащим врачом и специалистами по трансплантации.
При каких заболеваниях показана такая пересадка?
Чаще всего процедуру проводят при следующих патологиях:
Типы трансплантации костного мозга
Классифицируют такие процедуры по типу донора и выделяют следующие виды манипуляций:
Центр трансплантации костного мозга клиники «Анадолу»
На базе нашего медицинского центра с 2010 года функционирует специализированный центр пересадки костного мозга. В среднем врачи «Анадолу» проводят 250 пересадок в год у пациентов от 16 лет и старше.
В состав центра входят амбулатория, клиническое отделение трансплантации костного мозга и три лаборатории: генетического типирования, гемофореза, криоконсервации и обработки стволовых клеток. Наши специалисты — высококвалифицированные трансплантологи и гематологи, владеющие всеми современными методиками пересадки костного мозга. В своей работе они неукоснительно следуют международным протоколам лечения онкологических заболеваний крови и соблюдают все меры предосторожности и безопасности.
Отделение трансплантации костного мозга «Анадолу» работает не только с международным, но и турецким банком костного мозга, который позволяет максимально быстро — всего за несколько недель — подобрать подходящего донора. В мировом регистре этот процесс может занимать несколько месяцев.
Рацион для укрепления костей: какие продукты добавить?
В нашем организме 206 костей, но насколько они прочные и крепкие? Когда мы говорим о хорошем самочувствии, здоровье скелета – это последнее, о чем мы вспоминаем.
Кости скелета накапливают прочность и силу до 25 лет, а после 30-ти они постепенно начинают терять свою прочность, если постоянно не поддерживать физическую активность и баланс необходимых минералов – кальция, магния, фосфора.
Почему важно помнить о здоровье костей?
Здоровье костей не менее важно, чем здоровье любых других органов тела, особенно для женщин, так как плотность костей уменьшается после менопаузы. У женщин остеопороз встречается почти в 50% случаев. Потеря плотности кости может привести к остеопорозу, который, в свою очередь, грозит переломами при малейших нагрузках, тем самым уменьшая подвижность. Остеопорозом страдают и мужчины, но гораздо реже (всего около 4% населения) и в более позднем возрасте – около 70 лет.
Чем опасно это заболевание? Кости при нем становятся пористыми и хрупкими, поэтому, компрессия (сжатие) или резкие воздействия (при падениях, неловких движениях) могут вести к переломам. Чаще всего страдают позвонки, шейка бедра и плечевая кость.
Как и при всех других болезнях, профилактика – это основа борьбы с остеопорозом. Важно обращать внимание на здоровье ваших костей сейчас, независимо от того, сколько вам лет. Прочность костей достигается за счет регулярных упражнений (особенно силовых тренировок в комбинации с аэробными нагрузками) и включения в свой рацион продуктов для крепких костей.
Что влияет на наши кости?
Начнем с того, что костная масса на 80% определяется генетикой, а на остальное влияют такие факторы окружающей среды, как диета и физические упражнения. Поэтому 20% проблем со скелетом зависит от того, что происходит в детском и подростковом возрасте. В течение всей фазы роста скелета, крайне важно получить достаточное количество кальция и витамина D для наращивания костной массы. Кальций наиболее активно откладывается в костях именно в этот период. В дальнейшем кости только реминерализуются, то есть обновляются, но уже не растут.
Одного только кальция для крепости скелета недостаточно. Нужен еще и витамин D. Поступая с пищей или образуясь в коже после пребывания на солнце, он подвергается серии преобразований в организме, но, в конечном счете, активная форма витамина D связывается с рецептором витамина D в кишечнике, и это необходимо для всасывания кальция из кишечника в кровь.
Что важно знать об усвоении минералов?
Итак, для здоровья костей нужны не только источники кальция в рационе, но и витамин D, чтобы кальций мог усвоиться. Между тем, важно избегать приема железосодержащих добавок или даже употребления продуктов, богатых железом вместе с кальций-содержащими продуктами, поскольку железо и кальций препятствуют усвоению друг друга.
Помимо кальция, в построении костной ткани участвуют фосфор и магний. Они придают костям прочность и эластичность, формируют их пористую структуру. Чтобы кости были одновременно прочными и эластичными, важен баланс этих веществ в питании, а если одной только пищи недостаточно – нужно принимать добавки с кальцием, магнием и фосфатами.
Какие продукты могут пополнить запасы кальция, а также дают порцию необходимых витамина D, магния и фосфора?
Традиционное коровье (козье, кобылье, верблюжье молоко) все чаще заменяют растительными альтернативами (миндаль, три ореха, соя, овес, банан, кунжут и т. д.) важно помнить, кальций содержится и хорошо усваивается только из настоящих молочных продуктов.
Причем, чтобы кальций полноценно усвоился, эти продукты не должны быть с 0%-ной жирностью. Без жира не будет витамина D, а значит, кальций не будет полноценно усваиваться организмом. Поэтому, если вам нужно укрепить кости скелета и пополнить запасы кальция – помимо цельного молока, которое переносят не все люди, обратите внимание на греческий йогурт, сыр, творог и кефир.
Белок: но лучше – животный!
Специалисты рекомендуют для пациентов с остеопорозом животный белок, поскольку есть научные доказательства [1] того, что диеты с высоким содержанием белка важны для здоровья костей. Эксперты рекомендуют получать дозу белка из сардин и анчоусов, так как они богаты кальцием и витамином D. Менее полезным, но все еще хорошим источником белка будет стейк, поскольку высокое содержание железа может препятствовать усвоению кальция.
Продукты питания, использующиеся в средиземноморской диете
Исследования показали [2], что женщины, которые придерживались этого плана питания, имели более высокую плотность костной ткани. Средиземноморская диета включает: овощи и фрукты, рыбу, морепродукты, оливковое масло, сыр и йогурт, цельное зерно.
Овощи семейства крестоцветных
Существуют некоторые доказательства, что плотность костей у веганов не такая хорошая, как у тех, кто придерживается «более сбалансированной диеты», но необходимы дополнительные исследования. Есть растительная пища, которая также может укрепить кости. Овощи семейства крестоцветных, такие как брокколи, капуста и цветная капуста, богаты кальцием. То, что их потребление снижает количество переломов у женщин в постменопаузе [3], является еще одной причиной, чтобы принять на вооружение новые рецепты с этой группой овощей.
Овощи, богатые витамином К
Грибы, выращенные под влиянием ультрафиолета
Какие продукты богаты витамином D?
Яйца, лосось, молоко, йогурт, сардины и сельдь – это продукты, которые полезны для скелета. И конечно, пока лето, нужно чаще бывать на солнышке. Тем не менее, метаболизм витамина D является сложным процессом, и даже адекватное потребление, регулярные прогулки под солнцем могут привести к дефициту витамина D. В этом случае, на помощь придут добавки витамина D и кальция.
Сколько в граммах?
Взрослые должны получать 1000 мг кальция и 200 международных единиц (МЕ) витамина D в день. Если вам за 50 лет, принимайте 1200 мг кальция и 400–600 МЕ витамина D в день. Хотя кальций и витамин D можно принимать в виде добавок, лучше всего получать их за счет естественной диеты.
Влияние алкоголя
Любителям алкоголя стоит задумать о здоровье скелета. Известно, что алкогольные напитки вредны для здоровья костей. Алкоголь вымывает кальций из костей в мочу. Это справедливо для тех, кто пьет более 2 стаканов пива в день или более 50 г крепкого алкоголя.
[1] Mangano KM, Sahni S, Kerstetter JE. Dietary protein is beneficial to bone health under conditions of adequate calcium intake: an update on clinical research. Curr Opin Clin Nutr Metab Care. 2014;17(1):69‐74. doi:10.1097/MCO.0000000000000013
[2] Maltais ML, Desroches J, Dionne IJ. Changes in muscle mass and strength after menopause. J Musculoskelet Neuronal Interact. 2009;9(4):186‐197.
[3] Blekkenhorst LC, Hodgson JM, Lewis JR, et al. Vegetable and Fruit Intake and Fracture-Related Hospitalisations: A Prospective Study of Older Women. Nutrients. 2017;9(5):511. Published 2017 May 18. doi:10.3390/nu9050511
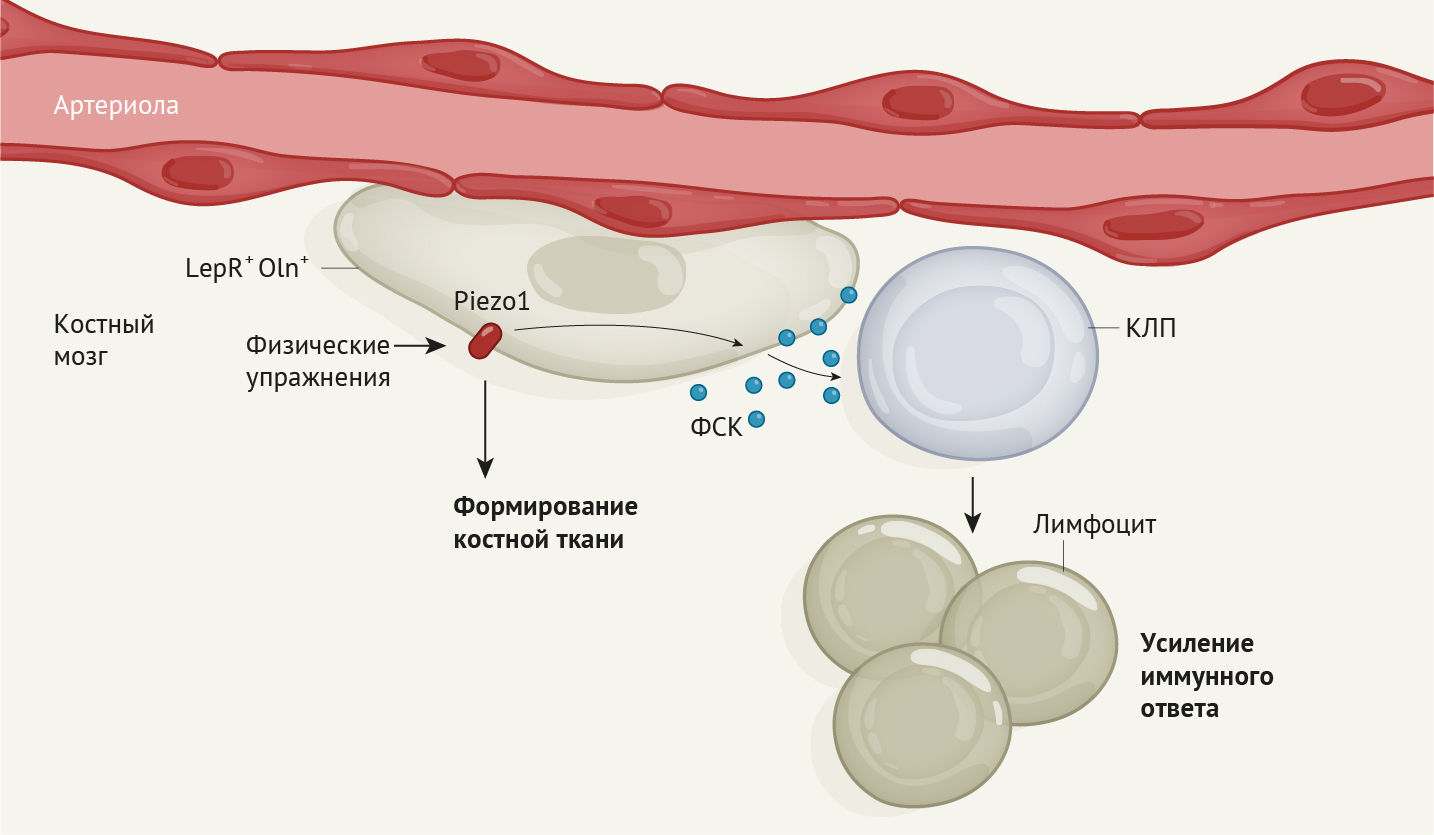
Физическая нагрузка стимулирует иммунные клетки костного мозга
В костном мозге был обнаружен особый тип предшественников остеоцитов, который, как выяснилось, помогает поддерживать образование иммунных клеток лимфоцитов в ответ на физические упражнения.
В костном мозге по-настоящему тесно от клеток. Бок о бок сосуществует много типов стволовых клеток [1, 2] и клеток-предшественников (например, предшественников иммунокомпетентных клеток). Их жизнедеятельность поддерживается за счет соседей, которые создают специальную защитную среду для стволовых клеток, называемую нишей. Взаимодействие между клетками ниши, также известными как стромальные клетки, и ранними предшественниками иммунных клеток в костном мозге изучено плохо. Понимание того, как координируется это взаимодействие, поможет лучше понять, как образуются предшественники иммунных клеток. В своей статье в «Nature» Shen с соавт. [3] решили часть этой загадки, определив роль физической нагрузки в процессе стимулирования связи между одним типом стромальных клеток и предшественниками иммунокомпетентных клеток у мышей, что в итоге помогло организму животных бороться с инфекцией.
Затем Shen с соавт. вывели генетически мутантных мышей, у которых Oln + клетки были лишены способности кодировать ФСК. Отсутствие этого фактора у Oln + клеток в итоге не влияло на гемопоэтические стволовые клетки или большинство иных типов гемопоэтических клеток-предшественников в костном мозге. Тем не менее, это привело к значительному уменьшению численности одного специфического типа гемопоэтических клеток — клеток-предшественников лимфопоэза (КПЛ), из которых развиваются лимфоциты. В поддержку гипотезы о том, что Oln + клетки способствуют образованию и поддержанию пула КПЛ, авторы исследования продемонстрировали, что Oln + клетки и КПЛ располагаются близко друг к другу в костном мозге. Затем ученые заразили мутантных мышей болезнетворной бактерией Listeria monocytogenes, от которой обычно организм очищают лимфоциты. Уничтожение патогенов в организме животных-мутантов происходило гораздо менее эффективно, чем у животных из группы контроля. Вследствие снижения численности КПЛ в организме животных не производились в достаточном количестве лимфоциты.
Известно, что механическая стимуляция костей во время выполнения упражнений способствует их формированию [6]. В заключительной серии экспериментов Shen с соавт. поместили мышей в клетки с беговыми колесами и обнаружили, что бег приводит к увеличению количества как Oln + клеток, так и КПЛ в костном мозге. Ученые выявили экспрессию белка механочувствительного ионного канала Piezo1 клетками Oln + и обнаружили, что у генетической линии мышей, у которых отсутствует этот белок, количество КПЛ аномально низкое. Таким образом, ученые открыли ранее неизвестный путь, с помощью которого физическая нагрузка, воспринимаемая через механочувствительный белок Piezo1, запускает экспрессию ФСК в клетках-предшественниках остеогенеза для поддержки функционирования КПЛ. В конечном счете, так контролируется часть функций иммунной системы (рис. 1).
Открытие того, что механочувствительные клетки-предшественники остеогенеза участвуют в борьбе с бактериальными инфекциями, впечатляет. Известно, что физические нагрузки могут стимулировать иммунную систему [7], однако успех работы Shen с соавт. показывает, почему это так. У результатов данной работы есть прямое клиническое применение. К примеру, существование механизма, раскрытого учеными в текущем исследовании, может быть использовано для разработки более эффективных методов усиления иммунного клеточного ответа (его запуск с помощью физических упражнений). Логичным следующим шагом станет проверка, действительно ли бег может улучшить элиминацию бактериальных патогенов у мышей. Еще один ключевой вопрос, который необходимо разрешить, заключается в том, поможет ли увеличение количества Oln + клеток и КПЛ в костном мозге обеспечить защиту от иных болезнетворных бактерий или даже вирусов, и может ли это усилить ответ на действие вакцинации.
Авторы также обнаружили, что количество ниш Oln + и количество КПЛ ниже в костном мозге 18-месячных мышей, чем их 2-месячных собратьев. Пожилые животные также активны [8], поэтому на снижение количества ниш и КПЛ, связанное со старением, влияют другие факторы, помимо снижения двигательной активности.
Крайне важно исследовать, к примеру, изменяется ли способ, с помощью которого ниши Oln + воспринимают механическую стимуляцию с течением времени. Или какие эпигенетические изменения (модификации ДНК, которые могут изменять экспрессию гена без изменения самой последовательности нуклеотидов ДНК) в старых Oln + клетках способствуют снижению эффективности восприятия механической стимуляции для генерации сигнальных молекул, таких как ФСК.
Хорошо известно, что механочувствительность играет важную роль в физиологии костной ткани, но ключевое значение механических сигналов было также описано для иных типов клеток, например, клеток-предшественников ткани поджелудочной железы, стволовых клеток кишечника и эндотелиальных клеток, образующих выстилку кровеносных сосудов. Хотя о клеточных нишах, которые поддерживают функционирование стволовых клеток вне костного мозга, известно меньше, мелкие сосуды и, следовательно, эндотелиальные клетки являются главными кандидатами на роль структурных элементов таких ниш. Тогда, возможно, что механочувствительность в формирующих ниши эндотелиальных клетках может способствовать поддержанию других типов стволовых клеток и клеток-предшественников. В таком случае работа Shen с соавт. может иметь большое значение для биологии стволовых клеток.
За что отвечает костный мозг

Что такое костный мозг
Костный мозг для кроветворной системы является важнейшим органом, ведь его главная функция – как раз осуществление гемопоэза, или кроветворения. Он непосредственно участвует в создании новых клеток крови взамен тех, что погибли, отмерли. Кроме того, единственной тканью взрослого человека, в которой содержатся незрелые клетки, известные также как стволовые, является именно костный мозг.
Костный мозг бывает двух типов: желтый, который представлен преимущественно жиром, и красный – основной орган кроветворения. В отличие от красного, желтый костный мозг не принимает участия в гемопоэзе.
Во время гемопоэза образуются клетки крови. Стартует гемопоэз в раннем эмбриональном периоде. Соответственно, существуют как эмбриональные кроветворные органы, так и те, что функционируют после рождения. К органам, которые отвечают за гемопоэз во время эмбрионального периода, относят желточный мешок, фетальную печень, селезенку и костный мозг. В желточном мешке появляются первые кроветворные стволовые клетки. Происходит это на 3-й неделе эмбриогенеза. Незадолго после, от 3-го месяца и до рождения, основным кроветворным органом плода становится печень, поскольку некоторые из стволовых клеток перемещаются туда. С 4-го же месяца эмбриогенеза начинается формирование клеток крови и в костном мозге. Кроме того, в кроветворении у плода участвуют тимус, лимфатические узлы и селезенка. В печени и селезенке сохраняются гемопоэтические стволовые клетки, находящиеся в «спящем» состоянии, чем часто объясняют факт возникновения за пределами костного мозга очагов кроветворения. Такое кроветворение называется экстрамедуллярным. Возникает оно при онкологических заболеваниях крови и в результате чрезмерной стимуляции гемопоэза.

Расположение гемопоэтической ткани у взрослого человека следующее: в костях таза ее больше всего – 40%, в телах позвонков значительно меньше – 28%, в костях черепа она составляет 13%, в эпифизах трубчатых костей и ребрах – 8%, в грудине меньше всего – только 2%. Оставшуюся часть костномозговых полостей занимает желтый костный мозг, являющийся, как вы помните, жировой тканью. При этом красный и желтый костный мозг находятся в равном соотношении: 1:1.
Структурно красный костный мозг подразделяется на: экстраваскулярный (собственно, гемопоэтическая ткань) и васкулярный, который состоит из широких венозных сосудов, называемых синусами. В сети ретикулиновых волокон внутри костных трабекул находится желеподобный дисперсный материал, который и является гемопоэтической тканью.
Кровоснабжение костного мозга называется перфузией. Его осуществляют основная питающая артерия и ее малые терминальные артериолы. Отток же крови происходит таким образом: по венозным капиллярам собирается кровь в центральный венозный синус через венозные сосуды. Стенки венозных сосудов состоят из следующих трех слоев клеток: адвентиции, базальной мембраны и эндотелия. Именно в ретикулуме – тонкой сети волокон соединительной ткани, образованной отростками адвентициальных клеток, располагаются кроветворные клетки. На объем гемопоэтического пространства влияют изменения в адвентициальных клетках: количество кроветворных клеток снижается, когда адвентициальные клетки увеличиваются из-за повышения содержания в них жира. Если рассматривать эту картину под микроскопом, она выглядит как трансформация красного костного мозга в желтый.
В тот момент, когда требования к кроветворению повышаются – адвентициальные клетки уменьшаются, тем самым способствуя увеличению гемопоэтического компонента костного мозга.
За что отвечает красный костный мозг

Гемопоэз объединяет два больших отдела кроветворения: лимфопоэз и миелопоэз.
Эритроциты, которые также называют «красные кровяные тельца» – клетки, не имеющие ядра, которым присуща форма двояковогнутого диска. Она поддерживается в эритроцитах благодаря спектрину (стабилизирующему белку мембраны). Размер эритроцита в норме колеблется между 7,5 мкм и 8,3 мкм, а продолжительность жизни составляет 90-120 дней. Всем известные основные группы крови (I, II, III, IV) выделяют на основании антигенных свойств эритроцитов. Функцию эритроциты выполняют чрезвычайно важную – они транспортируют дыхательные газы. Цитоплазма эритроцита заполнена гемоглобином на 96%. Это хромопротеид, состоящий из двух частей: глобина и гема. Первая является белковой, а вторая – небелковой и представляет собой комплекс протопорфирина IX и железа. Кислород из альвеол легких транспортируется к клеткам всего организма именно благодаря гемоглобину, и наоборот, от клеток к альвеолам – с помощью углекислого газа. В норме каждая молекула гемоглобина содержит две пары идентичных белковых цепей. Их обозначают буквами α и β из греческого алфавита. В зависимости от состава этих цепей различают три вида гемоглобина: эмбриональный, фетальный и гемоглобин взрослых.
В периферической крови помимо зрелых эритроцитов можно обнаружить молодые эритроциты – ретикулоциты. Это клетки без ядра, но содержат в себе большое количество РНК и рибосом, которые имеют мембранные рецепторы к трансферрину. РНК ретикулоцитов продолжает производить гемоглобин. На этой стадии возможна выработка гемоглобина до 30% от общего количества в эритроците. Большая же часть синтезируются на преретикулоцитных стадиях дифференцировки клетки – 70-80% гемоглобина. Когда ретикулоцит превращается в зрелый эритроцит, он больше не может производить гемоглобин, так как теряет РНК. В костном мозге эритроцит на стадии ретикулоцита находится в течение одного дня, а затем еще один день – в периферической крови.

Если специфическая зернистость отсутствует, лейкоциты называются агранулоцитами, а если присутствует – гранулоцитами. К первым относятся лимфоциты и моноциты.
Гранулоциты же отличаются между собой характером специфической зернистости и бывают трех видов:
Благодаря л ейкоцитам в организме реализуется защитная функция – иммунитет, который бывает специфический и неспецифический.
В одном из проявлений неспецифического иммунитета участвуют нейтрофилы, моноциты и тканевые макрофаги (в них превращаются моноциты после того, как выходят за пределы кровеносного русла). Они фагоцитируют (захватывают) с последующим лизисом (растворением) микробы, токсины и клеточный детрит (проще говоря, мусор). Эозинофилы обеспечивают защиту от паразитов и участвуют в аллергических реакциях (как и базофилы).
Лимфоциты осуществляют реакции специфического иммунитета, будь то врожденного или приобретенного. Специфический иммунитет, в свою очередь, бывает гуморальный и клеточный. Гуморальный иммунитет реализуется благодаря синтезу В-лимфоцитами иммуноглобулинов классов A, M, G, E, D; а клеточный – с помощью многообразных функций Т-лимфоцитов. Приобретенный иммунитет может формироваться естественным путем, вследствие различных инфекционных заболеваний, или в результате иммунизации организма.
Размеры лейкоцитов составляют от 6 мкм (малые лимфоциты) до 14 мкм (моноциты).
Лейкоциты отличаются между собой не только внешним видом и функцией, но и продолжительностью жизни. Так, например, длительность жизни лимфоцитов колеблется между несколькими часами и десятками лет. Моноциты циркулируют в крови на протяжении 72 часов, а потом выходят в ткани, где превращаются в фиксированные или мигрирующие макрофаги. Нейтрофилы находятся в крови 4-10 ч, с последующим выходом в ткани.
Тромбоциты – третий форменный элемент крови. Их приравнивают к истинным клеткам, хотя они и не являются таковыми. На самом деле, это частицы отшнуровавшейся цитоплазмы мегакариоцитов костного мозга, так называемые кровяные пластинки. Тромбоциты характеризуются свойствами агрегации (склеивания) и адгезии (прилипания). Их участие в механизмах свертывания крови и фибринолиза определяется наличием особых биологически активных веществ. Также они помогают поддерживать нормальную резистентность и функционирование микрососудов (ангиотрофическая функция). Размер тромбоцитов составляет 1-2 мкм, а продолжительность жизни – 8 суток.
За что отвечает желтый костный мозг
Желтый костный мозг обычно находится в диафизах трубчатых костей. Состоит из ретикулярной ткани и клеток адипоцитов, которые содержат специальный пигмент-липохром в центре полости длинных костей, а снаружи ее окружает слой красного костного мозга. Жир из адипоцитов, в случае крайней необходимости, например, после длительного голодания, организм может использовать в качестве источника энергии. В обычных условиях желтый костный мозг не участвует в гемопоэзе, но в исключительных случаях, например, после сильной кровопотери или при острой анемии, часть желтого костного мозга может превратиться в красный, чтобы ускорить восстановление крови.
Главные функции костного мозга

Недостаточная активность костного мозга может вызывать такие состояния как:
Кроме того, если вспомнить, что именно благодаря кровотоку все ткани и органы получают кислород и питательные вещества, то становится ясно: от костного мозга зависит абсолютно каждая клетка человеческого тела.
Также костный мозг – это стержневой элемент лимфатической системы. Все лимфоциты зарождаются именно в этой ткани. И если учесть, что иммунная система напрямую зависит от работоспособности лимфатической, то окажется, что без костного мозга не существовало бы и иммунитета. Большинство антител крови, которые защищают организм от патогенов, синтезируются именно в костном мозге.
Болезни костного мозга
Независимо от того, что вызвало повреждение ткани, особенно ее красной части – онкологическое заболевание или другие факторы – это всегда представляет угрозу для здоровья и жизни человека.
Миелопролиферативные расстройства
Нарушения со столь сложным названием возникают, если стволовые клетки размножаются неправильно. Таких заболеваний существует несколько типов:
Апластическая анемия

Апластическая анемия может быть приобретенной или врожденной. В первом случае стволовые клетки могут потерять способность превращаться в кровяные из-за воздействия токсинов, радиации или после тяжелых инфекционных заболеваний. Кроме того, эта болезнь иногда может проявляться как осложнение некоторых аутоиммунных нарушений, например, волчанки или ревматоидного артрита.
Лейкемия
Лейкемия, или “белокровие” – это вид рака, при котором в периферической крови появляется большое количество белых кровяных телец – лейкоцитов. Эти заболевания объединены под общим названием – гемобластозы.
Существуют такие принципы разделения гемобластозов:
Ученым трудно сказать, что именно вызывает лейкоз. Но принято считать, что повышают риск онкологических процессов в костном мозге облучение, влияние некоторых химических веществ, а также ряд генетических болезней.
Пересадка костного мозга: как, кому и зачем

Пересадка костного мозга – это, по сути, внедрение в организм пациента необходимых стволовых клеток. Стволовые клетки содержатся в эмбрионе, костном мозге, периферической крови человека, а также в пуповинной крови. Источником для пересадки могут служить все перечисленные варианты, кроме первого. Во время процедуры трансплантации собранные стволовые клетки внутривенно вводятся пациенту. После проникновения в кровоток донорские гемопоэтические стволовые частицы перемещаются в костный мозг больного, где, в случае удачно проведенной процедуры, начинают производить эритроциты, тромбоциты и лейкоциты.
На то, чтобы пересаженный материал прижился, обычно необходимо около 2-4 недель. Пересадка помогает больному организму восстановить способность самостоятельно производить необходимые элементы крови. К этой процедуре прибегают для лечения как онкологических, так и болезней другого типа.
Рассмотрим виды трансплантации костного мозга. Существует:
Возможные риски пересадки костного мозга
Несмотря на, казалось бы, простоту процедуры, на самом деле пересадка костного мозга не лишена серьезных рисков. После введение донорского материала у пациента может возникнуть реакция, которую называют «трансплантат против хозяина» (ТПХ). Это считается одним из самых опасных и самых частых осложнений после аллогенной пересадки. Суть реакции в том, что донорский костный мозг воспринимает организм реципиента как врага и начинает работать против него. Реакция «трансплантат против хозяина» случается почти в 40% случаев пересадки стволовых клеток. Это противостояние может привести даже к смерти реципиента. Считается, что риск возникновения реакции ТПХ увеличивается, если пациент старше 30 лет. В течение долгого времени врачи не брались пересаживать костный мозг людям в возрасте за 50, риск смертности после процедуры у них чрезвычайно высок. В наши дни к возрастному цензу врачи относятся уже с меньшей опаской.
Помимо реакции ТПХ, как осложнение на пересадку могут развиваться офтальмологические, эндокринные, легочные, неврологические, скелетно-мышечные, иммунные, инфекционные болезни, сердечная недостаточность, прогрессирование онкологического заболевания.
Эритроциты, лейкоциты, тромбоциты и компоненты лимфатической системы – все они производятся костным мозгом. О нем вспоминают редко и, как правило, только в случаях серьезных заболеваний. Костный мозг нельзя увидеть или прикоснуться к нему, а если с ним что-то не так, он не болит. Тем не менее это одна из наиболее важных тканей в организме и сбои в ее работе во многих случаях заканчиваются летальным исходом.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru