в каком слое эпидермиса находятся клетки лангерганса
Клетки Лангерганса
Наша кожа, являясь отдельным органом тела, защищает нас от внешних повреждающих факторов (механических, температурных) и не только. Кожа – это «совершенный» барьер, защищающий организм даже от патогенов, находящихся на ее поверхности. Но если барьерная система повреждается в силу разных причин, и патоген проникает через роговой слой, то к его уничтожению подключаются клетки иммунной системы.
Иммунная система включает в себя защитную систему (врожденная неспецифическая защита) и адаптивную (специфическая защита).
Основная деятельность неспецифической защитной системы направлена на распознавание патогенов и предотвращение проникновения последних в организм (или их немедленное уничтожение).
А специфическая защитная система не только распознает, но и запоминает патоген «в лицо» и способна быстро развернуть «борьбу» против него.
Специфические и неспецифические звенья иммунной системы тесно взаимодействуют. И главным связующим звеном между ними являются клетки Лангерганса, которые выступают в роли носителей информации о «вторжении» патогенов.
Другими словами, сеть клеток Лангерганса проводит постоянное сканирование субстанций, поступающих во внутреннюю среду через кожные покровы, будучи в любой момент готовой инициировать иммунный ответ на возможный патоген. Следует помнить, что любой микроорганизм не может проникнуть в кровь через неповрежденную кожу, минуя клетки Лангерганса.
Клетки Лангерганса составляют небольшой процент от клеток эпидермиса. При этом они тесно переплетаются друг с другом своими отростками, создавая тем самым своеобразную защитную оболочку человеческого тела. Указанная сеть из клеток Лангерганса покрывает всю площадь кожи и эффективно улавливает любые антигенные субстанции, проникающие трансдермальным путем.
Клетки Лангерганса могут очень долго удерживать на своей поверхности захваченные антигены, участвуя в иммунологической памяти. Они способны презентовать антигены не только в эпидермисе, но и в дерме.
Отростки клеток Лангерганса достигают до верхних слоев эпидермиса, поэтому они вполне доступны для биологически активных веществ, наносимых на кожу.
Если Вы являетесь косметологом, рекомендуем пройти регистрацию и после нашего подтверждения Вам станет доступна дополнительная профессиональная информация.
В каком слое эпидермиса находятся клетки лангерганса
Как следует из современного названия болезни, основным элементом морфологического субстрата является патологическая клетка Лангерганса (ПКЛ), которая фенотипически сходна с нормальной клеткой Лангерганса, но имеет некоторые иммуногистохимические отличия.
Первое упоминание о денритических клетках относится к 1868 г., когда P. Langerhans описал новый тип клеток, обнаруженных в эпидермисе кожи при окраске хлоридом золота и предположил, что они происходят из нервной ткани. Впоследствии эти клетки получили название «клетки Лангерганса», было доказано их костно-мозговое происхождение.
В 1961 г. М. S. Birbeck и соавт., изучая ультраструктуру клетки Лангерганса, выявили уникальное специфическое образование в ее цитоплазме, которое было названо «гранула Бирбека». В настоящее время это наиболее надежный морфологический маркер этих клеток. Позже, в 1973 г., С. Nezelof и соавт., изучая гистологическую картину гистиоцитозов, обнаружили, что именно клетки Лангерганса составляют морфологический субстрат гистиоцитоза X.
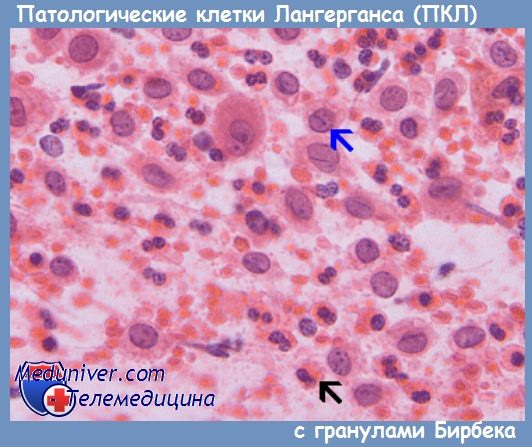
При изучении гистологических срезов, окрашенных гематоксилином и эозином, патологическая клетка Лангерганса выглядит как мононуклеарный элемент с диаметром 12—25 мкм. Клетка содержит центрально или слегка эксцентрично расположенное ядро, умеренное количество гомогенной розовой цитоплазмы с хорошо очерченными краями.
Редко в цитоплазме выявляются вакуоли или признаки фагоцитарной активности. Ядро часто складчатое, с зазубренными краями или дольчатое с нежным или негомогенным гранулярным хроматином; содержит одно—три базофильных ядрышка средней величины. Достоверная идентификация патологических клеток Лангерганса требует проведения электронной микроскопии.
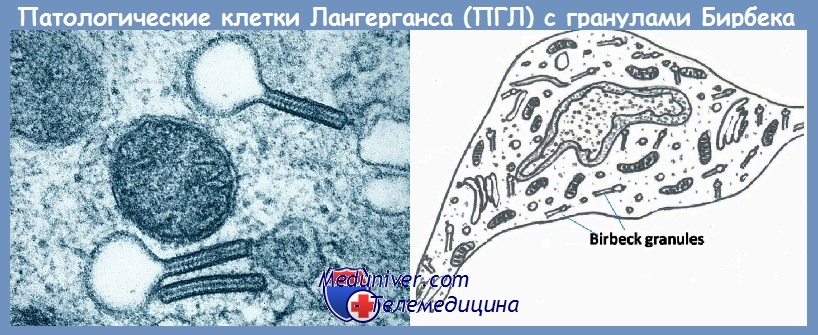
При ультраструктурном исследовании цитоплазма имеет зазубренный контур и псевдоподии. Она обильная, со множественными органеллами, включая шероховатую эндоплазматическую сеть, свободные полирибосомы, лизосомы и митохондрии; менее выражена гладкая эндоплазматическая сеть; иногда выявляется комплекс Гольджи. Уникальной цитоплазматической структурой, отличающей патологические клетки Лангерганса от других гистиоцитов, является гранула Бирбека.
Она имеет пенталамеллярную структуру разной длины. Иногда заканчивается расширением в виде пузырька, придающим ей форму теннисной ракетки. Гранулы Бирбека расположены по соседству или сливаются с цитоплазматической мембраной. Функции этой структуры неясны, однако ее выявление необходимо для четкой идентификации клетки.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Факторы старения кожи. Методики anti age терапии.
Ученые доказали, что старение кожи начинается сразу же после полового созревания. В 35-50 лет становится более заметным и длится приблизительно до 60 лет. После чего наступает относительно стабильный период.
Основные факторы старения
Во — первых, наследственно (генетически) запрограммированные изменения затрагивающие практически все слои кожи;
Во — вторых, физиологическое (возрастное) снижение синтеза гормонов в организме. Такие гормоны, как гормон роста, тестостерон, DHEA (дегидроэпиандростерон), мелатонин и др. незаменимы для физического здоровья и регенерации клеток всего организма, в том числе и кожи. Начиная с 20-летнего возраста выработка этих гормонов постепенно снижается;
И в — третьих, фотостарение – воздействие ультрафиолетовых лучей способствует образованию свободных радикалов, отрицательно действующих на структуры клеток кожи, значительно изменяя механизмы клеточного восстановления.
Старение кожи — это сложный многокомпонентный, многофакторный и растянутый во времени процесс.
На сегодняшний день нет однозначного определения что же такое старение кожи, однако уже сейчас понятно, что оно обусловлено накоплением «дефектов», как в клетках, так и в её межклеточных структурах.
Суммарный итог этих возрастных изменений таков:
Сегодня, благодаря достижениям современной науки, уже можно понять и объяснить многие процессы, происходящие в дерме со течением временем. Поэтому с уверенностью можно утверждать, что грамотное и своевременное использование методик косметологического ухода в сочетании со здоровым образом жизни способно если не остановить процесс биологического старения кожи то, по крайней мере, сделать его проявления менее выраженными.
Современное понимание причин и механизмов старения кожи позволяет объединить методы эстетической медицины в единую Anti-age программу, которая в условиях нашей клиники включает в себя:
В настоящее время для каждого профессионального специалиста anti-age на первое место выходит системный подход к организму с учетом иерархии и систем внутренней регуляции.
Это понимают и профессионалы, и клиенты, обращающиеся за омолаживающими процедурами с требованиями уровня их оказания выше посредственно среднего. Основной акцент на данном этапе развития эстетической индустрии ставится на самого человека, на глубокое понимание его внутренних системных процессов.
От этого синтеза в выигрыше оказываются решительно все. Клиент получает высокоэффективную услугу, результат от которой становится самоподдерживающимся, что и реализует истинный anti-age эффект. Специалист имеет уникальную возможность не просто воздействовать на тело, но делать это максимально целенаправленно и осознанно.
Здоровье проявляет себя через красоту, а красота манифестирует истинное самоподдерживающееся здоровье, и это реализуется через истинный anti-age результат.
Содержание
Дерматология в России
Зарегистрируйтесь!
Если Вы врач, то после регистрации на сайте Вы получите доступ к специальной информации.
Если Вы уже зарегистрированы, введите имя и пароль (форма в верхнем правом углу или здесь).
Лангергансо-клеточный гистиоцитоз
Лангергансо-клеточный гистиоцитоз
В случае LCH гранулематозные поражения, включающие лангерин-позитивные (CD207+) гистиоциты и воспалительный инфильтрат, могут возникать практически в любом органе или системе, но имеют особое сродство к костям, коже, легким и гипофизу (рис. 1).
LCH имеет разнообразную клиническую картину, варьирующую в своих проявлениях от единичных вялотекущих поражений до острых мультисистемных заболеваний. Дети с поражением печени, селезенки или костного мозга подвергаются самому высокому риску смерти от LCH и поэтому рассматриваются как пациенты, имеющие LCH высокого риска.
Хотя клинические результаты лечения неуклонно улучшались в течение последних десятилетий, стандартная химиотерапия (винбластин, преднизон и меркаптопурин) не может гарантировать излечение более 50% детей с высоким риском заболевания, и большинство пациентов имеют отсроченные последствия (5), включая нейродегенеративный синдром, который может возникнуть через годы после того, как пациент предположительно будет вылечен (6, 7).
В обзоре 1998 года Arceci и его коллеги описали тяжелое состояние отсутствия прогресса в терапии LCH, назвав эмпирическое лечение “колесом рулетки” и отметив, что “отсутствие консенсуса возникает из-за имеющейся неопределённости относительно того, является ли LCH в первую очередь опухолевым расстройством, иммунодисрегуляторным расстройством или расстройством с характеристиками перечисленных” (8).
Доброкачественный гистологический фенотип клеток CD207+, сопутствующий воспалительный инфильтрат и характерный местный и системный цитокиновый шторм поддерживают воспалительное происхождение LCH, тогда как клональность, соматические активирующие генные мутации в сигнальном пути митоген-активируемой протеинкиназы (MAPK) и общие мутации с гемопоэтическими предшественниками способствуют переклассификации LCH в миелоидное неопластическое заболевание.
Заболеваемость LCH сходна с детской лимфомой Ходжкина, что ставит вопрос о том, является ли LCH “орфанным заболеванием” или одним из наиболее распространенных детских онкологических заболеваний (9).
Этот пересмотр в классификации не только ограничил разработку рациональных терапевтических стратегий для пациентов с LCH, но и затруднил доступ к финансовым и организационным ресурсам, которые способствуют решению проблем в лечении при других детских неопластических состояниях (10).
Здесь мы рассмотрим историю LCH и обсудим недавние биологические открытия, которые позволяют перевести лечение LCH за пределы эмпирического «колеса рулетки» в эпоху персонализированной медицины.
Краткая история
Первые описания того, что мы теперь называем LCH, появились в начале 1900-х годов в виде отчетов о случаях и серий случаев. Болезнь Хенда-Шюллер-Кристчена, которая описывается как эозинофильная гранулёма костей, несахарный диабет, и экзофтальм у детей ранних лет жизни (11-13).
Болезнь Леттера–Сивеве была описана у младенцев с агрессивными и в целом фатальными системными заболеваниями, включая инфильтрацию кожи, печени, селезенки и костного мозга ретикулоэндотелиальными клетками (рис. 1).
В середине 1900-х годов Фарбер и Лихтенштейн отметили, что биопсии образцов пациентов, умерших от болезни Леттера-Сиве и образцы, полученные от пациентов с клинически легкой эозинофильной гранулемой, были неразличимы, и оба патолога предположили, что эти состояния представляют собой проявления одного заболевания (16, 17).
Лихтенштейн предложил общий диагноз – гистиоцитоз Х, причем Х указывает на неопределенное происхождение клеток. Два десятилетия спустя, с появлением электронной микроскопии, Незелоф и его коллеги идентифицировали уникальную внутриклеточную органеллу, гранулу Бирбека, в очагах поражений при гистиоцитозе Х (рис. 2) (18).
С его точки зрения гранулы Бирбека считались характерными органеллами для эпидермальных клеток Лангерганса, клеток кожи, мононуклеарной фагоцитарной системы. Гистиоцитоз Х был переименован в гистиоцитоз из клеток Лангерганса, отражая концепцию о том, что клетки LCH представляют собой дисфункциональные эпидермальные клетки Лангерганса.
В течение следующих десятилетий в обзорах обсуждался вопрос о том, является ли LCH заболеванием, связанным с трансформированными клетками Лангерганса или нормальными клетками Лангерганса, ставшими патологическими из-за неадекватных воздействий (8).
ЛАНГЕРИН, ВОСПАЛЕНИЕ И LCH
Клетки Лангерганса названы в честь Пола Лангерганса, яркого молодого студента-медика, который работал с новой техникой окрашивания коллоидным золотом в середине 19-го века.
В 1868 году Лангерганс описал популяцию эпидермальных клеток, составляющую примерно 1% эпидермальных клеток, с характерными дендритами, которые он описал как внекожные нервы (20).
Теперь мы знаем, что эпидермальные клетки Лангерганса – это не нервы, а дендритные клетки, гетерогенная группа кроветворных клеток, присутствующая в тканях и лимфоидных органах. В 1970-х годах Штейнман и Кон отличили дендритные клетки от макрофагов на основе специфических морфологических особенностей дендритных клеток и их высокой способности представлять антигены и активировать антигенспецифические Т-клетки (21, 22).
Эпидермальные клетки Лангерганса уникальны среди дендритных клеток тем, что они возникают не из миелоидных клеток-предшественниц в костном мозге, а из клеток–предшественниц желточного мешка и эмбриональных моноцитов печени, которые заселяют кожу до рождения и сохраняются локально в устойчивом состоянии (24, 25).
Однако при тяжелой травме или воспалении моноцитарные клетки периферической крови могут мигрировать в эпидермис и дифференцироваться в клетки, подобные клеткам Лангерганса (26).
Активированные клетки Лангерганса активируются через хемокиновый рецептор CCR7, мигрируют в дренирующие лимфатические узлы, где они представляют антиген Т–клеткам и в конечном итоге подвергаются апоптозу или элиминируют антиген посредством других механизмов (рис. 3А) (27).
Незрелые эпидермальные клетки Лангерганса экспрессируют высокий уровень лангерина (CD207), лектина, необходимого для образования гранул Бирбека, который первоначально считался присущим только для клеток Лангерганса (30).
Гистиоцитарные нарушения обычно характеризуются клеточным фенотипом: LCH сочетает поверхностные маркеры с эпидермальными клетками Лангерганса (CD1a+/CD207+), тогда как поверхностные маркеры ювенильной ксантогранулемы и болезни Эрдгейма–Честера более характерны для макрофагов (CD14+/CD68+/CD163+/фактор XIIIa–положительный).
Поражения у пациентов с гистиоцитарной саркомой или злокачественным гистиоцитозом более агрессивны, чем поражения LCH, с гистологическими признаками макрофагально–моноцитарной клональности, включая CD68 и CD163-позитивность, и более высоким митотическим индексом (31).
В некоторых случаях возникает смешанное заболевание, при котором отдельные поражения имеют различные фенотипы или одно поражение имеет смешанный фенотип (рис. 2) (32).
При поражении LCH патологические дендритные клетки составляют от менее чем 1% и более чем 70% при гранулематозном поражения (медиана – примерно 8%) (33). Остальная часть очага поражения состоит из воспалительного инфильтрата, включающего активированные Т-клетки на фоне цитокинового шторма (34-36).
Иммунная дисрегуляция четко характеризует аспекты патогенеза LCH, хотя механизмы, приводящие к воспалению, остаются неопределенными.
В 1990-х годах Уиллман и его коллеги исследовали неслучайную инактивацию локусов Х-хромосомы и обнаружили, что процент клональных клеток приближается к проценту гистиоцитов CD1a+ в очагах поражения у пациенток с LCH (36).
Хотя это открытие предопределяло характеристику LCH как миелоидного неопластического заболевания, его биологическое значение оставалось неопределенным в течение десятилетий. Несмотря на предположения о клональности клеток Лангерганса (37, 38), не было обнаружено никаких признаков пролиферации внутри очага поражения (34, 36), и грубых геномных изменений выявлено также не было (39).
СОВРЕМЕННОЕ ПРЕДСТАВЛЕНИЕ О LCH
СОМАТИЧЕСКИЕ МУТАЦИИ MAPK-ПУТИ И LCH
Усовершенствованная геномная технология исследования предвещала прорыв в изучении биологии LCH. Используя платформу пиросеквенирования OncoMap, Бадалиан-Вэри и его коллеги идентифицировали мутацию BRAF V600E в 57% поражений LCH (40), находка, которая впоследствии была верифицирована в других сериях наблюдений и обусловлена патогенными клетками LCH (33, 41-44).
BRAF – это центральная киназа сигнально–трансдукционного пути RAS-RAF-MEK, которая участвует во многих клеточных функциях (рис. 4А). Мутация BRAF V600E делает путь MAPK конститутивно активным (46).
Хотя соматические мутации BRAF V600E встречаются в 7% всех случаев онкопатологии человека, они также часто встречаются при доброкачественных образованиях, таких как меланоцитарные невусы и полипы толстой кишки (46, 47).
Секвенирование всего экзома выявило взаимоисключающие мутации, активирующие MAPK-путь, в оставшемся незатронутом «геномном ландшафте», без существенной разницы в частоте мутаций между поражениями низкого и высокого риска (48, 49).
В дополнение к BRAF V600E, другие активирующие мутации в BRAF, включая делеции внутри рамки считывания, слияния и дупликации, были зарегистрированы при поражениях LCH. Дополнительные мутации гена MAPK-пути выявленые in vitro включают вставки или делеции в экзонах 2 и 3 MAP2K1 и редкие мутации ARAF (44, 48-52).
Активирующие соматические мутации в генах рецепторных тирозинкиназ (ERBB3), NRAS и KRAS также были зарегистрированы при поражении LCH у взрослых (44, 49, 53, 54).
В установленной серии соматическая активирующая мутация в гене MAPK-пути была идентифицирована более чем в 85% случаев (51), что согласуется с универсальной активацией внеклеточной сигнально-регулируемой киназы (ERK), наблюдаемой в клетках LCH (рис. 4B) (40, 49).
LCH КАК СЛЕДСТВИЕ НАРУШЕНИЯ ДИФФЕРЕНЦИРОВКИ МИЕЛОИДНЫХ КЛЕТОК
Достижения в изучении онтогенеза дендритных клеток и описательные исследования клеток LCH CD207+ было трудно сопоставить с моделью клеток LCH, представляющих собой трансформированные или активированные эпидермальные клетки Лангерганса.
Были обнаружены альтернативные дендритно-клеточные подклассы, способные экспрессировать лангерин и образовывать гранулы Бирбека, что характерно для тканей в стабильном состоянии с повышенным рекрутированием из крови в ткани во время воспаления (25).
Обширное тканевое распределение CD207+ дендритных клеток включает органы, подверженные риску образования поражений при LCH, в отличие от ограниченного тропизма клеток Лангерганса к эпидермису и дренирующим кожу лимфатическим узлам.
Кроме того, профилирование экспрессии генов при поражении CD207+ LCH показало минимальное пересечение с эпидермальными клетками Лангерганса, но показало относительно повышенную экспрессию генов, связанных с незрелыми предшественниками миелоидных дендритных клеток (36).
Более тщательное изучение дифференцировочного статуса клеток при LCH в очагах поражения выявило гетерогенные субпопуляции CD1a+ с переменной экспрессией CD207+ (55, 56).
Вместе эти данные говорят о том, что клетки при LCH с большей вероятностью возникают в результате дисрегуляции дифференцировки или рекрутирования клеток–предшественниц, полученных из костного мозга, чем из трансформированных или активированных эпидермальных клеток Лангерганса.
BRAF V600E представляет важный биомаркер, с помощью которого можно было изучать гемопоэтические клетки, чтобы определить происхождение патологических клеток при LCH. Удивительно, но мутированные BRAF V600E–позитивные клетки были последовательно идентифицированы в мононуклеарных клетках периферической крови (PBMCs) у пациентов с высоким риском LCH с BRAF V600E-позитивными поражениями, хотя мутированные клетки составляли очень низкий процент этих клеток (обычно 12%) в пораженных областях (19). Микроглия – это резидентные миелоидные клетки центральной нервной системы, которые возникают из желточного мешка во время беременности. Mass et al. сообщалось, что эритромиелоидные предшественники клеток желточного мешка с усиленной экспрессией BRAF V600E могут заселять мозг BRAF V600E-положительной микроглией у мышей с развитием прогрессирующей нейродегенерации у взрослых (29). Поэтому было выдвинуто предположение, что соматические мутации в клетках желточного мешка плода представляют собой источник нейродегенеративного LCH. В исследовании с участием пациентов с LCH персистенция BRAF V600E–позитивных клеток в периферической крови после химиотерапии при отсутствии системных поражений LCH была специфична для пациентов с нейродегенеративным LCH.
Кроме того, исследование биоптатов головного мозга таких пациентов показало периваскулярную инфильтрацию BRAF V600E-позитивными клетками с моноцитарным фенотипом (CD14+CD33+CD163+P2RY12–), что подтверждает роль циркулирующих предшественников, как источника патогенных BRAF V600E–позитивных клеток (рис. 2) (19).
Это наблюдение согласуется с моделью, в которой гемопоэтический клон, вызывающий первоначальные поражения при LCH, сохраняется (или вновь появляется) после предполагаемого излечения и служит резервуаром для будущего нейродегенеративного LCH (рис. 3B). Как и в случае кожного LCH, возможно множественное происхождение (например, желточный мешок и костный мозг).
ЭПИДЕМИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ LCH
Сообщалось, что ежегодная заболеваемость LCH составляет 4,6 случая на 1 миллион детей в возрасте до 15 лет при соотношении мальчиков и девочек 1,2:1 (59).
Предполагаемая заболеваемость среди взрослых составляет 1-2 случая на миллион, хотя LCH, вероятно, недостаточно диагностируется в этой популяции (60).
Раса и этническое происхождение, по-видимому, влияют на риск развития LCH. Статистические исследования в Соединенных Штатах показали рост заболеваемости среди латиноамериканцев и снижение заболеваемости среди чернокожих детей (61, 62).
Кроме того, исследование с участием пациентов с LCH в Техасе показало, что латиноамериканские матери с большей вероятностью имели детей с LCH, чем не латиноамериканские матери (63).
LCH может присутствовать до, после или вместе с другими гистологическими видами рака, часто с общими мутациями, с клональностью, хотя неясно, дает ли LCH в анамнезе повышенный риск развития рака у детей (64, 65).
СОВРЕМЕННЫЕ ПОДХОДЫ К ЛЕЧЕНИЮ
Несмотря на успехи в изучении патогенетических механизмов LCH, современный стандарт первой линии терапии при мультифокальной LCH остается эмпирически назначение химиотерапии.
Общие результаты улучшались в клинических испытаниях LCH за последние десятилетия, хотя выживаемость без прогрессирования среди пациентов высокого риска остается менее чем 50% (см. Таблицу S1 в приложении, доступном вместе с полным текстом этой статьи по адресу NEJM.org) (3, 4, 28, 66, 67).
Наша готовность к резистентности заболевания к стартовой терапии, вероятно, исходит из исторической неопределенности относительно того, считать ли LCH онкопатологией или аутоиммунным заболеванием, что также отражается в тенденции использовать термин “реактивация”, а не на “рецидив».
Однако даже у пациентов с низким риском, для которых показатель ранней смертности невелик, неудачи лечения связаны с повышенным долгосрочным риском осложнений, включая нейродегенерацию (5).
В исследовании LCH-III дети с LCH низкого риска, получавшие в качестве терапии первой линии винбластин и преднизолон в течение 12 месяцев, имели более высокие показатели выживаемости без прогрессирования, чем пациенты, получавшие лечение в течение 6 месяцев (5-летняя частота рецидивов 37% против 54%; Р = 0,03) (4).
Потенциал длительной химиотерапии (12 месяцев против 24 месяцев) для повышения выживаемости без прогрессирования у пациентов с LCH высокого риска в настоящее время тестируется в исследовании LCH-IV frontline therapy, проведенном Обществом гистиоцитов (ClinicalTrials.gov номер, NCT02205762).
В другом многоцентровом исследовании лечение винбластином и преднизоном, как препаратами первой линии, сравнивается с цитарабином на основании гипотезы о том, что клетки-предшественницы LCH, во многом похожие на миелоидные предшественницы при онкопатологии, такой как острый миелоидный лейкоз, могут быть чувствительны к нуклеозидным аналогам (NCT02670707).
Существуют скудные данные, которые можно использовать как клинические рекомендации при состояниях после того, как назначение препаратов первой линии не привело к результату. Аналоги нуклеозидов могут быть обоснованным выбором терапии при LCH, хотя оптимальная дозировка еще не определена.
В исследовании фазы 2 низкие дозы кладрибина редко приводили к излечению после 6 месяцев терапии (68). Напротив, лечение кладрибином и цитарабином, аналогичное лечению острого лейкоза, приводило к очень высоким показателям излечения среди пациентов высокого риска, но было связано с длительной госпитализацией и высокими показателями смертности, связанной с лечением (69,70).
Аллогенная трансплантация гемопоэтических клеток также может оказать лечебный эффект для пациентов с рефрактерным или рецидивирующим LCH: данные американского и европейского регистра с 2000 по 2013 год показали 3-летнюю общую выживаемость от 71 до 77% (71).
Данные серий наблюдений также показали многообещающие результаты при менее агрессивном подходе, при котором монотерапия цитарабином или клофарабином назначается в умеренных дозах в амбулаторных условиях (таблица S2 в приложении) (72, 73).
Данные клинических рекомендаций взрослым с LCH и пациентам с нейродегенеративным LCH ограничены тематическими исследованиями и сериями наблюдений. У взрослых могут наблюдаться поражения смешанного фенотипа, которые могут сосуществовать с другими миелоидными новообразованиями.
Изолированный легочный LCH может развиться у взрослых курильщиков. Винбластин и преднизон могут вызывать серьёзные побочные эффекты у взрослых, и в целом реакция на химиотерапию у взрослых менее устойчива, чем у детей (74, 75).
Клинические подходы к нейродегенеративному LCH исторически были ограничены интерпретацией нейродегенерации как аутоиммунного или паранеопластического феномена. Сообщалось, что внутривенное введение иммуноглобулина уменьшает выраженность симптомов (76).
Однако, если нейродегенеративный LCH является проявлением воспаления, вызванного клональными, активированными MAPK миелоидными клетками в центральной нервной системе, терапия, направленная на LCH, может быть более подходящей (19, 29). На самом деле у некоторых пациентов с нейродегенеративным LCH наблюдаются острые реакции на цитарабин или таргетную терапию вемурафенибом (19, 77).
ТАРГЕТНАЯ ТЕРАПИЯ
Несмотря на открытие мутации BRAF V600E при LCH в 2010 году и существенных доказательств того, что LCH обусловлен патологической активацией MAPK в миелоидных предшественниках, было завершено лишь несколько исследований, направленных на разработку таргетной терапии у детей.
Ранние исследования с участием взрослых с LCH или связанной с ней болезнью Эрдгейма–Честера показали перспективное направление ингибирования MAPK-пути.
В исследовании фазы 1-2 “basket” (VE-BASKET) с участием 14 взрослых с BRAF V600E–положительным LCH или болезнью Эрдгейма–Честера, которое можно было оценить, лечение вемурафенибом привело к 41%-ному ответу в соответствии с Критериями оценки ответа при солидных опухолях (RECIST) (78).
Напротив, ретроспективное исследование вемурафениба у 12 взрослых с болезнью Эрдгейма–Честера показало, что частота метаболического ответа (т. е. доля пациентов с положительным поглощением на позитронно-эмиссионной томографии [ПЭТ] до лечения и отрицательным поглощением во время лечения) составила 100% (79).
Разница в этих результатах исследования, вероятно, отражает влияние ингибирования BRAF V600E на метаболическую активность по сравнению с влиянием на цитотоксичность (таблица S3 в приложении). В последующем отчете по результатам исследования VE-BASKET все пациенты с LCH или болезнью Эрдгейма-Честера, которые могли быть оценены, имели метаболический ответ (80). Как метаболический ответ приводит к улучшению выживаемости, пока не определено.
Ограниченное число отчетов о случаях заболевания у детей также свидетельствует о возможности клинического ответа у детей с рефрактерным LCH (таблица 4 в Дополнительном приложении). Аналогичным образом, ранние отчеты о случаях заболевания и серии исследований подтверждают потенциальную пользу ингибирования МЕК (таблицы S3 и S4 в приложении) (44, 54, 81).
Потенциал МAPK-таргетной терапии LCH неизвестен. В отдаленном исходе после прерывания терапии ингибиторами Вемурафениба/BRAF в исследовании Erdheim-Chester Disease (LOVE) рецидив произошел у 75% пациентов (взрослых с болезнью Эрдгейма–Честера) после прекращения терапии ингибиторами BRAF V600E (81).
Хотя BRAF V600E–позитивные клетки периферической крови и циркулирующая внеклеточная ДНК BRAF V600E у пациентов с заболеваниями высокого риска обычно не обнаруживаются при полном ответе на терапию, эти биомаркеры могут оставаться обнаруживаемыми у пациентов, получавших ингибитор BRAF V600E, несмотря на клинические реакции (19, 33, 82, 83).
Это наблюдение предполагает, что таргетная терапия ингибиторами MAPK может подавлять, а не ликвидировать мутировавшие клетки-предшественницы LCH. Перспективное исследование клеток периферической крови в клинических испытаниях будет полезно для определения клинической значимости выявления минимальной активности заболевания для лечения LCH.
Неопределенный профиль токсичности препаратов, все еще находящихся на ранней стадии оценки у детей, является еще одним фактором, который ставит под сомнение внедрение лечения ингибиторами MAPK при детском LCH.
В исследованиях с участием взрослых с LCH или болезнью Эрдгейма–Честера токсические эффекты ингибиторов MAPK соответствовали тем, которые наблюдались в других исследованиях рака.
При применении ингибиторов BRAF-V600E сообщалось о сыпи, артралгиях, пирексии, тошноте, рвоте, диарее, усталости и возможности развития других опухолей (чаще всего плоскоклеточного рака кожи), а при применении ингибиторов MEK – о сыпи, офтальмологическом воспалительном процессе, лекарственной реакции с эозинофилией и системными симптомами (DRESS), рабдомиолизе и пневмоните (78, 81, 84, 85).
После того как безопасность и эффективность монотерапии ингибиторами MAPK у детей будут установлены, эти исследования могут заложить основу для изучения безопасности и эффективности комбинаций таргетных препаратов или химиотерапии в сочетании с ингибиторами MAPK.
МОЛЕКУЛЯРНАЯ СТРАТИФИКАЦИЯ РИСКА
Взаимоисключающие мутации MAPK-пути и активированный (фосфорилированный) ERK были идентифицированы почти во всех поражениях при LCH (40, 43, 49, 51).
Существуют ли предсказуемые клинические различия в случаях LCH, обусловленных различными мутациями MAPK? Хотя MAPK обычно рассматривается как линейный путь (по крайней мере, ниже уровня RAF), вполне возможно, что специфические мутации имеют уникальные последствия. Анализ in vitro CD207+ клеток в первичных очагах LCH показывает мутационно-специфическое влияние на активацию ERK (49).
Два исследования показали, что пациенты с мутацией BRAF V600E имели повышенный риск неудачного проведения лечения препапарами первой линии нейродегенеративного LCH, хотя результаты варьировали в зависимости от связи между статусом мутации BRAF и степенью тяжести заболевания на момент исследования (33, 87).
Проспективные исследования, включая оценку генотипа LCH-клеток, вероятно, будут необходимы для окончательного определения относительного риска различных драйверных мутаций на клинические исходы при LCH.
Различия между этническими группами США в риске приобретения LCH предполагают, что наследственные факторы риска могут играть определенную роль в восприимчивости LCH и реакции на терапию (61).
Кроме того, исследование геномной ассоциации выявило вариант SMAD6, кодирующий ингибитор SMAD для передачи сигналов костным морфогенетическим белком, трансформирующим фактором роста β (TGF-β) или и тем, и другим, который связан с повышенным риском развития LCH и с большей вероятностью присутствует в латиноамериканских популяциях, чем в других этнических группах (88).
Играет ли сигнальный путь SMAD6 или TGF-β роль в патогенезе LCH, неизвестно, но эти данные, наряду с предрасположенностью к LCH, указывают на патогенетические механизмы, выходящие за рамки соматических мутаций в генах MAPK.
ДОПОЛНИТЕЛЬНЫЕ ЦЕЛИ ЛЕЧЕНИЯ
Современные методы лечения LCH остаются неоптимальными. Лечение первой линии винбластином и преднизоном даёт плохие результаты, и, хотя терапия с помощью высокодозных аналогов нуклеозидов может быть эффективной, она также очень токсична.
Ранние сообщения и испытания ингибиторов BRAF и MEK многообещающи, хотя побочные эффекты не являются тривиальными, а потенциал лечения неопределенен. По мере изучения патогенетических механизмов, лежащих за пределами активации ERK, могут быть выявлены дополнительные терапевтические возможности. Сигнальный путь MAPK играет решающую роль в клеточных функциях, включая клеточную дифференцировку, пролиферацию и жизнедеятельность специфическим для клетки образом (47, 89). Хотя ранние исследования выявили признаки митозов в некоторых очагах LCH и сообщили о высоких уровнях экспрессии Ki67 (маркера клеточной пролиферации) (90), более поздние исследования показали, что нормальные эпидермальные клетки Лангерганса и CD207+ клетки в очагах LCH имеют сходные скорости пролиферации (36, 41, 91). BRAF V600E–позитивные клетки обычно составляют менее 1% от общего количества PBMCs и аспиратов костного мозга у пациентов с высоким риском, что говорит о том, что предшествующая гиперпролиферация также маловероятна.
В отсутствие усиленной пролиферации вполне вероятно, что накопление и персистенция патологических дендритных клеток составляют механизм формирования поражения. BRAF V600E в поражениях CD207+ LCH сильно ингибирует экспрессию CCR7 (91), который кодирует хемокиновый рецептор, необходимый для миграции дендритных клеток (92).
Кроме того, BRAF V600E стимулирует экспрессию BCL2L1, что приводит к резистентности к апоптозу (91).
Таким образом, патологическая активация сигнального пути MAPK приводит к подавлению миграции и повышению выживаемости дендритных клеток, причем CD207+-клетки сохраняются в очагах LCH и устойчивы к гибели (рис. 3С).
Терапевтические стратегии, нацеленные на миграцию и выживание дендритных клеток, могут представлять собой многообещающие новые подходы.
Процент CD207+ клеток в очагах LCH сильно варьирует, но обычно представляет собой меньшинство пораженных клеток, с медианой 8% в одном исследовании (33).
В нормальных условиях дендритные клетки взаимодействуют с Т-клетками, стимулируя антигенспецифические реакции. Функциональные взаимодействия между CD207+ клетками и опухолево-инфильтрирующими Т-клетками при поражении LCH неясны, хотя CD207+ клетки экспрессируют высокие уровни лиганда программируемой смерти 1 (PD-L1), инфильтрирующие Т-клетки экспрессируют высокие уровни белка коингибиторного рецептора программируемой смерти 1 (PD-1), а инфильтрирующие лимфоциты обогащены активированными CD4+ регуляторными супрессорными Т-клетками (36, 41).
По мере выяснения механизмов, приводящих к рекрутированию и активации Т-клеток, терапия, направленная на факторы местного и системного воспаления, может принести некоторую клиническую пользу. Раннее исследование талидомида и серия случаев, в которых пациенты получали лечение индометацином, предполагают возможность клинического ответа на противовоспалительные средства (94, 95).
Нарушение иммунного микроокружения может также объяснить потенциал местной инъекции глюкокортикоидов или даже простого кюретажа для лечения изолированных поражений костей при LCH (96).
КЛАССИФИКАЦИЯ
Является ли ЛЧ раком? Ответ несет в себе важный смысл. Двадцать лет назад Арчечи и его коллеги предположили, что неопределенность в отношении того, является ли LCH раком или иммунным расстройством, привела к “противоречивому” иммунохимиотерапевтическому подходу к лечению LCH (8).
Первая линия терапии винбластином и преднизоном остается стандартом лечения, обеспечивая улучшенную общую выживаемость, но все еще с высокими показателями рефрактерности лечения (4).
Мы полагаем, что наличие активирующих соматических мутаций MAPK в устойчивых миелоидных клетках-предшественницах дает основание для определения LCH как миелоидного неопластического расстройства (33, 57).
Общество гистиоцитов также поддерживает реклассификацию гистиоцитарных нарушений на основе мутаций клеток кроветворной линии (97).
Такое переосмысление LCH открывает возможности для дополнительных клинических исследований, проводимых совместными исследовательскими организациями в области детской онкологии в дополнение к продолжающимся усилиям Общества гистиоцитов.
ВЫВОДЫ
Биологические перспективы LCH эволюционировали от известных случаев, описывающих спектр паттернов заболевания, до гистологически унифицированного диагноза (гистиоцитоз Х) и общих цитоплазматических структур с эпидермальными клетками Лангерганса (Лангерганс-клеточный гистиоцитоз).
Клинические достижения исторически сдерживались неопределенными механизмами патогенеза. Ускоренный прогресс в последнее десятилетие определил LCH как расстройство, обусловленное ошибочной миелоидной дифференцировкой, причем степень заболевания определяется клеткой-предшественницей, в которой возникают активирующие соматические мутации MAPK.
Задача, с которой мы сейчас сталкиваемся, состоит в том, чтобы перевести биологические открытия в улучшенные результаты лечения для детей и взрослых с LCH.