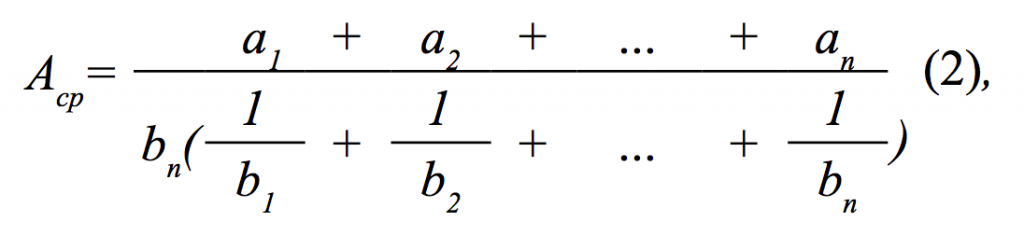в какую группу патогенности входит вирус sars cov 2
В какую группу патогенности входит вирус sars cov 2
Исследование предназначено для количественного определения антигена нуклеокапсидного белка (N) вируса SARS-CoV-2 в образце биоматериала. Тест является эффективной альтернативой ПЦР-тестированию и предназначен для диагностики COVID-19 у людей любого возраста без признаков ОРВИ. Анализ позволяет выявить специфический вирусный белок – нуклеокапсидный антиген SARS‑CoV‑2 в мазке биоматериала. Актуален для тех, кто беспокоится о своем здоровье и хочет быстро узнать свой COVID‑статус. Выполняется на полностью автоматизированном высокотехнологичном оборудовании и имеет очень высокую чувствительность и специфичность.
Результат теста выдается в количественном формате, позволяющем дополнительно к COVID-статусу определить вирусную нагрузку.
Антиген N вируса SARS-CoV-2, быстрый тест на ковид, антигенная детекция вируса SARS-CoV-2, определение антигена N вируса SARS-CoV-2, диагностика коронавирусной инфекции (COVID-19).
Синонимы английские
SARS-CoV-2 Antigen, SARS-CoV-2 Ag, Ag-RDTs (diagnostics tests) for COVID-19.
Иммунохемилюминесцентный анализ (ИХЛА).
Какой биоматериал можно использовать для исследования?
Мазок из ротоглотки и носоглотки.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Коронавирусная инфекция (COVID-19) — это острая респираторная инфекция, вызываемая РНК-содержащим вирусом SARS-Cov-2.
Коронавирус SARS-CoV-2 попадает в организм человека через клетки-мишени, имеющие на своей поверхности рецепторы ангиотензинпревращающего фермента II типа (ACE2). Такие рецепторы располагаются на клетках эпителия дыхательного тракта, почек, пищевода, мочевого пузыря, подвздошной кишки, сердца, ЦНС. Однако основной и быстродостижимой мишенью являются альвеолярные клетки II типа (AT2) легких, что определяет развитие пневмоний.
Большинство людей с COVID-19 переносят заболевание в легкой и неосложненной форме, однако примерно у 14 % зараженных развивается тяжелая форма болезни, требующая госпитализации и кислородной поддержки. Около 5 % пациентов нуждается в лечении в условиях палаты интенсивной терапии. При тяжелом течении заболевание может быть осложнено острым респираторным дистресс-синдромом, сепсисом, полиорганной недостаточностью (острое поражение почек и сердца). Распространение SARS-CoV-2 из системного кровотока или через пластинку решетчатой кости может привести к поражению головного мозга. Изменение обоняния (гипосмия) на ранней стадии заболевания может свидетельствовать о поражении ЦНС. Пожилые пациенты и пациенты с сопутствующими состояниями (сердечно-сосудистые заболевания, сахарный диабет и др.) имеют повышенный риск развития тяжелой формы COVID-19 и летального исхода. Молодые люди и дети часто могут переносить инфекцию бессимптомно, что способствует распространению COVID-19 среди населения.
К основным симптомам COVID-19 относятся:
Реже заболевание проявляется диареей, тошнотой и рвотой.
Лабораторная диагностика коронавирусной инфекции проводится с использованием молекулярно-генетических и серологических методов, которые позволяют выявить генетический материал вируса, специфические антитела к SARS-CoV-2 и антигенные структуры вируса. Согласно рекомендациям ВОЗ и управлению по санитарному надзору за качеством пищевых продуктов и медикаментов (Food and Drug Administration, США), количественное определение антигена нуклеокапсидного белка (N) вируса SARS-CoV-2 методом иммунохемилюминесцентного анализа является высокоэффективным тестом для диагностики коронавирусной инфекции. Показатели диагностической чувствительности и специфичности данного метода не уступают таковым при проведении ПЦР-анализа на РНК вируса SARS-CoV-2. Антигенная детекция вируса SARS-CoV-2 позволяет в сжатые сроки подтвердить/исключить наличие коронавирусной инфекции.
Тест на антиген может определить наличие COVID-19, если вирусная нагрузка высокая, т.е. в носоглотке находятся сотни тысяч и миллионы копий вируса, что чаще бывает в самом начале заболевания или в период пика коронавирусной болезни. При средней или низкой вирусной нагрузке результат теста может быть ложноотрицательным.
Положительный результат теста на антиген, если имеются симптомы заболевания, свидетельствует о том, что человек болен COVID-19. Однако если результат положительный, а симптомов нет, необходимо в течение ближайших двух дней выполнить ПЦР-анализ для подтверждения результатов.
Отрицательный результат теста на антиген не исключает инфицирования COVID-19:
Тест на антиген не рекомендуется лицам с подозрением на COVID-19 без клинических проявлений, у которых количество вируса в носоглотке может быть небольшим и тест не сможет его выявить.
Отрицательный результат теста на антиген не является свидетельством о выздоровлении от коронавирусной инфекции, документом для снятия самоизоляции в случае прибытия из стран «красной зоны». В этих случаях требуется результат ПЦР.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Причины положительного результата:
Причины отрицательного результата:
Кто назначает исследование?
Инфекционист, педиатр, врач общей практики, анестезиолог-реаниматолог.
Что вы должны знать
Общая информация
В конце 2019 года в Китайской Народной Республике (КНР) произошла вспышка новой коронавирусной инфекции с эпицентром в городе Ухань (провинция Хубэй), возбудителю которой было дано временное название 2019-nCoV.
Всемирная организация здравоохранения (ВОЗ) 11 февраля 2020 г. присвоила официальное название инфекции, вызванной новым коронавирусом, – COVID-19 («Coronavirus disease 2019»). Международный комитет по таксономии вирусов 11 февраля 2020 г. присвоил официальное название возбудителю инфекции – SARS-CoV-2.
Появление COVID-19 поставило перед специалистами здравоохранения задачи, связанные с быстрой диагностикой и оказанием медицинской помощи больным. В настоящее время сведения об эпидемиологии, клинических особенностях, профилактике и лечении этого заболевания ограничены. Известно, что наиболее распространенным клиническим проявлением нового варианта коронавирусной инфекции является двусторонняя пневмония, у 3-4% пациентов зарегистрировано развитие острого респираторного дистресс-синдрома (ОРДС).
Патогенез
Новый коронавирус SARS-CoV-2 представляет собой одноцепочечный РНК-содержащий вирус, относится к семейству Coronaviridae, относится к линии Beta-CoV B. Вирус отнесен ко II группе патогенности, как и некоторые другие представители этого семейства (вирус SARS-CoV, MERS-CoV).
Коронавирус SARS-CoV-2 предположительно является рекомбинантным вирусом между коронавирусом летучих мышей и неизвестным по происхождению коронавирусом. Генетическая последовательность SARSCoV-2 сходна с последовательностью SARS-CoV по меньшей мере на 79%.
Входные ворота возбудителя – эпителий верхних дыхательных путей и эпителиоциты желудка и кишечника. Начальным этапом заражения является проникновение SARS-CoV-2 в клетки-мишени, имеющие рецепторы ангиотензинпревращающего фермента II типа (ACE2). Рецепторы ACE2 представлены на клетках дыхательного тракта, почек, пищевода, мочевого пузыря, подвздошной кишки, сердца, ЦНС. Однако основной и быстро достижимой мишенью являются альвеолярные клетки II типа (AT2) легких, что определяет развитие пневмонии. Также обсуждается роль CD147 в инвазии клеток SARS-CoV-2.
Установлено, что диссеминация SARS-CoV-2 из системного кровотока или через пластинку решетчатой кости (Lamina cribrosa) может привести к поражению головного мозга. Изменение обоняния (гипосмия) у больного на ранней стадии заболевания может свидетельствовать о поражении ЦНС, так и об отеке слизистой оболочки носоглотки.
Многие аспекты патогенеза коронавирусной инфекции нуждаются в дальнейшем комплексном изучении.
Эпидемиологическая характеристика
С декабря 2019 г. по март 2020 г. наиболее широкое распространение SARS-CoV-2 получил на территории КНР, в которой подтвержденные случаи заболевания были зарегистрированы во всех административных образованиях. Наибольшее количество заболевших выявлено в Юго-Восточной части КНР с эпицентром в провинции Хубэй (84% от общего числа случаев в КНР).
С конца января 2020 г. во многих странах мира стали регистрироваться случаи заболевания COVID-19, преимущественно связанные с поездками в КНР. В конце февраля 2020 г. резко осложнилась эпидемиологическая обстановка по COVID-19 в Южной Корее, Иране и Италии, что в последующем привело к значительному росту числа случаев заболевания в других странах мира, связанных с поездками в эти страны. ВОЗ объявила 11 марта 2020 г. о начале пандемии COVID-19.
Основным источником инфекции является больной человек, в том числе находящийся в инкубационном периоде заболевания.
Передача инфекции осуществляется воздушно-капельным, воздушно-пылевым и контактным путями. Ведущим путем передачи SARS-CoV-2 является воздушно-капельный, который реализуется при кашле, чихании и разговоре на близком (менее 2 метров) расстоянии. Контактный путь передачи осуществляется во время рукопожатий и других видах непосредственного контакта с инфицированным человеком, а также через пищевые продукты, поверхности и предметы, контаминированные вирусом. Известно, что при комнатной температуре SARS-CoV-2 способен сохранять жизнеспособность на различных объектах окружающей среды в течение 3 суток.
По имеющимся научным данным возможен фекально-оральный механизм передачи вируса. РНК SARS-CoV-2 обнаруживалась при исследовании образцов фекалий больных. Нуклеокапсидный белок COVID-19 был обнаружен в цитоплазме эпителиальных клеток слюнных желез, желудка, двенадцатиперстной кишки и прямой кишки, мочевыводящих путей Установлена роль COVID-19 как инфекции, связанной с оказанием медицинской помощи.
SARS-CoV-2 включен в перечень заболеваний, представляющих опасность для окружающих (постановление Правительства Российской Федерации от 31 января 2020 г. № 66).
Стандартное определение случая заболевания COVID-19
Подозрительный на COVID-19 случай
Клинические проявления острой респираторной инфекции (температура тела выше 37,5 °C и один или более из следующих признаков: кашель – сухой или со скудной мокротой, одышка, ощущение заложенности в грудной клетке, насыщение крови кислородом по данным пульсоксиметрии (SpO2) ≤ 95%, боль в горле, насморк и другие катаральные симптомы, слабость, головная боль, аносмия, диарея) при отсутствии других известных причин, которые объясняют клиническую картину вне зависимости от эпидемиологического анамнеза.
Вероятный (клинически подтвержденный) случай COVID-19
1. Клинические проявления острой респираторной инфекции (температура тела выше 37,5 °C и один или более признаков: кашель, сухой или со скудной мокротой, одышка, ощущение заложенности в грудной клетке, насыщение крови кислородом по данным пульсоксиметрии (SpO2) ≤ 95%, боль в горле, насморк и другие катаральные симптомы, слабость, головная боль, аносмия, диарея) при наличии хотя бы одного из эпидемиологических признаков:
· возвращение из зарубежной поездки за 14 дней до появления симптомов;
· наличие тесных контактов за последние 14 дней с лицом, находящимся под наблюдением по COVID-19, который в последующем заболел;
· наличие тесных контактов за последние 14 дней с лицом, у которого лабораторно подтвержден диагноз COVID-19;
· работа с лицами, у которых выявлен подозрительный или подтвержденный случай заболевания COVID-19.
2. Наличие клинических проявлений, указанных в п.1, в сочетании с характерными изменениями в легких по данным компьютерной томографии или обзорной рентгенографии органов грудной клетки (см. Приложение 1 настоящих рекомендаций) вне зависимости от результатов однократного лабораторного исследования на наличие РНК SARS-CoV-2 и эпидемиологического анамнеза.
3. Наличие клинических проявлений (указаны в п.1), в сочетании с характерными изменениями в легких по данным лучевых исследований (указаны в п.2) при невозможности проведения лабораторного исследования на наличие РНК SARS-CoV-2.
Подтвержденный случай COVID-19
Положительный результат лабораторного исследования на наличие РНК SARS-CoV-2 с применением методов амплификации нуклеиновых кислот вне зависимости от клинических проявлений.
Другие случаи, требующие обследования на COVID-19
При обращении в медицинские учреждения пациентов без признаков поражения дыхательной системы при наличии следующих данных эпидемиологического анамнеза:
• возвращение из зарубежной поездки за 14 дней до обращения;
• наличие тесных контактов за последние 14 дней с лицами, находящимися под наблюдением по инфекции, вызванной новым коронавирусом SARS-CoV-2, которые в последующем заболели;
• наличие тесных контактов за последние 14 дней с лицами, у которых лабораторно подтвержден диагноз COVID-19;
• работа с лицами, у которых выявлен подозрительный или подтвержденный случай заболевания COVID-19.
Для обеспечения достоверного статистического учета при наличии у пациента коронавирусной инфекции, или подозрения на нее, заключительный клинический диагноз должен быть сформулирован в соответствии с правилами МКБ-10.
В статистике заболеваемости в конце эпизода оказания медицинской помощи из нескольких имеющихся у пациента заболеваний должно быть выбрано только одно заболевание в качестве основного, на долю которого пришлась наибольшая часть использованных ресурсов.
Источник: Временные методические рекомендациипо профилактике, диагностике и лечению новой коронавирусной инфекции (COVID-19). Версия 6 от 28.04.2020 (Минздрав РФ)
Кратко о коронавирусе SARS-COV-2 и его мутациях
В последнее время в некоторых странах мира зафиксированы случаи повторного заражения (реинфекции) возбудителем новой коронавирусной инфекции под названием COVID-19.
Также установлено, что если человек заболевает снова, то это, скорее всего, связано со встречей с другим вариантом той же инфекции. Кроме того, известно, что в этом случае заболевание может протекать в тяжелой форме.
ЧТО ТАКОЕ ШТАММ КОРОНАВИРУСА SARS-COV-2?
Геном SARS-CoV-2 представляет собой длинную последовательность РНК, состоящую почти из 30 000 символов (нуклеотидов), которые работают в строгой последовательности. Этот порядок может измениться: если каждая новая копия вируса собрана в одном из этих соединений, может произойти ошибка — замена одного нуклеотида другим — и в результате код всей цепи немного изменится. В каждом новом» хозяине» геном вируса изменяется незначительно.
Эти изменения могут быть очень незначительными, но они позволяют установить связь между инфицированными людьми или следовать по пути, который выбрал вирус. Под словом «племя» ученые подразумевают генетически иную ветвь вируса, которая отличается от своего «отца» одной или несколькими мутациями. Разница может составлять лишь долю процента от общего генома, но каждая новая последовательность РНК может вызвать новую ветвь вируса, то есть новый штамм.
Скорость, с которой происходят генетические изменения, варьируется от вируса к вирусу, и SARS-CoV-2 мутирует относительно медленно. Большинство геномов этого вируса отличаются друг от друга небольшим количеством точечных заменителей, а число отличий от исходного варианта не превышает 30-почти 30 тысяч нуклеотидов.
КАКИЕ ШТАММЫ КОРОНАВИРУСА СУЩЕСТВУЮТ?
Основных штаммов нового коронавируса семь, они начинались с букв GR, G, GH, O, S, L и V. С индексом L — вирус был обнаружен в декабре 2019 года в Ухане, Китай. Но теперь он постепенно исчезает.
Остальные штаммы неравномерно распределены по всему миру: на каждом континенте, как правило, наиболее распространены не более двух основных вариаций.
ЧТО НУЖНО ЗНАТЬ О СТРУКТУРЕ И ДЕЙСТВИИ КОРОНАВИРУСА SARS-COV-2?
Последний импортируется не из Китая, а из других азиатских стран. Эти два штамма были обнаружены в 99% образцов, протестированных в России. На рисунке схематически показано, как проявляет себя коронавирус в отношении человека.
КАК РАЗВИВАЛСЯ КОРОНАВИРУС SARS-COV-2 В РОССИИ?
Общее число мутаций, обнаруженных в секвенированных геномах вируса SARS-CoV-2, составляет многие тысячи, но лишь немногие из них были зарегистрированы и стабильно наследуются.
Сейчас таких единичных мутаций насчитывается около 22, они произошли в январе-марте этого года. Позднее новые племена перестали широко распространяться, т. е. до начала эпидемии в России в геноме вируса стабильно регистрировались три основные группы мутаций, которые, согласно исследованию Роспотребнадзора, формировали «три ветви эволюционного развития».
К концу марта 2020 года развитие этих трех основных направлений и циркулирующих штаммов с мутациями в генах orf1b (P314L) и S (D614G) замедлилось. Эти две мутации были основными долгосрочными изменениями в геноме вируса SARS-CoV-2, подчеркивается в исследовании.
Роспотребнадзор считает, что мутация в гене S связана со снижением патогенности (способности вызывать заболевания, попадающие в организм). Агентство отмечает, что это также связано с улучшением лечения пациентов во время пандемии. Влияние мутации в гене orf1b (P314L) до сих пор плохо изучено.
Вирусы постоянно мутируют, но коронавирусы мутируют гораздо медленнее, чем другие РНК-вирусы. Несмотря на активную циркуляцию по всему миру, SARS-CoV-2 изменился менее чем на 0,1% по сравнению с вирусом, первоначально выделенным в Китае 11 месяцев назад.
Основные изменения были выявлены в первые месяцы размножения, и распространенные в настоящее время варианты вируса аналогичны тем, которые были выделены весной. Штамм S (D614G) в настоящее время является предметом пристального внимания ученых.
Впервые он был обнаружен в Индонезии в августе 2020 года; в то время сообщалось, что этот штамм был в 10 раз более заразным, чем исходный штамм вируса. Некоторые исследования, проведенные в Forerunner (т. е. не рецензируемые и не опубликованные в научных публикациях), заключают, что эта мутация действительно может иметь более высокую инфекционную способность и более высокую вирусную нагрузку при заражении этой разновидностью. Но окончательных решений нет. Вирус быстро замещает S (Спайк) вирион в поверхностном белке, что повышает переносимость (свойство инфекционных заболеваний, венерических организмов — здоровых), но не клиническое течение заболевания, так как другие различия в штаммах вируса минимальны.
Первые варианты вируса двух мутаций, распространенные в России, были обнаружены в конце января 2020 года в Китае, а затем и в Австралии. В феврале 2020 года эти варианты были обнаружены в большинстве западноевропейских стран, Саудовской Аравии, США, Канаде, Мексике, Бразилии, Марокко и Сенегале. Детальное сравнение геномов вирусов в России и за рубежом показывает, что в стране циркулируют штаммы, завезенные из Западной Европы. Они были отправлены в марте и апреле 2020 года.
Коронавирус очень мало мутировал за эти девять месяцев и не изменился в местах, ответственных за проявления эпидемического процесса, за его, скажем так, агрессивность и ожесточенность. Минздрав России считает, что вирус обладает низкой способностью к мутациям — он накапливает всего около двух точечных изменений в месяц, то есть за год может произойти около 24 мутаций. Распространение основных вариантов вируса, циркулирующих в России, в целом аналогично распространению в Европе.
Есть некоторые различия, но у нас нет оснований полагать, что эти различия каким-то образом изменяют клиническое течение или эпидемиологию COVID-19 в России по сравнению с европейскими странами. Роспотребнадзор сообщил, что ежемесячно ученые ФБУН ГНЦ совместно с РИЦ «Вектор» полностью расшифровывают более 150 геномов нового коронавируса. Полученные ими данные будут использованы для анализа актуальности используемых диагностических тест-систем, выявления завозных случаев заболевания и оценки региональных особенностей генетического разнообразия SARS-CoV-2.
Сейчас геномы вирусов секвенируются и собирают данные в различных лабораториях по всему миру, в том числе в российском центре имени Чумакова. Ученые, по ее словам, будут коррелировать геномы вирусов с клинической картиной пациентов, от которых они изолированы, что прольет свет на важность наиболее распространенных мутаций. Она признает, что изучение влияния каждой конкретной мутации на клиническую картину КОВИДА-19 сложно.
Ученые должны изучить важность каждой конкретной мутации для структуры мутировавших белков и определить роль этих мутаций в развитии клинических симптомов и повреждении легких в экспериментах на животных. В настоящее время разрабатываются, анонсируются и регистрируются всё новые вакцины против SARS-CoV-2.
ДОЛЖНЫ ЛИ МЫ БОЯТЬСЯ МУТАЦИЙ?
Важен также вопрос о различном воздействии инфицированных, например, могут ли некоторые штаммы быть более заразными, чем другие. Из заявлений Роспотребнадзора следует, что мутации вируса не так уж плохи. Однако в научной литературе уже сообщалось о нескольких случаях повторной коронавирусной инфекции. Для повторного выявления инфекции ученые каждый раз проверяют генетический состав возбудителя и убеждаются, что штамм вируса отличается от первого, чем вызывает заболевания, — иначе нельзя с уверенностью сказать, что это вторичная инфекция, а не длительный первичный случай. Голландское информационное агентство BNO подсчитывает все повторяющиеся заболевания, когда-либо записанные, и сопровождает их ссылкой на источник.
По данным агентства, во всем мире известно 24 случая повторных инфекций, один из которых был смертельным. 89-летний пациент из Нидерландов скончался от рака. Повторные случаи заражения также произошли в Гонконге, Бельгии, США и Эквадоре. Каждый день в России почти 20 тысяч случаев, некоторые из которых связаны с вирусами, издавна циркулирующими в стране, частично с импортными вариантами, связанными с инфекциями в других странах, часто очень далекими.
Поэтому, конечно, можно импортировать, а затем изолировать вариант вируса, который ранее не был обнаружен в России, как это было недавно в Норвегии. Однако это не означает немедленного изменения эпидемиологической ситуации с Ковид-19.
В октябре 2020 года The Lancet опубликовала исследование, в котором были описаны два случая повторной коронавирусной инфекции. У пациента из американского штата Невада болезнь была более тяжелой после очередной инфекции. 25- летний мужчина должен был попасть в больницу из-за недостатка кислорода, и компьютерная томография показала, что у него вирусная пневмония.
Ученые обнаружили, что он был заражен другим штаммом, генетически отличным от предыдущего возбудителя. Таким образом, более раннее воздействие SARS-CoV-2 не может гарантировать полный иммунитет. Все люди, независимо от того, был ли ранее диагностирован коронавирус или нет, должны принимать те же меры предосторожности.
БУДУТ ЛИ ВАКЦИНЫ ЭФФЕКТИВНЫМИ, ЕСЛИ ВИРУС МУТИРУЕТ?
До сих пор ученые считают, что вакцины, разработанные во всем мире для борьбы с первыми штаммами нового коронавирус, будут столь же эффективны против новых мутаций. Ученые пояснили, что большинство вакцин, разработанных во всем мире, были смоделированы оригинальным штаммом d-вируса, который чаще встречается в последовательностях, опубликованных в начале пандемии.
С тех пор вирус мутировал в штамм G, вариации которого в настоящее время доминируют в мире. Исследователи были обеспокоены тем, что эта мутация негативно повлияет на эффективность разработанных вакцин. Несмотря на мутацию d614g в белке, эксперименты и моделирование подтвердили, что вакцины остаются эффективными.
Наиболее распространенный штамм G, вероятно, не требует частого выбора новых вакцин, в отличие от гриппа, который требует разработки вакцин против циркулирующих штаммов каждый год. Поскольку различия в штаммах, циркулирующих в России, минимальные, они, вероятно, существенно не влияют на структуру вирусных белков.
Таким образом, созданные и применяемые вакцины от COVID-19, не нужно воспроизводить каждый год.
Составили: канд. мед. наук, доцент Гуменюк С.А., врач-оториноларинголог Байчорова О.Х. , 2021 год
Вирулицидная активность импульсного ультрафиолетового излучения сплошного спектра в отношении коронавируса SARS-CoV‑2 А.
В связи с пандемией Covid-2019 государственные медицинские и противоэпидемические службы России и большинства стран мира предпринимают беспрецедентные меры по профилактике и ликвидации данной угрозы. [1,2,3].
Основными путями передачи нового коронавируса SARS–CoV-2 являются воздушно-капельный (кашель и чихание) и контактный (через прикосновения). Коронавирус сохраняется в воздухе виде аэрозоля на протяжении 8—10 часов, на бумаге 3 часа, на банкнотах 4 дня, на дереве и одежде 2 дня, на стекле 4 дня, на металле и пластике 7 дней. [4]. Поэтому обязательному обеззараживанию должны подвергаться не только воздух, но и поверхности объектов в помещении [5,6].
Наименее трудоёмкими и универсальными методами, позволяющими одновременно обеззараживать воздух и поверхности помещении, являются аэрозольная обработка химическими дезинфектантами и облучение бактерицидным ультрафиолетовым излучением. Широкое использование аэрозольной дезинфекции ограничивается высокой токсичностью применяемых химических дезинфектантов и длительным временем (до 3-4 часов) воздействия, основная часть которого затрачивается на их нейтрализацию для безопасной эксплуатации помещений.
При разработке конкретной бактерицидной установки на основе ультрафиолетовой технологии требуется знание ее энергетических доз, которые необходимы для доказательства ее эффективности в отношении определённого микроорганизма или вируса [7].
В дальнейшем они необходимы для разработки оптимальных режимов обеззараживания их в воздухе и/или на открытых поверхностях. Режимы, сочетающие высокую степень инактивации конкретных микроорганизмов и вирусов (99,99 – 100%) за минимальное время обработки, смогут обеспечить высокую надёжность дезинфекционных мероприятий.
В России и за рубежом в клиническую практику активно внедряется в качестве наиболее эффективного, оперативного и наименее трудоёмкого метода ультрафиолетовая технология, использующая высокоинтенсивное ультрафиолетовое излучение сплошного спектра. Созданные на ее основе импульсные установки с ксеноновыми лампами, предназначенные для обеззараживания воздуха и открытых поверхностей помещений, демонстрируют высокую эффективность в отношении самых устойчивых микроорганизмов (MRSA,VRE, C.difficile, МЛУ-, ШЛУ-ТБ) и вирусов (полиомиелита, гриппа А, гепатита С, аденовируса) за минимальный промежуток времени (от 1 мин.) [8,9,10].
Исследования возможности высокоэффективного обеззараживания поверхностей, контаминированных коронавирусом SARS–СoV-2 с помощью ультрафиолетового излучения сплошного спектра и определение бактерицидных доз для получения требуемого эффекта является актуальной задачей, позволяющей грамотно разработать методы и регламенты обеззараживания помещений импульсными бактерицидными установками.
Материалы и методы
Экспериментальные исследования проводились на базе ФГБУ «48 Центральный научно-исследовательский институт» Минобороны России.
Исследования проводились с учетом основных требований Санитарно-эпидемиологических правил СП 1.3.3118-13 «Безопасность работы с микроорганизмами I-II групп патогенности (опасности)», Руководства Р 3.5.1904-04 «Использование ультрафиолетового бактерицидного излучения для обеззараживания воздуха в помещениях», Методическими указаниями МУ 3.5.2431-08 «Изучение и оценка вирулицидной активности дезинфицирующих средств», 2010., а также по общепринятым методикам, разработанным в ЦНИИ» Минобороны России.
Оборудование
Тест-объекты
Тест-вирус
В исследованиях использовалась живая культура вируса SARS-CoV-2 (изолят В от 16.03.2020 г) с исходной биологической активностью 5,8∙106 БОЕ∙мл-1.
Определение биологической концентрации коронавируса (биологической активности, уровней контаминации) проводили на флаконах с монослоем суточного возраста клеток Vero С1008 (площадью 25 см2) методом негативных колоний под агаровым покрытием. Биологическую активность рассчитывали по формуле 1:
где: а1-аn – среднее число негативных колоний с 1-го по n-е разведение исследуемого материала; b1-bn – степень разведения исследуемого материала.
Уровни контаминации поверхности тест-объектов, соответственно инициальную и вторичную контаминации, рассчитывали по формуле (3):
где: АS – уровень контаминации, (БОЕ∙см-2); V – объем сорбирующей жидкости, используемой для смыва биологического материала с поверхности, (мл); S – площадь контаминации тест-объекта, (см2).
Статистическую обработку полученных данных проводили на основании вычисления среднего квадратичного отклонения по результатам пяти экспериментов.
Персонал, проводящий исследования с микроорганизмами I-II групп патогенности, был обеспечен рабочей и защитной одеждой, средствами индивидуальной защиты и средствами личной гигиены по регламентированным нормам. Испытания осуществлялись в «заразной» зоне по условиям максимально изолированной лаборатории.
Порядок проведения испытаний
Испытания проводили в рабочем помещении «заразной» зоны при температуре воздуха (24±1)оС и относительной влажности (42±3) %.
Установки располагались следующим порядком:
Испытания установок проводились в штатных режимах работы: «Бактерицидный», «Спороцидный», «Туберкулоцидный и фунгицидный», предназначенных для обеззараживания поверхностей (Таблица 1).
Первоначально готовили монослой суточного возраста культуры клеток Vero во флаконах. Для этого из флаконов с монослоем клеток, отобранных для опыта, после термостатирования сливали ростовую среду и маркировали их. На тест-объекты наносили по 0,1 мл исходной культуры вируса с биологической активностью 1,0∙106 БОЕ∙мл-1. Этот объем равномерно распределяли по всей поверхности тест-объекта стеклянным шпателем. Тест-объекты распределялись на контрольные и опытные. Контрольными служили тест-объекты на момент нанесения коронавируса, опытными – после их облучения с различной экспозицией с помощью импульсных УФ установок. На каждом режиме облучалось по 5 тест-объектов.
Пробы с тест-объектов до и после облучения отбирали методом смыва двумя марлевыми тампонами (увлажненным и сухим). Каждая проба подвергалась ручному встряхиванию в течение 3 мин в 10 мл сорбирующей жидкости.
Для определения в пробах биологической активности коронавируса в каждый флакон с монослоем вносили по 0,5 мл соответствующего разведения сорбирующей жидкости и покачивая флакон, равномерно распределяли инокулят по всему монослою. Флаконы укладывали горизонтально, при этом поверхность с инфицированным клеточным монослоем находилась внизу. Флаконы инкубировали в термостате при температуре (37,0оС ±0,5) в течение 60 мин. После инкубирования инокулят удаляли пипеткой и в каждый флакон вносили по 10 мл первичного агарового покрытия, доведенного до температуры (42,0оС. ±0,5). Далее флаконы укладывали горизонтально, при этом поверхность с инфицированным монослоем находилась внизу. После затвердевания покрытия (10-15 мин) флаконы переворачивали монослоем вверх и помещали в термостат с температурой (37,0оС ±0,5) на 48 часов. По истечении срока инкубации с целью окрашивания монослоя культуры клеток во флаконы вносили вторичное агаровое покрытие, содержащее нейтральный красный, в объеме 10 мл и продолжали инкубировать при температуре (37,0оС ±0,5) в течении 24 часов. После чего подсчитывали количество негативных колоний. Испытания сопровождались постановкой следующих контролей: контроль исходной биологической активности коронавируса; контроль разводящей (сорбирующей) жидкости, контроль культуры клеток Vero 1008.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
Результаты определения уровней исходной и остаточной контаминации тест-объектов, контаминированных коронавирусом, а также эффективность их обеззараживания установкой «Альфа-06» для режимов № 1-3 представлены в таблице 2.3
Результаты определения уровней исходной и остаточной контаминации тест-объектов, контаминированных коронавирусом, а также эффективность их дезинфекции установкой «Альфа-09» для режимов № 4-6 представлены в таблице 3.
Полученные результаты экспериментов позволяют констатировать, что импульсное ультрафиолетовое излучение сплошного спектра, генерируемое установками «Альфа-06» и «Альфа-09» обладает высокой вирулицидной активностью в отношении короновируса SARS-CoV-2, вплоть до полной его инактивации (100%).
Проведенные испытания импульсных установок показали, что эффективность обработки поверхности установками:
Полученные результаты позволяют определить летальные поверхностные бактерицидные дозы импульсного ультрафиолетового излучения сплошного спектра, требуемые для полного обезвреживания поверхностей от SARS-CoV-2. Так для достижения 100% его инактивации на металлической поверхности требуются бактерицидные дозы (в спектральном интервале 200 – 300 нм) до 30 мДж/см2, а оценка пороговых доз (90% эффективность) даёт значения, не превышающие D90 = 4 мДж/см2. Эти данные позволяют разработать режимы работы импульсных установок и порядок обработки помещений с позиций доказательной медицины.
Полученные результаты позволяют рекомендовать использовать импульсные ультрафиолетовые установки «Альфа-06» и «Альфа-09» для обеззараживания помещений при проведении в них противоэпидемических мероприятий, связанных с высоким риском заноса и дальнейшего распространения возбудителя коронавирусной инфекции.