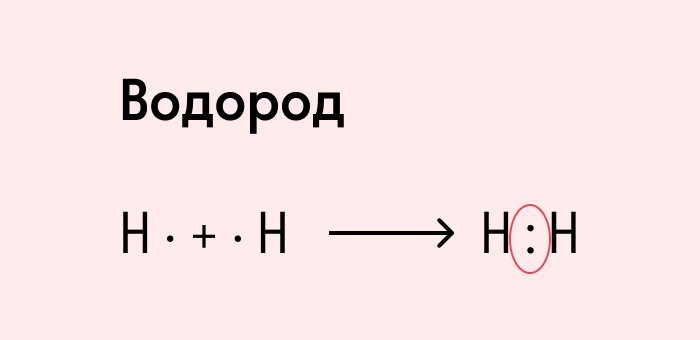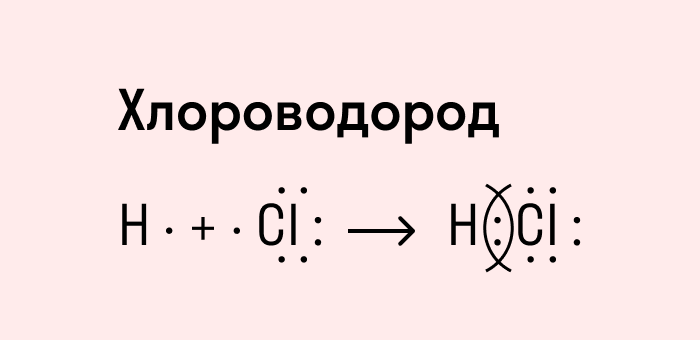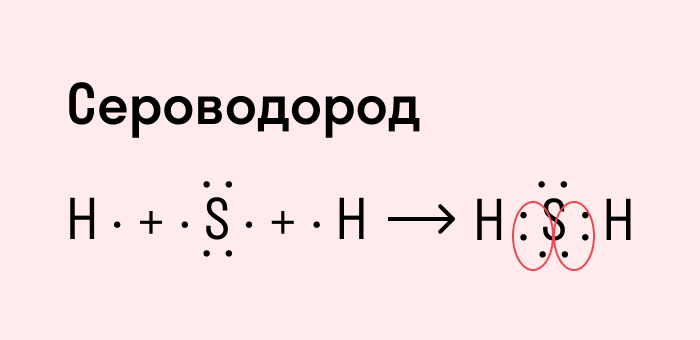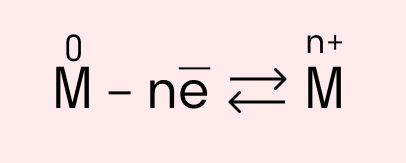в молекуле хлороводорода какая связь
Свойства хлороводорода, способы получения
Хлороводород — что это такое, формула
Хлороводород — это бесцветный газ с резким неприятным запахом.
Формула: HCl
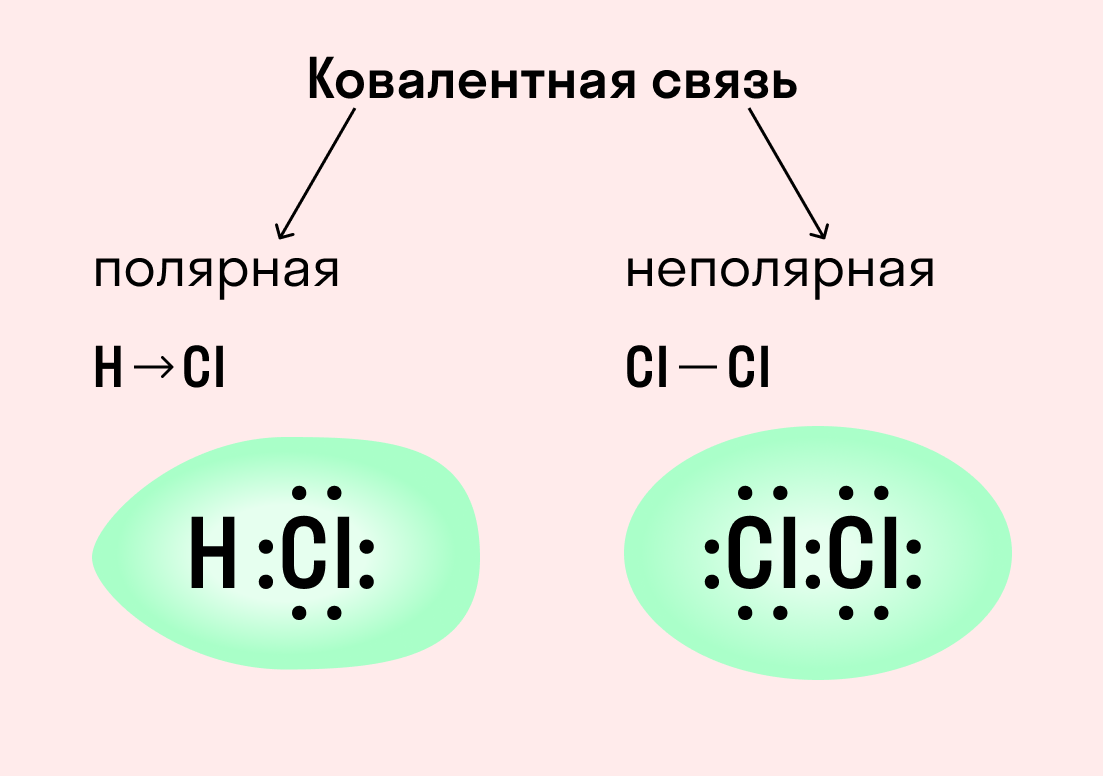
Строение его молекулы определяет название соединения. Атомы хлора и водорода соединены ковалентной полярной связью.
Физические и химические свойства
Раствор хлороводорода в воде называют соляной кислотой. Процесс растворения можно описать с помощью следующего уравнения реакции:
При растворении хлороводорода выделяется большое количество теплоты.
Соляную кислоту относят к сильным одноосновным кислотам. Соединение активно вступает в химические реакции со следующими веществами:
В результате такого взаимодействия формируются соли соляной кислоты — хлориды:
M g + 2 H C l → M g C l 2 + H 2 ↑
F e O + 2 H C l → F e C l 2 + H 2 O
В присутствии сильных окислителей или в процессе электролиза хлороводород способен проявлять свойства восстановителя, при этом окисляясь с выделением газообразного хлора:
M n O 2 + 4 H C l → M n C l 2 + C l 2 ↑ + 2 H 2 O
В условиях повышенной температуры происходит окисление хлороводорода кислородом в присутствии катализатора, роль которого играет хлорид меди ( I I ) C u C l 2 :
4 H C l + O 2 → 2 H 2 O + 2 C l 2 ↑
Концентрированная соляная кислота взаимодействует с медью, что сопровождается образованием комплекса одновалентной меди:
2 C u + 4 H C l → 2 H [ C u C l 2 ] + H 2 ↑
Смесь, в состав которой входят три объемные части концентрированной соляной кислоты и одна объемная часть концентрированной азотной кислоты, носит название «царская водка». Данная смесь способна растворять золото и платину.
«Царская водка» характеризуется высокой окислительной способностью, что объясняется наличием в составе смеси хлористого нитрозила N O C l и хлора, находящихся в равновесии с исходными веществами:
За счет большого содержания хлорид-ионов в растворе происходит связывание металла. В результате образуется хлоридный комплекс, что является причиной его растворения:
3 P t + 4 H N O 3 + 18 H C l → 3 H 2 [ P t C l 6 ] + 4 N O + 8 H 2 O
В процессе присоединения хлороводорода к серному ангидриду происходит образование хлорсульфоновой кислоты H S O 3 C l :
S O 3 + H C l → H S O 3 C l
Хлороводород вступает в реакции присоединения по кратным связям в органических соединениях (электрофильное присоединение):
Взаимодействие с основаниями
Соляная кислота взаимодействует практически со всеми основаниями. При этом протекают реакции ионного обмена, в результате которых получают соль и воду:
При смешении соляной кислоты с аммиаком протекает реакция присоединения. В результате взаимодействия образуется соль в виде хлорида аммония. Уравнение реакции будет выглядеть так:
H C l + N H 3 → N H 4 C l
Соляная кислота также вступает в реакцию с амфотерными гидроксидами, которые в данном случае проявляют основные свойства. Взаимодействие с гидроксидом цинка:
2 H C l + Z n ( O H ) 2 → Z n C l 2 + 2 H 2 O
Способы получения, область применения
Лабораторный способ получения хлористого водорода заключается в реакции концентрированной серной кислоты с твердым хлоридом натрия (поваренной солью) в условиях повышенной температуры:
N a C l + H 2 S O 4 → N a H S O 4 + H C l ↑
P C l 5 + H 2 O → P O C l 3 + 2 H C l
R C O C l + H 2 O → R C O O H + H C l
Устаревший промышленный способ получения хлористого водорода заключался в методике Леблана. В процессе реакции твердый хлорид натрия взаимодействует с концентрированной серной кислотой.
В современной промышленности хлороводород производят с помощью прямого синтеза из простых веществ:
В промышленных масштабах хлористый водород производят на специальных установках путем сжигания водорода в хлоре. Причем водород попадает в пламя в небольшом избытке. Тогда весь объем подаваемого хлора реагирует, и на выходе получается продукт более высокого качества.
Газообразный хлороводород практически не используется из-за его физических и химических характеристик. Широкое применение находит соляная кислота:
Техника безопасности
При попадании хлороводорода в дыхательные пути может наступить сильное удушье. А его водный раствор высокой концентрации вызывает химические ожоги. Поэтому работать с хлористым водородом и соляной кислотой следует только в маске (респираторе), защитных перчатках и очках.
При вдыхании газа необходимо немедленно вывести пострадавшего на воздух и при необходимости сделать искусственное дыхание. В случае проглатывания соляной кислоты требуется промывание желудка.
Если кислота попала на кожу, пораженный участок следует промыть водой и обработать слабым раствором соды, который нейтрализуют кислоту. В случае попадания на слизистые оболочки после промывания нужно закапать глаза, нос или горло раствором новокаина и дикаина с адреналином.
Хлороводород
| Хлороводород | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | хлористый водород |
| Химическая формула | HCl |
| Физические свойства | |
| Состояние (ст. усл.) | газ |
| Отн. молек. масса | 36,4606 а. е. м. |
| Молярная масса | 36,4606 г/моль |
| Плотность | 1.477 г/л, газ (25 °C) г/см³ |
| Термические свойства | |
| Температура плавления | −114,22 °C |
| Температура кипения | −85 °C |
| Температура разложения | 1500 °C |
| Критическая точка | 51,4 °C |
| Энтальпия образования (ст. усл.) | -92,31 кДж/моль |
| Химические свойства | |
| pKa | — 4 |
| Растворимость в воде | 72,47 (20 °C) г/100 мл |
| Классификация | |
| Рег. номер CAS | [7647-01-0] |
Содержание
Свойства
Водный раствор хлористого водорода называется соляной кислотой. При растворении в воде протекают следующие процессы:
Процесс растворения сильно экзотермичен. С водой HCl образует азеотропную смесь, содержащую 20,24 % HCl.
Соляная кислота является сильной одноосновной кислотой, она энергично взаимодействует со всеми металлами, стоящими в ряду напряжений левее водорода, с основными и амфотерными оксидами, основаниями и солями, образуя соли — хлориды:
Mg + 2 HCl → MgCl2 + H2↑ FeO + 2 HCl → FeCl2 + H2O
Хлориды чрезвычайно распространены и имеют широчайшее применение (галит, сильвин). Большинство из них хорошо растворяется в воде и полностью диссоциирует на ионы. Слаборастворимыми являются хлорид свинца (PbCl2), хлорид серебра (AgCl), хлорид ртути(I) (Hg2Cl2, каломель) и хлорид меди(I) (CuCl).
При действии сильных окислителей или при электролизе хлороводород проявляет восстановительные свойства:
При нагревании хлороводород окисляется кислородом (катализатор — хлорид меди(II) CuCl2):
Однако, концентрированная соляная кислота реагирует с медью, при этом образуется комплекс одновалентной меди:
Смесь 3 объемных частей концентрированной соляной и 1 объемной доли концентрированной азотной кислот называется «царской водкой». Царская водка способна растворять даже золото и платину. Высокая окислительная активность царской водки обусловлена присутствием в ней хлористого нитрозила и хлора, находящихся в равновесии с исходными веществами:
Благодаря высокой концентрации хлорид-ионов в растворе металл связывается в хлоридный комплекс, что способствует его растворению:
Для хлороводорода также характерны реакции присоединения к кратным связям (электрофильное присоединение):
Получение
В лабораторных условиях хлороводород получают, воздействуя концентрированной серной кислотой на хлорид натрия (поваренную соль) при слабом нагревании:
В промышленности хлороводород ранее получали в основном сульфатным методом (методом Леблана), основанном на взаимодействии хлорида натрия с концентрированной серной кислотой. В настоящее время для получения хлороводорода обычно используют прямой синтез из простых веществ:
В производственных условиях синтез осуществляется в специальных установках, в которых водород непрерывно сгорает ровным пламенем в токе хлора, смешиваясь с ним непосредственно в факеле горелке. Тем самым достигается спокойное (без взрыва) протекание реакции. Водород подается в избытке (5 — 10 %), что позволяет полностью использовать более ценный хлор и получить незагрязненную хлором соляную кислоту.
Соляную кислоту получают растворением газообразного хлороводорода в воде.
Применение
Водный раствор широко используется для получения хлоридов, для травления металлов, очистки поверхности сосудов, скважин от карбонатов, обработки руд, при производстве каучуков, глутамината натрия, соды, хлора и других продуктов. Также применяется в органическом синтезе.
Безопасность
Примечания
Литература
Ссылки
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | — | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Хлороводород» в других словарях:
хлороводород — хлороводород … Орфографический словарь-справочник
ХЛОРОВОДОРОД — (НСl) бесцветный дымящий на воздухе газ с резким запахом, токсичен; плотность 1,64 кг/м3, tпл = 84,8 °С. Очень хорошо растворяется в воде с образованием хлороводородной (соляной) кислоты. В промышленности его получают прямым синтезом из (см.) и… … Большая политехническая энциклопедия
хлороводород — хем. соединение на хлорот со водородот, безбоен гас, се растворува во вода како солна киселина хлороводородна киселина хем. соединение на хлорот и водородот, на, хлороводород има широка примена во хемиската индустрија … Macedonian dictionary
хлороводород — vandenilio chloridas statusas T sritis chemija formulė HCl atitikmenys: angl. hydrochloric acid; hydrogen chloride rus. водорода хлорид; хлороводород … Chemijos terminų aiškinamasis žodynas
Хлороводород — хлористый водород (см. Хлор) … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
хлороводород — (хлористый водород), HCl, бесцветный, дымящий на воздухе газ; tпл 114,2°C, tкип 85,1°C. Хорошо растворяется в воде с образованием соляной кислоты. В промышленности получают как побочный продукт при хлорировании органических соединений, синтезом … Энциклопедический словарь
ХЛОРОВОДОРОД — (хлористый водород), НС1, бесцв., дымящий на воздухе газ; tnл 114,2 °С, tкип 85,1 оС. Хорошо растворяется в воде с образованием соляной кислоты. В пром сти получают как побочный продукт при хлорировании органич. соед., синтезом из элементов,… … Естествознание. Энциклопедический словарь
хлороводород — хлороводоро/д, а … Слитно. Раздельно. Через дефис.
хлороводород — хлористый водород … Cловарь химических синонимов I
хлористый водород — хлороводород … Cловарь химических синонимов I
Химическая связь
Химическая связь и строение вещества
Все системы стремятся к равновесию и к уменьшению свободной энергии — так гласит один из постулатов химической термодинамики. Атомы, взаимодействующие в молекуле вещества, тоже подчиняются этому закону. Они стремятся образовать устойчивую конфигурацию — 8-электронную или 2-электронную внешнюю оболочку. Этот процесс взаимодействия называется химической связью, благодаря ему получаются молекулы и молекулярные соединения.
| Химическая связь — это взаимодействие между атомами в молекуле вещества, в ходе которого два электрона (по одному от каждого атома) образуют общую электронную пару либо электрон переходит от одного атома к другому. |
Как понятно из определения химической связи, при взаимодействии двух атомов один из них может притянуть к себе внешние электроны другого. Эта способность называется электроотрицательностью (ЭО). Атом с более высокой электроотрицательностью (ЭО) при образовании химической связи с другим атомом может вызвать смещение к себе общей электронной пары.
Механизм образования химической связи
Существует два механизма взаимодействия атомов:
обменный — предполагает выделение по одному внешнему электрону от каждого атома и соединение их в общую пару;
донорно-акцепторный — происходит, когда один атом (донор) выделяет два электрона, а второй атом (акцептор) принимает их на свою свободную орбиталь.
Независимо от механизма химическая связь между атомами сопровождается выделением энергии. Чем выше ЭО атомов, т. е. их способность притягивать электроны, тем сильнее и этот энергетический всплеск.
| Энергией связи называют ту энергию, которая выделяется при взаимодействии атомов. Она определяет прочность химической связи и по величине равна усилию, необходимому для ее разрыва. |
Также на прочность влияют следующие показатели:
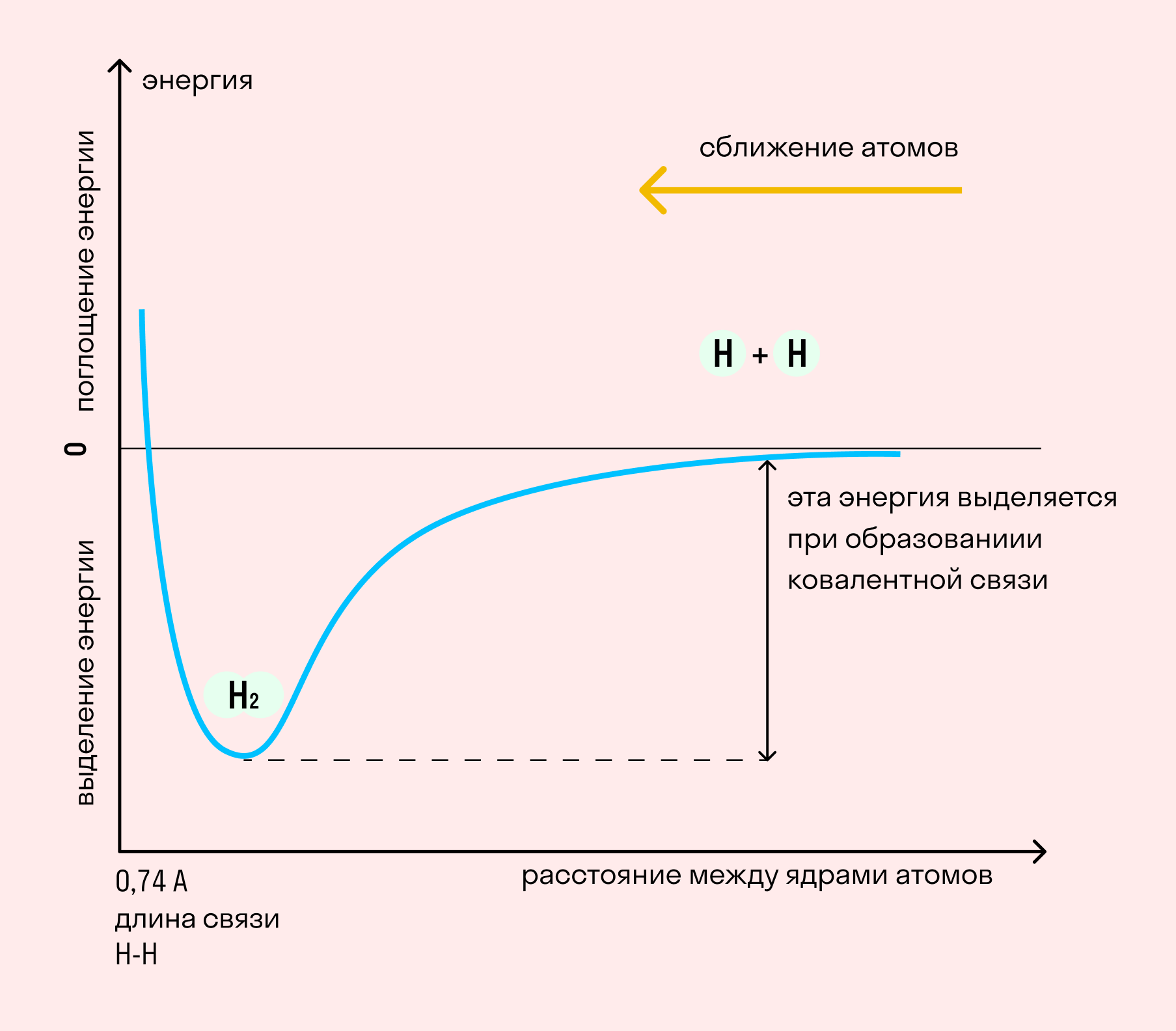
Длина связи — расстояние между ядрами атомов. С уменьшением этого расстояния растет энергия связи и увеличивается ее прочность.
Кратность связи — количество электронных пар, появившихся при взаимодействии атомов. Чем больше это число, тем выше энергия и, соответственно, прочность связи.
На примере химической связи в молекуле водорода посмотрим, как меняется энергия системы при сокращении расстояния между ядрами атомов. По мере сближения ядер электронные орбитали этих атомов начинают перекрывать друг друга, в итоге появляется общая молекулярная орбиталь. Неспаренные электроны через области перекрывания смещаются от одного атома в сторону другого, возникают общие электронные пары. Все это сопровождается нарастающим выделением энергии. Сближение происходит до тех пор, пока силу притяжения не компенсирует сила отталкивания одноименных зарядов.
Основные типы химических связей
Различают четыре вида связей в химии: ковалентную, ионную, металлическую и водородную. Но в чистом виде они встречаются редко, обычно имеет место наложение нескольких типов химических связей. Например, в молекуле фосфата аммония (NH4)3PO4присутствует одновременно ионная связь между ионами и ковалентная связь внутри ионов.
Также отметим, что при образовании кристалла от типа связи между частицами зависит, какой будет кристаллическая решетка. Если это ковалентная связь — образуется атомная решетка, если водородная — молекулярная решетка, а если ионная или металлическая — соответственно, будет ионная или металлическая решетка. Таком образом, влияя на тип кристаллической решетки, химическая связь определяет и физические свойства вещества: твердость, летучесть, температуру плавления и т. д.
Основные характеристики химической связи:
насыщенность — ограничение по количеству образуемых связей из-за конечного числа неспаренных электронов;
полярность — неравномерная электронная плотность между атомами и смещение общей пары электронов к одному из них;
направленность — ориентация связи в пространстве, расположение орбиталей атомов под определенным углом друг к другу.
Ковалентная связь
Как уже говорилось выше, этот тип связи имеет два механизма образования: обменный и донорно-акцепторный. При обменном механизме объединяются в пару свободные электроны двух атомов, а при донорно-акцепторном — пара электронов одного из атомов смещается к другому на его свободную орбиталь.
| Ковалентная связь — это процесс взаимодействия между атомами с одинаковыми или близкими радиусами, при котором возникает общая электронная пара. Если эта пара принадлежит в равной мере обоим взаимодействующим атомам — это неполярная связь, а если она смещается к одному из них — это полярная связь. |
Как вы помните, сила притяжения электронов определяется электроотрицательностью атома. Если у двух атомов она одинакова, между ними будет неполярная связь, а если один из атомов имеет большую ЭО — к нему сместится общая электронная пара и получится полярная химическая связь.
Ковалентная неполярная связь образуется в молекулах простых веществ, неметаллов с одинаковой ЭО: Cl2, O2, N2, F2 и других.
Посмотрим на схему образования этой химической связи. У атомов водорода есть по одному внешнему электрону, которые и образуют общую пару.
Ковалентная полярная связь характерна для неметаллов с разным уровнем ЭО: HCl, NH3,HBr, H2O, H2S и других.
Посмотрим схему такой связи в молекуле хлороводорода. У водорода имеется один свободный электрон, а у хлора — семь. Таким образом, всего есть два неспаренных электрона, которые соединяются в общую пару. Поскольку в данном случае ЭО выше у хлора, эта пара смещается к нему.
Другой пример — молекула сероводорода H2S. В данном случае мы видим, что каждый атом водорода имеет по одной химической связи, в то время как атом серы — две. Количество связей определяет валентность атома в конкретном соединении, поэтому валентность серы в сероводороде — II.
Число связей, которые могут быть у атома в молекуле вещества, называется валентностью.
Характеристики ковалентной связи:
Ионная связь
Как понятно из названия, данный тип связи основан на взаимном притяжении ионов с противоположными зарядами. Он возможен между веществами с большой разницей ЭО — металлом и неметаллом. Механизм таков: один из атомов отдает свои электроны другому атому и заряжается положительно. Второй атом принимает электроны на свободную орбиталь и получает отрицательный заряд. В результате этого процесса образуются ионы.
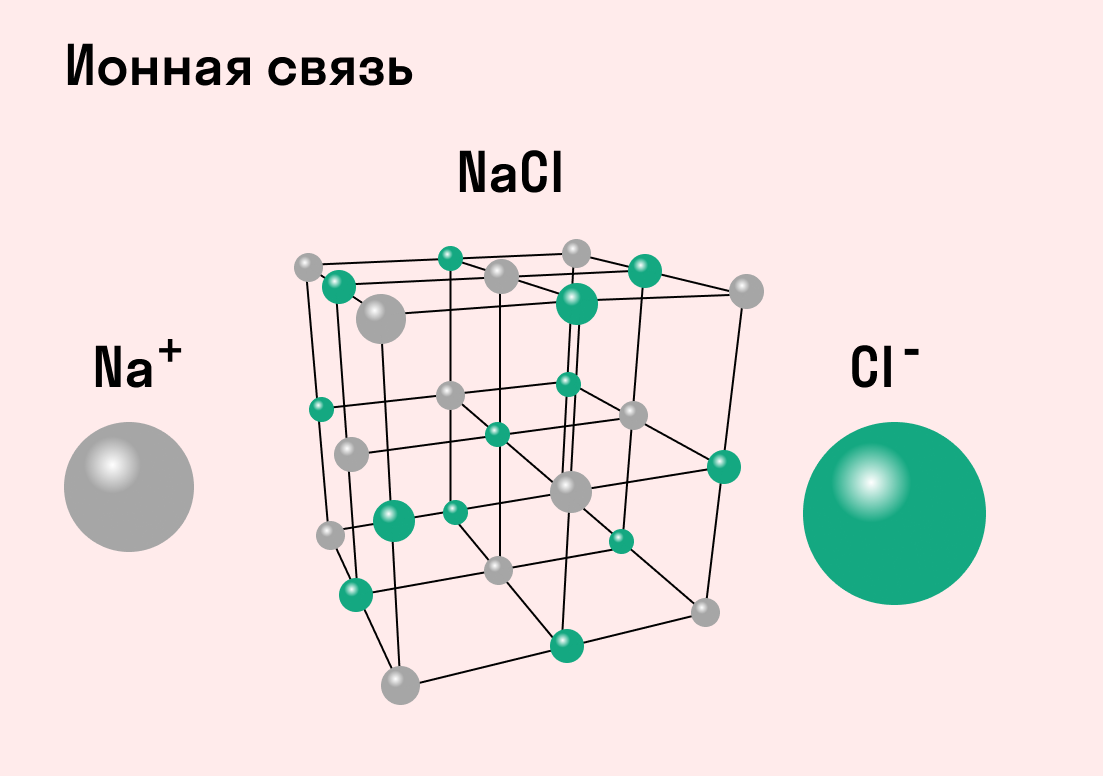
| Ионная связь — это такое взаимодействие между атомами в молекуле вещества, итогом которого становится образование и взаимное притяжение ионов. |
Разноименно заряженные ионы стремятся друг к другу за счет кулоновского притяжения, которое одинаково направлено во все стороны. Благодаря этому притяжению образуются ионные кристаллы, в решетке которых заряды ионов чередуются. У каждого иона есть определенное количество ближайших соседей — оно называется координационным числом.
Обычно ионная связь появляется между атомами металла и неметалла в таких соединениях, как NaF, CaCl2, BaO, NaCl, MgF2, RbI и других. Ниже схема ионной связи в молекуле хлорида натрия.
Характеристики ионной связи:
не имеет направленности.
Ковалентная и ионная связь в целом похожи, и одну из них можно рассматривать, как крайнее выражение другой. Но все же между ними есть существенная разница. Сравним эти виды химических связей в таблице.
Характеризуется появлением электронных пар, принадлежащих обоим атомам.
Характеризуется появлением и взаимным притяжением ионов.
Общая пара электронов испытывает притяжение со стороны обоих ядер атомов.
Ионы с противоположными зарядами подвержены кулоновскому притяжению.
Имеет направленность и насыщенность.
Ненасыщенна и не имеет направленности.
Количество связей, образуемых атомом, называется валентностью.
Количество ближайших соседей атома называется координационным числом.
Образуется между неметаллами с одинаковой или не сильно отличающейся ЭО.
Образуется между металлами и неметаллами — веществами со значимо разной ЭО.
Металлическая связь
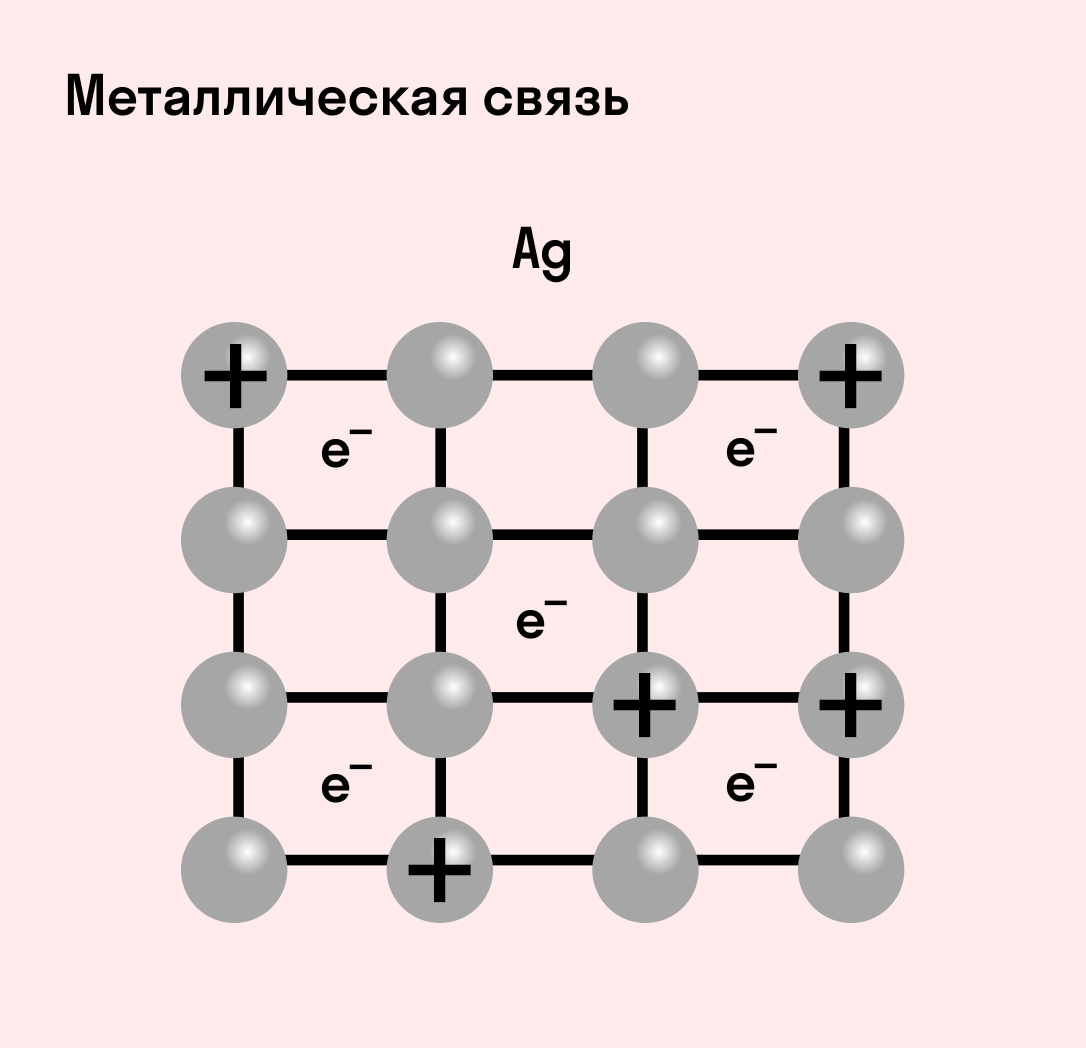
Отличительная особенность металлов в том, что их атомы имеют достаточно большие радиусы и легко отдают свои внешние электроны, превращаясь в положительно заряженные ионы (катионы). В итоге получается кристаллическая решетка, в узлах которой находятся ионы, а вокруг беспорядочно перемещаются электроны проводимости, образуя «электронное облако» или «электронный газ».
Свободные электроны мигрируют от одного иона к другому, временно соединяясь с ними и снова отрываясь в свободное плавание. Этот механизм по своей природе имеет сходство с ковалентной связью, но взаимодействие происходит не между отдельными атомами, а в веществе.
| Металлическая связь — это взаимодействие положительных ионов металлов и отрицательно заряженных электронов, которые являются частью «электронного облака», рассеянного по всему объему вещества. |
Наличие такого «электронного облака», которое может прийти в направленное движение, обусловливает электропроводность металлов. Другие их качества — пластичность и ковкость, объясняются тем, что ионы в кристаллической решетке легко смещаются. Поэтому металл при ударном воздействии способен растягиваться, но не разрушаться.
Характеристики металлической связи:
Металлическая связь присуща как простым веществам — таким как Na, Ba, Ag, Cu, так и сложным сплавам — например, AlCr2, CuAl11Fe4, Ca2Cu и другим.
Схема металлической связи:
M — металл,
n — число свободных внешних электронов.
К примеру, у железа в чистом виде на внешнем уровне есть два электрона, поэтому его схема металлической связи выглядит так:
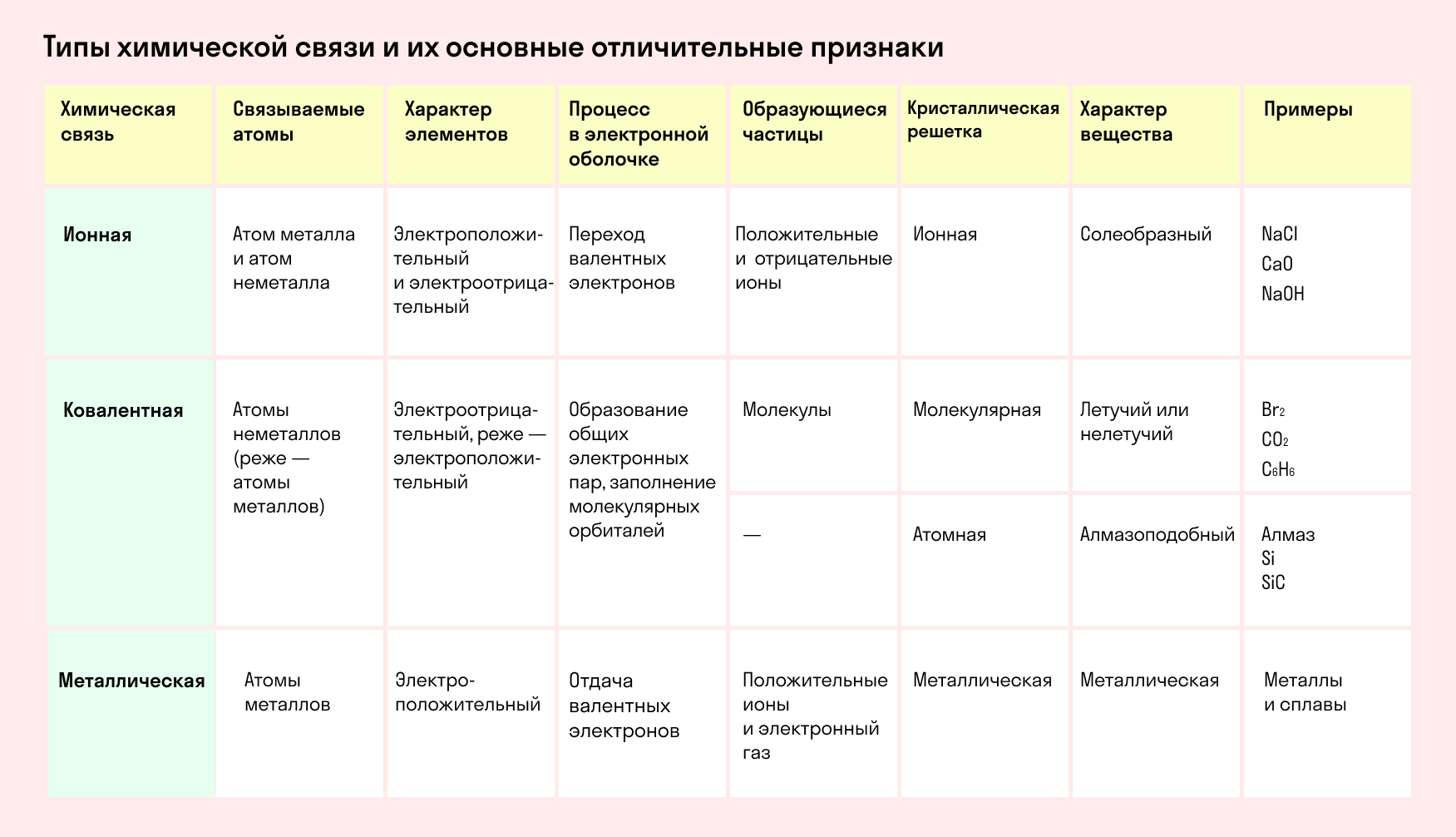
Обобщим все полученные знания. Таблица ниже описывает кратко химические связи и строение вещества.
Типы химической связи и их основные отличительные признаки
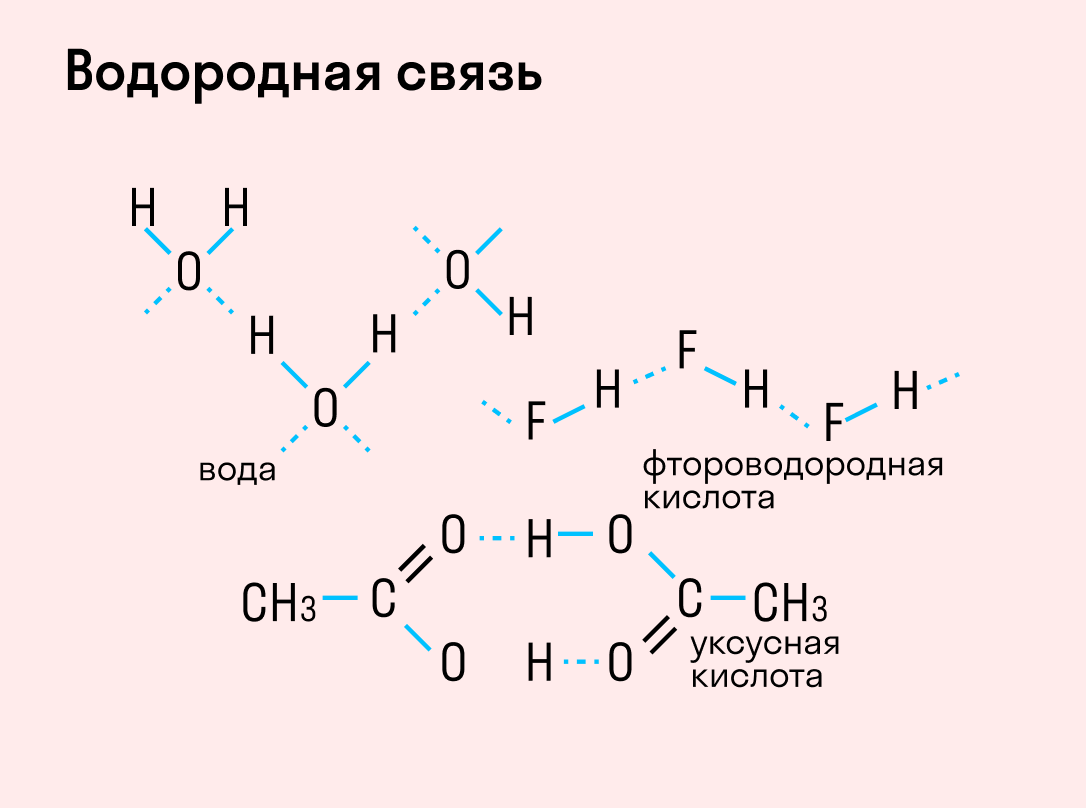
Водородная связь
Данный тип связи в химии стоит отдельно, поскольку он может быть как внутри молекулы, так и между молекулами. Как правило, у неорганических веществ эта связь происходит между молекулами.
| Водородная связь образуется между молекулами, содержащими водород. Точнее, между атомами водорода в этих молекулах и атомами с большей ЭО в других молекулах вещества. |
Объясним подробнее механизм этого вида химической связи. Есть молекулы А и В, содержащие водород. При этом в молекуле А есть электроотрицательные атомы, а в молекуле В водород имеет ковалентную полярную связь с другими электроотрицательными атомами. В этом случае между атомом водорода в молекуле В и электроотрицательным атомом в молекуле А образуется водородная связь.
Такое взаимодействие носит донорно-акцепторный характер. Донором электронов в данном случае выступают электроотрицательные элементы, а акцептором — водород.
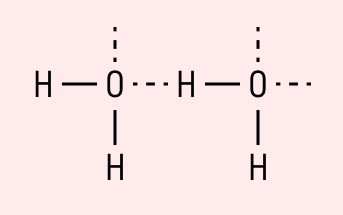
Графически водородная связь обозначается тремя точками. Ниже приведена схема такого взаимодействия на примере молекул воды.
Характеристики водородной связи:
Кратко о химических связях
Итак, самое главное. Химической связью называют взаимодействие атомов, причиной которого является стремление системы приобрести устойчивое состояние. Во время взаимодействия свободные внешние электроны атомов объединяются в пары либо внешний электрон одного атома переходит к другому.
Образование химической связи сопровождается выделением энергии. Эта энергия растет с увеличением количества образованных электронных пар и с сокращением расстояния между ядрами атомов.
Основные виды химических связей: ковалентная (полярная и неполярная), ионная, металлическая и водородная. В отличие от всех остальных водородная ближе к молекулярным связям, поскольку может быть как внутри молекулы, так и между разными молекулами.
Как определить тип химической связи:
Ковалентная полярная связь образуется в молекулах неметаллов между атомами со сходной ЭО.
Ковалентная неполярная связь имеет место между атомами с разной ЭО.
Ионная связь ведет к образованию и взаимному притяжению ионов. Она происходит между атомами металла и неметалла.
Металлическая связь бывает только между атомами металлов. Это взаимодействие положительных ионов в кристаллической решетке и свободных отрицательных электронов. Масса рассеянных по всему объему свободных электронов представляет собой «электронное облако».
Водородная связь появляется при условии, что есть атом с высокой ЭО и атом водорода, связанный с другой электроотрицательной частицей ковалентной связью.
Химическая связь и строение молекулы: типом химической связи определяется кристаллическая решетка вещества: ионная, металлическая, атомная или молекулярная.
Определить тип химической связи в 8 классе поможет таблица.