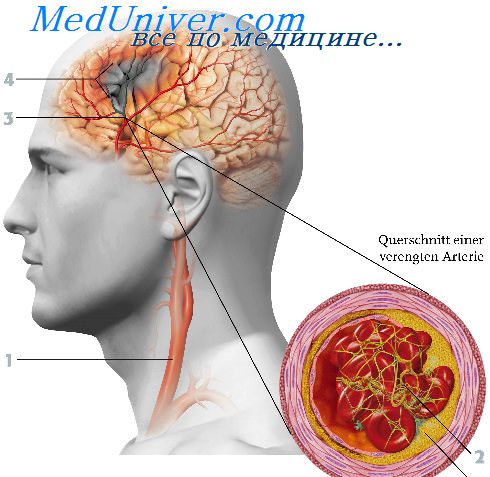
заболевание сосудов головного мозга у детей
Определение значения венозных церебральных нарушений у детей в клинической практике с возможностью обоснованной терапии
Проведено клинико-ультразвуковое обследование детей с головными болями. Выявлен большой процент нарушений церебральной гемодинамики, наиболее выраженные венозные нарушения отмечены у детей со структурными церебральными аномалиями. Рассмотрены подходы к те
Clinical ultrasonic examination of children with headaches was conducted. High percentage of disorders in cerebral hemodynamics was revealed, the most pronounced venous disorders were revealed in children with structural cerebral anomalies. Approaches to their therapy were considered.
Нарушения церебрального кровообращения имеют большое значение в клинических проявлениях цереброваскулярной патологии от головной боли до развития энцефалопатии и влияют на функциональное состояние мозга у пациентов любого возраста. Достаточно хорошо изучены артериальные нарушения, тогда как гемодинамическим венозным нарушениям часто не уделяется достаточно внимания.
60 лет назад М. И. Холоденко впервые описал энцефалопатию (венозную), развившуюся при венозном застое головного мозга. Церебральная венозная патология (формы) у взрослых пациентов представлена в работах физиологов и клиницистов: Е. З. Неймарк (1971), М. Я. Бердичевский (1989), И. Д. Стулин, В. А. Карлов (1981–2016), В. Д. Трошин (1995–1999), М. М. Одинак (1997–2010), В. А. Шахнович (1996–1999), М. В. Шумилина (2003–2016) [1–14].
В детской клинической флебологии большую роль имеют работы отечественных ученых: В. Д. Трошин (1995), Е. М. Бурцев (1986, 1999), А. В. Андреев (1998, 1999, 2004) [5, 10,12–13].
Бердичевский выделил формы нарушений церебральной венозной гемодинамики (дистоническую и застойно-гипоксическую), в 1999 г. В. Д. Трошиным представлены клинические проявления этих нарушений — энцефалопатии. Синдромы венозной энцефалопатии, представленные в литературе: астеновегетативный, псевдотуморозно-гипертензионный, полиморфный, беттолепсии, психопатологический, инсультообразный, терминальных и претерминальных судорог. Астеновегетативный и псевдотуморозно-гипертензионный синдромы наиболее часто встречаются в клинической практике [2, 5, 9, 12–15]. Но несмотря на столь длительный срок изучения и такое количество научных работ, даже при наличии выраженных церебральных венозных проявлений вопрос о самом наличии «венозной энцефалопатии» или, другими терминами, «венозной дисциркуляторной энцефалопатии», «венозной дисгемии» продолжает дискутироваться и не всегда принимается во внимание в практике врачей.
Затруднение церебрального венозного оттока (затруднение венозной и ликвородинамики) кратковременно, с компенсацией проявляется при физическом напряжении в физиологических условиях (при проведении функциональных проб), а также при повышении ликворного давления, аномалиях строения церебральных вен (впадающих в синусы) и синусов мозга. Нарушения центральных регуляторных механизмов сосудистого тонуса [5] — еще один фактор нарушений венозной циркуляции с проявлением астеновегетативного синдрома (венозной дистонии, флебопатии), чаще у пациентов с дисплазией соединительной ткани (ДСТ).
Опыт нашей работы показывает, что до сих пор не в полном объеме используются возможности современных инструментальных методов исследования, особенно у пациентов с функциональными (а не только органическими) нарушениями. Необходимо проводить ультразвуковые исследования церебрального и экстрацеребрального артериального и венозного кровотока с определением структурных и скоростных характеристик. Основным является немногочисленность исследований по отдельным нозологическим формам у детей, нет единых показателей нормы гемодинамических показателей (скоростей и индексов), разночтения в оценке полученных результатов, недостаточная информированность детских неврологов и педиатров о возможности раннего выявления нарушений церебральной венозной гемодинамики [14–18]. Хронические церебральные венозные нарушения в большинстве случаев приводят к различным клиническим проявлениям венозной энцефалопатии, которые значительно ухудшают когнитивные навыки, школьную успеваемость, физическую активность ребенка.
Взаимосвязь флебо- и ликвороциркуляции часто приводит к манифестации симптомов нарушения ликвородинамики (гипертензивных нарушений) от субклинических (характерные головные боли, вегетативные нарушения по типу «панических атак», но при отсутствии изменений на глазном дне) до внутричерепной венозной гипертензии («тяжелые» до рвоты головные боли распирающего характера, преимущественно в ночные утренние часы, выраженные вегетативные нарушения, изменения на глазном дне). Затруднение ликвороциркуляции и венозного оттока (флебогипертензии) из полости черепа с возможным развитием венозного застоя с гипоксией и гиперкапнией (отек мозговой ткани) приводит к нарушению компенсаторных механизмов с нарушением метаболических процессов. Таким образом, у пациентов с нарушениями церебрального венозного оттока и проявлениями венозной энцефалопатии проблема восстановления флебо- и ликвороциркуляции (гипертензии) является основной и определяет актуальность выбора медикаментозных средств, с обязательным учетом состояния венозного церебрального оттока.
Наиболее оптимальным в диагностике и медикаментозной терапии является системный подход в оценке этиологии, клиники и патогенеза нарушений венозной гемодинамики. При выборе медикаментозной терапии церебральных венозных нарушений имеются определенные сложности, так как обычно отсутствует патогенетическое обоснование назначения «сосудистой» терапии «вслепую», игнорирующей диагностические методы; возможно, с этим связаны неудачи или кратковременность эффекта. Патогенетически обоснованные схемы терапии направлены на снижение продукции ликвора (диуретики, венотоники), восстановление гемодинамических и метаболических показателей (венотоники, препараты ноотропного ряда), с учетом симптоматики и диагностических особенностей. Не допустимо «хаотичное» назначение «сосудистых» препаратов.
В течение 17 лет используя клинические и гемодинамические данные нарушений церебральной венозной гемодинамики у детей, нами разработаны (под контролем методов ультразвуковой диагностики) схемы патогенетически обоснованной терапии (уровень доказательности D). Диуретики и венотоники являются основой в терапии венозных нарушений. Диакарб® обладает патогенетическим действием — подавляет активность фермента карбоангидразы в сосудистых сплетениях желудочков головного мозга, что приводит к снижению продукции ликвора, при этом отличаясь от осмотических диуретиков «мягким» действием без электролитных нарушений при длительном применении [19–20].
Венотоники растительного (Эскузан®, дигидроэрготамин мезилат, эрготамин и др.) и синтетического (Детралекс®) происхождения используются для нормализации венозного оттока (исторически в литературе представлено действие на периферические сосуды). Учитывая выраженное защитное действие на капилляры (артериальные и венозные) с антиэкссудативным действием, назначен тритерпеновый гликозид (сапонин) из плодов конского каштана: эсцин (AESCINE), Эскузан®.
У детей с нарушениями венозного церебрального кровообращения страдает прежде всего мозговая ткань (от гипоксии до застоя), что сопровождается развитием метаболических расстройств. Поэтому обязательно в комплексном лечении включение метаболических препаратов, которые влияют на обмен веществ в тканях естественных медиаторов нервной и гуморальной регуляции.
Семакс® — препарат из группы нейропептидов, обладающий ноотропным и адаптивным эффектами. Основа механизма действия препарата Семакс® — модуляция адаптивных изменений и повышение сопротивления клеточного метаболизма лимбической системы к гипоксии.
Целью настоящей работы было определение значения венозных церебральных нарушений у детей в клинической практике с возможностью коррекции (обоснованной терапии) этих нарушений.
Материалы и методы исследования
Проведено неврологическое и ультразвуковое исследование брахиоцефальных сосудов более, чем у 7000 детей (от полутора до 18 лет), что позволило определить наличие (или отсутствие) взаимосвязи клинических проявлений с состоянием церебральной и экстрацеребральной гемодинамики.
Исследования проводились на ультразвуковых аппаратах: Ангиодин (по технологии «multigate» с одновременной регистрацией допплерограмм с различных глубин) «БИОСС» (Россия), Сономед-400/М «Спектромед» (Россия), Toshiba Aplio 500 (Япония), Voluson 730 Expert (GE), Logiq P-5. Визуализация кавернозных синусов, глазных вен проведена с помощью предложенной нами новой методологии [23, 24]. Магнитно-резонансная томография (МРТ) — в структурном и сосудистом режимах.
Результаты исследования
Синдромы ДСТ отмечены у 70% детей, из них у 32% детей синдром неврологических нарушений (головная боль, вегетативная дисфункция, тики, минимальная мозговая дисфункция, синдром дефицита внимания и гиперактивности).
Дети с головными болями распределены на группы согласно клиническим проявлениям и критериям Международной классификации головных болей [24, 25]. Продолжая наши клинические исследования и используя полученные данные комплексного ультразвукового исследования, отмечено, что процентное соотношение различных типов головных болей у детей — мигрень, головные боли напряжения и головные боли, вызванные нарушением церебральной венозной гемодинамики («неклассифицированные головные боли»), — практически одинаковое (25%, 27%, 26% соответственно). Остальные 22% — это дети с головными болями, возникающими при изменении артериального давления (АД) (как повышении, так и понижении АД).
Но у детей всех этих групп отмечено нарушение венозного оттока по основным венозным коллекторам (до 40%) [13, 19, 24–26].
У 112 пациентов (6–12 лет) с выраженными венозными гемодинамическими нарушениями по кавернозным синусам, вене Галена, прямому синусу с помощью МРТ получены следующие данные: выявлена аномалия строения краниовертебрального перехода (Арнольда–Киари I степени) у 57 детей; аномалии строения глубоких вен головного мозга у 55 детей: гипоплазия поперечных синусов у всех детей, в сочетании с гипоплазией сигмовидных синусов у 90% и верхнего сагиттального синуса у 7% [24, 25] (рис. 1).
Аномалии строения костной и сосудистой системы выявлены у детей с головными болями, вызванными нарушением церебральной венозной гемодинамики, и относятся к проявлению синдрома ДСТ. Но, как правило, эти пациенты являются «трудными» на амбулаторном приеме, так как наличие аномалий строения часто объясняет невозможность проведения каких-либо терапевтических мероприятий. Таким образом, клинические особенности нарушений венозной церебральной гемодинамики являются определяющими и наиболее «ярко» проявляются у пациентов (не только детского возраста) с аномалиями строения (Арнольда–Киари I степени, глубоких вен мозга). Так как основная жалоба — головные боли, необходимо подчеркнуть, что они имеют очень характерные признаки, хорошо описываются пациентами любого возраста: распирающего характера в затылочной и теменной областях (100%), возникающие (преимущественно) во время или после ночного и дневного сна (76–92%); синдром «тугих воротников, высокой подушки». Усиление головных болей отмечено после физических упражнений (наклонов, прыжков, кувырков на уроках физкультуры, занятиях спортом — 76%), после уроков в школе (длительная статическая поза — 65%), перемене атмосферного давления, температуры окружающей среды, смене климатических условий (97%). Зрительные расстройства, кратковременное снижение остроты зрения, появление пелены, двоения также часто связаны с головной болью (43%).
.png)
При исследовании гемодинамических показателей методами транскраниальной допплерографии (ТКДГ) и транскраниального дуплексного сканирования (ТКДС) у всех пациентов выявлено нарушение оттока по глубоким венам мозга (прямому синусу и вене Галена) с повышением линейной скорости кровотока до 58 см/с (при норме 14–22 см/с), по кавернозным синусам более 30 см/с (при норме 10–12 см/с) у 46–64% детей [22, 25, 26].
Также регистрировались выраженные нарушения венозного оттока по основному и позвоночным венозным сплетениям (в норме не регистрируется), по сосудам вертебрально-базилярного бассейна — нарушение скоростных характеристик по основной артерии (рис. 2), которое преобладало у пациентов с аномалией Арнольда–Киари I (табл. 1).
Схемы медикаментозной терапии включали Диакарб® 0,25 мг, Эскузан® и Семакс® 1%.
Значительные положительные результаты получены на следующей схеме приема ацетазоламида (Диакарб®) 0,25 мг: 1 таблетка (1/2) утром до еды — 2 дня (выходные дни) в неделю. Курс лечения 2 месяца под контролем измерения артериального и венозного давления и гемодинамических показателей церебрального артериального и венозного кровотока.
Эскузан® 20 мг по 8 капель 3 раза после еды (утром, вечером, на ночь).
Для восстановления клеточного метаболизма, поврежденного при венозных церебральных нарушениях, нами рекомендован препарат Семакс® 1%.
В соответствии с объективными данными и показателями ТКДГ (ТКДС) у 85% детей отмечен выраженный положительный эффект от терапии, проведенной в течение первых 2 месяцев, у 15% детей — после второго курса лечения (рис. 3).
По результатам проведенных курсов (первого и второго) лечения происходило значительное восстановление венозного оттока (уменьшение линейной скорости кровотока (ЛСК)) по глубоким венам мозга после первого курса лечения при аномалии Арнольда–Киари, при гипоплазии синусов мозга улучшение (восстановление) венозного оттока происходило постепенно после второго курса лечения (рис. 4, табл. 2).
Клинически это проявлялось значительным снижением интенсивности и частоты головной боли, тошноты, рвоты, носовых кровотечений (до полного исчезновения этих симптомов).
Результаты исследования кровотока по прямому синусу и вене Галена до и после лечения: снижение ЛСК с 47 см/с до 36 см/с и с 50 см/с до 38 см/с соответственно у пациентов с аномалией Арнольда–Киари. У пациентов с гипоплазией венозных синусов замедление ЛСК по прямому синусу с 44 см/с до 28 см/с и по вене Галена с 47 см/с до 32 см/с. Также происходило исчезновение пульсации (рис. 5).
Обсуждение
Хронические церебральные венозные нарушения клинически в большинстве случаев проявляются симптомами венозной энцефалопатии (головные боли, часто пароксизмы вегетативных нарушений по типу «панических атак», значительно ухудшающие качество жизни детей, усиливающие когнитивные нарушения и т. д.). Но не достаточно ориентироваться при постановке диагноза с последующим назначением медикаментозной терапии только на головные боли. Отмечено, что у детей характер головной боли достоверно не отражает истинное состояние церебральной гемодинамики. Необходимо проводить комплексное исследование церебрального артериального и венозного кровотока с определением структурных и скоростных характеристик, а также различной степени выраженности венозной дисфункции. Ультразвуковые методы диагностики сосудов головы и шеи являются скрининговым, безопасным (многократно повторяемым) методом у детей, позволяющим определить наличие нарушений церебральной гемодинамики, выявить особенности артериальных или венозных нарушений. При выраженных нарушениях церебральной гемодинамики необходимо проводить МРТ-исследование в режиме МР-венографии. Также изучение особенностей проявлений церебральной венозной патологии позволяет определить тактику патогенетического лечения и осуществлять контроль его эффективности.
Основным препаратом является Диакарб® 0,25 мг, который играет большую роль в восстановлении церебральных гемо- и ликвородинамических нарушений. Отношение к этому препарату только как препарату «симптоматического лечения» не совсем корректно. В литературе отмечено одно из фармакологических действий ацетазоламида — метаболическая ауторегуляция мозгового кровотока с вазодилятацией микроциркуляторного русла, в которое входят и венулы (флебо- и ликвороотток). Учитывая, что при нарушениях церебрального венозного оттока чаще всего регистрируется усиление скорости венозного потока, то одной из причин его восстановления (снижения скорости) при приеме ацетазоламида является также вазодилятация венозных сосудов (так как нарушения возникают за счет либо сдавления, в том числе и ликвором, — с последующим сужением, либо при наличии анатомических препятствий). Предпочтение приема препарата Диакарб® зависит от его свойств: снижая избыточную продукцию жидкости (спинномозговая, внутриглазная), за счет подавления активности карбоангидразы приводит к уменьшению продукции жидкости, т. е. точка приложения действия ацетазоламида — любой орган/система органов, где есть карбоангидраза (эритроциты, сосудистые сплетения головного мозга, ресничное тело глаза). Также Диакарб® оказывает влияние на метаболическую регуляцию мозгового кровотока, вызывая вазодилятацию микроциркуляторного русла, в которое входят и венулы, а учитывая, что чаще всего регистрируется усиление скорости венозного оттока (за счет сдавления/сужения сосудов), то одной из причин восстановления оттока (снижения скорости) и является вазодилятация венозных сосудов. Таким образом, необходимо акцентировать внимание на том, что препарат Диакарб® участвует в сложном процессе притока/оттока церебральной гемодинамики, восстанавливая венозный и ликворный отток. Современное представление о дозировании препарата ацетазоламид (Диакарб®), 0,25, изменилось (3 раза по 3 дня с паузами в 2–3 дня лишь поддерживают диурез, так как выведение ацетазоламида из организма происходит через 24 часа). При нарушениях церебральной венозной гемодинамики (доброкачественное течение) необходимо «мягкое», «ненасильственное», «неинвазивное» воздействие на восстановление венозного оттока из полости черепа, из-за «нежной» морфологии венозное русло является тем тонким местом, которое реагирует — «рвется» при различных воздействиях, поэтому длительный прием с краткими паузами не оправдан при венозных церебральных нарушениях. Отмечаем, что выработка ликвора происходит в 3–5 часов утра (подтверждение — головные боли в утренние часы), поэтому детям с клиническими и гемодинамическими (ТКДГ, ТКДС) нарушениями церебральной венозной гемодинамики (доброкачественного течения) для «мягкого» воздействия нами предложены «короткие» схемы приема препарата Диакарб® при длительном приеме. Также по данным наших исследований применение препарата Диакарб® необходимо в сочетании с вазоактивными препаратами: Эскузан®, Эскулюс композитум.
Отмечен хороший эффект в составе комплексной терапии препаратами с ноотропным действием (Семакс®), так как у детей с церебральными венозными нарушениями в результате гипоксии, а затем отека развиваются метаболические нарушения мозговой ткани. Семакс® из группы регуляторных пептидов обладает высокой физиологической активностью и полифункциональностью: способствует нормализации в мозговой ткани уровня наиболее важных нейротрофических факторов (фактора роста нервов, фактора роста и дифференцировки нервной ткани и трофического фактора роста нейрона, что повышает функциональную пластичность мозговой ткани (усиливается рост дендритов и плотность межнейрональных связей) и способствует более полноценному восстановлению нарушенных функций, т. е. является нейромодулятором ЦНС.
Нейрометаболический эффект препарата Семакс® связан с активизацией транспорта и усвоения глюкозы, повышением выработки АТФ нейронами и глиальными клетками, что улучшает переносимость гипоксии нервной тканью. Также за счет антиоксидантного и антигипоксического влияния при венозных церебральных нарушениях, приводящих к набуханию, отеку и снижению деятельности нервных клеток, оказывает гуморально-метаболическое влияние на показатели вегетативной регуляции, таким образом являясь нейрозащитным препаратом.
Определено позитивное влияние препарата Семакс® на восстановление нарушений парасимпатического отдела вегетативной нервной системы также за счет нейрометаболического действия (ноотропное, психостимулирующее, нейрозащитное, антиоксидантное и антигипоксическое).
Выводы
Литература
М. Ф. Абрамова, кандидат медицинских наук
ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Заболевание сосудов головного мозга у детей
Врожденные пороки сосудов формируются вследствие нарушения развития сосудистой системы и могут быть в виде аневризм или аномалий строения капилляров между артериальной и венозной системой.
Артериальные и артерио-венозные аневризмы — это дефект стенки сосуда в месте бифуркации артерий или вен. Нарушение строения сосудистой стенки сопровождается ее мешотчатым расширением (аневризма).
У детей раннего возраста наиболее частой аномалией является дефект развития вены Галена. Порок представляет собой прямой анастомоз между задней мозговой или верхней мозжечковой артерией и веной Галена. Аневризматическое расширение сдавливает сильвиев водопровод, III желудочек, пластинку четверохолмия. В результате артерио-венозного шунтирования и переполнения венозной системы у ребенка с рождения развивается сердечная недостаточность. Сдавление III желудочка и сильвиева водопровода приводит к формированию гидроцефалии. На первом году жизни она проявляется быстрым нарастанием окружности черепа без клинических признаков повышения внутричерепного давления. Заподозрить возможность аневризмы помогает наличие других сосудистых аномалий на лице, черепе, туловище, конечностях, а также изменения со стороны сердца. На 2—3-м году жизни ребенка основным в клинике заболевания является синдром повышения внутричерепного давления.
Дети малоактивны, плохо спят, страдают головной болью, рвотой. В области лба, висков — расширение поверхностных вен, их извитость. При больших размерах аневризмы наблюдается односторонний, реже двусторонний, различной степени выраженности «пульсирующий экзофтальм». Артерио-венозное шунтирование сопровождается шумом в голове, который нередко отмечается ребенком и может быть прослушан врачом. Шум бывает локальным или диффузным, интенсивность его изменяется синхронно с пульсом. Очаговая неврологическая симптоматика проявляется птозом, косоглазием, вялой реакцией зрачков на свет, снижением зрения. Эти симптомы возникают в результате сдавления аневризмой черепномозговых нервов, часто бывают «мерцающими». На глазном дне — выраженные застойные явления, отек соска зрительного нерва, возможны аномалии развития сосудов глазного дна.
Наличие артерио-венозного шунта подтверждается повышением парциального давления кислорода в яремной вене. Это простой и демонстративный тест для диагноза аномалии вены Галена. Диагноз уточняется с помощью пневмоэнцефалографии, которая позволяет выявить наличие масс, проецирующихся кпереди от III желудочка. Ангиография устанавливает характер и размер аневризмы.
Артерио-венозные аневризмы, локализующиеся на поверхности гемисфер, в бассейнах передней и средней мозговых артерий, у детей раннего возраста могут быть «немыми». Однако в некоторых случаях отмечаются периодические мигренозные головные боли, очаговые неврологические симптомы. Основные из них — фокальные моторные и сенсорные припадки. Они могут быть единственным симптомом в течение многих лет, не сопровождаются изменениями биоэлектрической активности мозга в межприступный период.
Артериальные аневризмы у детей раннего возраста обычно клинически не проявляются. В редких случаях отмечаются головная боль, нарушения сна. Головная боль усиливается после физического или эмоционального напряжения. В неврологическом статусе возможно изолированное преходящее одностороннее поражение черепномозговых нервов, чаще глазодвигательных. Диагноз артериальной или артерио-венозной аневризмы уточняется с помощью ангиографии.
Разрыв аневризмы наступает внезапно или может быть спровоцирован физическим напряжением, травмой. О возможности разрыва аневризмы всегда следует подумать, когда тяжелое состояние — потеря сознания, судороги — развивается у ребенка после легкой травмы головы. Разрыв артериальной и артерио-венозной аневризмы характеризуется клиникой внутричерепного кровоизлияния. Наиболее часто наблюдаются субарахноидальные кровоизлияния.
У детей раннего возраста наблюдаются и другие типы пороков развития сосудов головного мозга: телеангиэктазии, кавернозные гемангиомы. Они могут быть изолированными, но чаще являются одним из проявлений генетически детерминированпых заболеваний, таких, как энцефалотригеминальный ангиоматоз (болезнь Штурге — Вебера), цереброретинальный ангиоматоз Гиппеля-Линдау, сосудисто-костная дизэмбриоплазия и др.
.gif)
.png)
_575.gif)
.gif)