зона мозга отвечающая за сон
Зона мозга отвечающая за сон
История становления и современное состояние проблемы сна и бодрствования подробно изложены в целой серии монографий, опубликованных в последние годы. Мы кратко остановимся лишь на тех аспектах этой проблемы, которые имеют непосредственное отношение к патогенезу паркинсонизма.
Благодаря классическим опытам бельгийского нейрофизиолога Бремера, проведенным в 30-х гг. текущего столетия, было впервые доказано, что механизмы, поддерживающие бодрствование, расположены в стволе головного мозга. При пересечении у кошки ствола мозга на уровне среднего мозга наблюдалась ЭЭГ-картина постоянного сна, при пересечении же мозга на более низком уровне — на уровне первого шейного сегмента — констатировалось типичное чередование ЭЭГ-картины сна и бодрствования.
Наступление поведенческой и ЭЭГ-картины постоянного сна в первом эксперименте объясняли отсечением от полушарий стволовых структур, обеспечивающих бодрствование.
Эти структуры были окончательно идентифицированы в 1949 г. в результате исследований Моруцци и Мэгуна, которыми было показано, что раздражение ретикулярной формации ствола мозга закономерно вызывало пробуждение спящего животного с характерными изменениями на ЭЭГ.
В последующих экспериментах было доказано, что перерезка специфических лемнисковых систем ствола мозга при интактности ретикулярной формации не приводит к подобным изменениям поведения и ЭЭГ. Поведенческая и ЭЭГ-картина сна наступала только при разрушении ретикулярной формации, сконцентрированной в медиальных отделах ствола мозга. Активирующую ретикулярную систему называют также системой пробуждения (arousal system).
Электроэнцефалографическая реакция в виде угнетения медленных волн и появления быстрых низкоамплитудных колебаний с тех пор называется реакцией активации, или реакцией пробуждения (arousal reaction).
По современным представлениям, бодрствование является не однозначным, а сложно градуированным процессом, который может флюктуировать от состояния напряженной бдительности до расслабленного бодрствования, и обеспечивается активирующей восходящей системой, прослеживаемой на всем протяжении ствола мозга и гипоталамуса, с особым сгущением ее нейронов в понто-мезенцефальной области. Наступление естественного сна поначалу объясняли функциональной блокадой активирующих импульсаций с реципрокным облегчением синхронизирующих механизмов зрительного бугра.
Однако большая серия последующих работ привела к существенному изменению и усложнению вышеуказанной схемы.
Помимо таламуса было выявлено наличие еще двух синхронизирующих структур в каудальных отделах мозгового ствола, а также гипногенной системы, расположенной в базальных отделах переднего мозга. Раздражение головки хвостатого ядра приводит к появлению в коре мозга билатерально синхронных вспышек веретенообразных волн, сходных с «сонными веретенами», и поведенческой заторможенности. Этот эффект реализуется через передневентральное ядро таламуса.
Описаны и другие структуры мозга, принимающие участие в механизмах синхронизации. Таким образом, и активирующие, и сомногенные системы мозга представляют собой сложные комплексы мозговых образований, расположенных на разных уровнях мозга и объединенных общей задачей координированного управления базисными состояниями организма. В настоящее время сон рассматривается как сложно организованный активный процесс, состоящий из двух основных фаз — фазы, медленного и фазы быстрого сна.
Основным ЭЭГ-проявлением фазы медленного сна являются синхронизированные корковые потенциалы в виде «сонных веретен» и высокоамплитудных медленных дельта-волн. В зависимости от представленности тех или иных компонентов на ЭЭГ в фазе медленного сна выделяют четыре последовательно наступающие стадии: поверхностный сон (I стадия), легкий сон (стадия «сонных веретен», или II стадия), сон средней глубины (III стадия) и глубокий сон (IV стадия). Последние две стадии иногда называют дельта-сном. Дельта-сон завершает фазу медленного сна, за которой следует фаза быстрого сна.
Голова – предмет тёмный, но исследованию подлежит. Что за что отвечает в головном мозге?
Способность дышать и двигаться, чувствовать боль и любить, создавать гениальные творения и совершать зло, подчас не поддающееся объяснению. Благодаря чему всё это возможно? Где скрывается наше «я»?
Как устроен головной мозг человека, как соотносятся его строение и функции, и каковы их особенности?
Попробуем разобраться в некоторых из них.
Существует положение, что чем более проста некая функция, тем точнее место ее локализации в головном мозге. С другой стороны, наиболее сложные функции обеспечиваются слаженной работой всего мозга, в связи с чем понятие «коркового центра» (определённой области коры головного мозга) большей частью относительное и условное.
Внезапно залаяла собака во дворе? Ориентировочный рефлекс в ответ на резкий звук возможен благодаря среднему мозгу. Кроме того, через этот отдел проходят пути, обеспечивающие зрение, слух, способность к движению и бдительности, контроль температуры и ряд других, которыми занимаются другие отделы мозга.
КОРА БОЛЬШИХ ПОЛУШАРИЙ ИМЕЕТ СЛОЖНОЕ
СТРОЕНИЕ И СОДЕРЖИТ 12-18 МЛРД НЕРВНЫХ
КЛЕТОК И БОРОЗДАМИ ДЕЛИТСЯ НА НЕСКОЛЬКО ДОЛЕЙ
А теперь закройте глаза и коснитесь пальцами кончика носа. Получилось без особого труда, не так ли? Это при том, что в этом плавном действии было задействовано много разных мышц. За координацию, равновесие, нормальные движения спасибо мозжечку.
Сложнее, сложнее
Эмоции, такие эмоции. Без них наша жизнь была бы не такой счастливой (несчастной?). Внутренняя борьба, иногда заставляющая нас сделать то, о чем мы потом пожалеем. Знакомо? Благодарим лимбическую систему. Интересно что это такое? Чуть подробнее о ней (и ее частях).
Беспокоитесь, грустите? А может вам страшно? Это возможно благодаря миндалевидному телу (миндалине). Любопытный факт: с левой миндалиной бывает связано и чувство счастья, а вот у правой «настроение» плохое всегда.
Читайте материал по теме: Билл Гейтс и его синдром Аспергера
И наконец.
Итак, какова ее роль?
Читайте материал по теме: Что происходит с мозгом аутистов?
С лобной долей связана также наша способность к движению (благодаря моторной коре), чёткому и разборчивому письму, артикуляции.
Ассоциативные функции обеспечиваются теменной долей коры. Здесь располагаются области, отвечающие за осязание, чёткие, комбинированные целенаправленные движения, чтение, познавание предметов, явлений, их смысла и символического значения.
Бросается в глаза, что.
Наиболее сложные функции памяти и мышления не имеют чёткого расположения, в их реализации принимают участие различные области мозга.
Почему важно знать, как связаны функция и структура головного мозга?
Диагностика. Представьте: у человека сильно разболелась голова. Спустя несколько минут он уже не смог поднять правую руку, а его речь стала невнятной. У пациента ухудшилось зрение с одной стороны, тогда как офтальмолог патологию со стороны глаз не обнаружил. Или, например, человек перестал понимать обращённую к нему речь.
Читайте материал по теме: Как предотвратить инсульт?
Зная о том, какие отделы в головном мозге отвечают за ту или иную способность, можно предполагать место расположения патологического процесса.
Лечение и реабилитация. Предположим, что в результате повреждения участка головного мозга после инсульта у человека «выпала» какая-то функция. Значит ли это, что теперь она не вернётся? Нет, далеко не всегда.
Благодаря такому свойству мозга, как пластичность, возможно эту функцию восстановить. Говоря простыми словами, под пластичностью можно понимать способность других областей мозга брать на себя функцию повреждённой его части. Однако этим процессом нужно целенаправленно заниматься. Поэтому после инсульта больному бывает необходим курс нейрореабилитации, в процессе которого он заново учится говорить, ходить, обслуживать себя.
Нет. Приведённые выше описания взаимоотношений структуры и функции далеко не исчерпывающие: на деле всё гораздо сложнее и выходит далеко за рамки объёма небольшой статьи.
Зона мозга отвечающая за сон
Добавить в закладки
Вы сможете увидеть эту публикацию в личном кабинете
Добавить в закладки
Вы сможете увидеть эту публикацию в личном кабинете
Добавить в закладки
Вы сможете увидеть эту публикацию в личном кабинете
Добавить в закладки
Вы сможете увидеть эту публикацию в личном кабинете
Добавить в закладки
Вы сможете увидеть эту публикацию в личном кабинете
Добавить в закладки
Вы сможете увидеть эту публикацию в личном кабинете
Добавить в закладки
Вы сможете увидеть эту публикацию в личном кабинете
Добавить в закладки
Вы сможете увидеть эту публикацию в личном кабинете
Подпишитесь на нашу рассылку и получайте новости о последних проектах, мероприятиях и материалах ПостНауки
Мозг не отличает сон от яви
Происходящее во сне кажется нам реальным вплоть до пробуждения. А как воспринимает сновидения наш мозг? Исследователи из Института психиатрии Общества имени Макса Планка решили проверить, какие зоны коры активны в то время, когда мы видим сны. Узнать это оказалось непросто: ученым пришлось разыскать людей, владеющих техникой осознанных сновидений.
Когда нам снится, что мы бежим, едем или летим — воспринимает ли наш мозг эти действия как реальные? Казалось бы, ответ очевиден: вряд ли. Иначе мы бы, не просыпаясь, бегали, крутили педали под одеялом, а может быть, и освоили бы искусство левитации. Но вот немецкие исследователи из Института психиатрии Общества имени Макса Планка решили проверить этот, казалось бы, совершенно неоспоримый факт. Их заинтересовал вопрос: какие зоны активизируются в мозге в то время, когда мы совершаем какое-либо действие во сне?
Впрочем, говорят, что таких людей немало: почти каждому из нас хотя бы раз в жизни удавалось управлять своим сном. Другое дело, что немногие могут делать это осознанно. Однако есть люди, увлекающиеся подобными практиками: при помощи специальных техник и медитаций они тренируют сознание, чтобы смотреть сны «по заказу» и управлять своими действиями во время сновидения.
На призыв мюнхенских ученых откликнулись шестеро таких умельцев. Исследователи положили их спать в фМРТ-сканер. При появлении управляемого сна они должны были подать наблюдателям знак — за закрытыми веками пошевелить глазами. В самом же сне ученые попросили добровольцев сжать левую или правую руку — несложное движение, для выполнения которого наяву активизируются совершенно определенные зоны коры.
Увидеть управляемый сон удалось всего двум из шестерых участников. Но каково же было удивление ученых, когда во время сжимания руки во сне мозг активизировал те же самые участки, что и наяву! Получается, что сон — это не своеобразное «кино», которое мы смотрим каждую ночь, в противном случае, в работу включались бы только зоны зрительного анализатора.
Впрочем, работа мозга при «просмотре» сновидений не совсем идентична таковой наяву — иначе бы все мы стали лунатиками. Во сне молчит область мозга, отвечающая за принятие решений — и потому зоны моторной коры не активизируются. Исключением как раз становятся больные лунатизмом, или, выражаясь более научно, сомнамбулизмом. Этим расстройством страдают около 2 процентов населения земли, чаще всего оно встречается у детей и подростков — по-видимому, мозг некоторых из них не сразу обучается «правильно вести себя» во время сна и активизирует моторные зоны.
Лунатики встают с постели и ходят, не просыпаясь. В таком состоянии они порой могут совершать довольно сложные действия — перекладывать предметы, открывать двери, поливать цветы. Многие сомнамбулы способны даже ответить на несложный вопрос, вроде «Как тебя зовут?».
Лунатизм наблюдается во время медленной фазы сна — той же, на которой к нам приходит 80 процентов сновидений, кошмары, от которых мы просыпаемся в холодном поту. В этой же фазе сна люди разговаривают, а те, кто страдает ночным недержанием, мочатся в постель. Снохождение считается нервным расстройством, поскольку такой режим сна, конечно, нельзя считать нормальным — все-таки это состояние задумано природой как отдых.
К тому же, сомнамбулы подвергают себя опасности: некоторые из них вываливаются из окон, приняв их за двери, выходят на крышу или на оживленное шоссе. Разбудить лунатика трудно — в этой фазе сон у людей необычайно крепок. Родным, заставшим лунатика во время ночных хождений, рекомендуется аккуратно проводить его до постели. Благо, лунатики послушны: на команду, произнесенную уверенным тоном, их сознание откликается немедленным выполнением.
Известно, что склонность к лунатизму передается по наследству. В феврале этого года американские ученые нашли участок ДНК, отвечающий за склонность к развитию сомнамбулизма. Исследователи отыскали необычную семью, в которой целых девять человек были лунатиками. Причем их снохождение было столь частым и долгим, что нередко заканчивалось травмами, а один из них, ставший героем семейной легенды, умудрялся, не просыпаясь, надевать восемь пар носков.
Исследователям повезло и в том, что, несмотря на привычку к лунатизму, члены семьи отличались завидным долголетием и плодовитостью: в исследовании приняли четыре поколения родственников, всего 22 человека. Сделав анализ ДНК, полученной из слюны лунатиков и их родных, специалисты обнаружили в 20-й хромосоме специфический участок. Присутствие его копии в геноме с вероятностью в 50 процентов определяло, что в будущем человек станет лунатиком. Ученые решили продолжить исследование, чтобы определить, какой из 28 генов, входящих в данный участок, является виновником сомнамбулического расстройства.
Добавьте «Правду.Ру» в свои источники в Яндекс.Новости или News.Google, либо Яндекс.Дзен
Быстрые новости в Telegram-канале Правды.Ру. Не забудьте подписаться, чтоб быть в курсе событий.
Сон и старение I: «Часы в мозге» и влияние генов на ритм жизни
Сон и старение I: «Часы в мозге» и влияние генов на ритм жизни
Эпифиз вырабатывает «гормон сна» мелатонин ночью, а солнечный свет тормозит его образование. Мелатонин — главный регулятор циркадных ритмов, управляющих распорядком дня человека.
Автор
Редакторы
Новая неделя, новый день, новый год. Время жизни разбито на отрывки разной длительности, и все эти отрывки повторяются. Каждые несколько часов нам хочется есть. Каждый вечер мы ложимся спать. Каждые четыре недели организм женщины вырабатывает яйцеклетку. Большинство процессов, происходящих с нашим телом, циклично, и одни циклы завязаны на другие. И хотя старение организма периодическим процессом не назовёшь (ведь никто не молодеет!), его ход напрямую зависит от биоритмов человека, в частности, от цикла сна и бодрствования. Доказательства этому находятся и на уровне поведения, и на уровне отдельных органов, клеток и генов.
Старение и долголетие
Цикл статей, задуманных в рамках спецпроекта «биомолекулы» для фонда «Наука за продление жизни».
В этом цикле рассмотрим общие проблемы старения клеток и организмов, научные подходы к долголетию и продлению здоровой жизни, связь сна и старения, питания и продолжительности жизни (обратимся к нутригеномике), расскажем про организмы с пренебрежимым старением, осветим темы (эпи)генетики старения и анабиоза.
Конечно, феномен старения настолько сложен, что пока рано говорить о радикальных успехах в борьбе с ним и даже о четком понимании его причин и механизмов. Но мы постараемся подобрать наиболее интересную и серьёзную информацию о нащупанных связях, модельных объектах, разрабатываемых и уже доступных технологиях коррекции возрастзависимых нарушений.
Краткое содержание спецпроекта освещено в видеоролике «Стареть или не стареть? // Всё как у зверей». Подробности же узнаете из наших статей.
Следите за обновлениями!
Часы в мозге
Как показывает практика, механизмы смены сна и бодрствования можно объяснить даже детям — «„Проснись!“ — „Усни. “ — „Проснись!“ — „Усни. “ — „Проснись!“» [1]. — Ред.
У дрозофил нашли подобие «гена сна», что описано в статье «Бессонные ночи дрозофилы» [2]. Чисто теоретически это может привести к тому, что потребностью во сне можно будет управлять, но вряд ли мы это когда-то увидим. — Ред.
Есть предположение, что изначально (много миллионов лет назад) циркадные ритмы помогали организмам не умирать от кислорода, которого в тот момент в атмосфере стало аномально много для тогдашних обитателей планеты — «Прообраз биологических часов» [3]. — Ред.
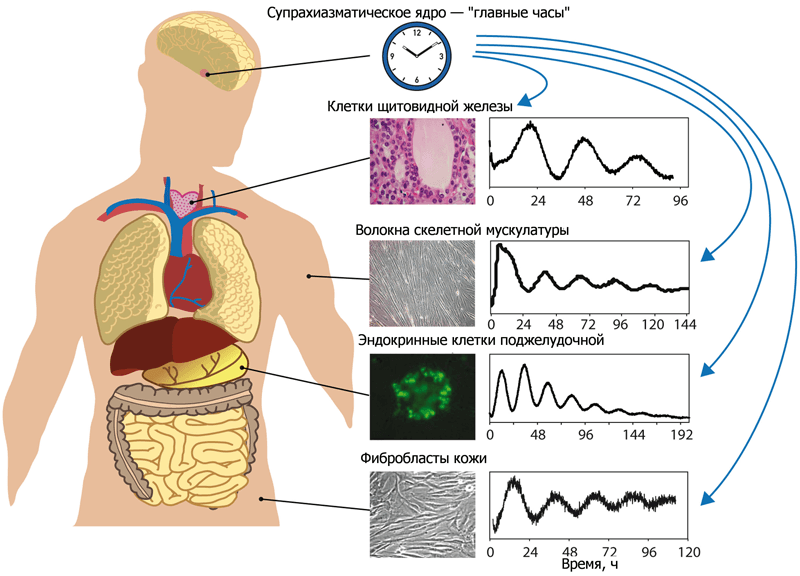
Рисунок 1. Влияние супрахиазматического ядра гипоталамуса на работу различных клеток организма. Функционирование клеток всех типов тканей подчиняется центральному ритму, который задаёт супрахиазматическое ядро гипоталамуса. Оно «следит» за тем, чтобы сигналы от нервной и эндокринной систем приходили к клеткам в одно и то же время — фактически, синхронизирует их. Кстати, то же можно сделать и вне организма: выращивая в культурах несколько образцов различных тканей человека, можно эти культуры синхронизировать, если имитировать сигналы SCN. Такая синхронизация активности культур различных типов клеток одного и того же человека представлена на графиках.
В ходе исследований посмертных срезов мозга здоровых пожилых людей выяснилось, что с возрастом нейроны SCN дегенерируют. Изменяется и структура LC. Кроме того, активность лобных долей коры значительно падает с возрастом (и степень снижения этой активности напрямую отражается на интеллекте), что показано в исследованиях фМРТ [4]. Всё это приводит к тому, что со временем у людей исчезают острые пики активности при бодрствовании. То есть пожилые, конечно, бодрствуют, но внимательность и скорость мышления у них не так хороши, как раньше. Вероятно, причина этого — постепенное ухудшение работы мозговых регуляторов сна и бодрствования.
У пожилых по сравнению с молодыми эффективность сна снижена. С этим может быть связана старческая сонливость, возникающая даже тогда, когда человек определённо выспался. Судя по всему, возрастное падение качества сна не вызвано какими-то конкретными патологиями, это просто часть обычного процесса старения. Впрочем, так ли неизбежно само старение, вопрос.
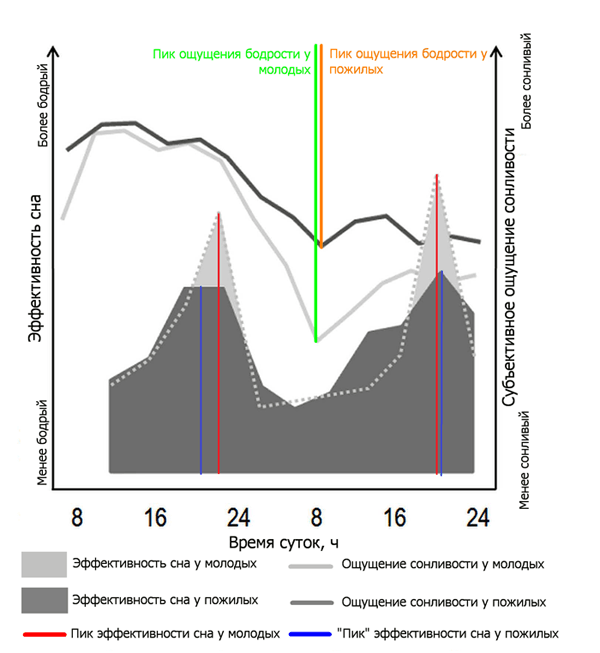
Кроме того, старые хуже переносят вынужденный пропуск сна. Это показали эксперименты, в ходе которых 12 мужчин возрастом 21–31 год и 11 мужчин возрастом 61–70 лет не спали 40 часов (рис. 2). У пожилых субъективное ощущение сонливости было сильнее, чем у молодых, да и внимание из-за недосыпа падало заметнее [5].
Другой эксперимент с такой же длительностью провели в 2005 году [6]. Его результаты тоже представлены на рисунке 2 (закрашенные серым области). В нём двум группам участников-мужчин (опять пожилым и молодым) нужно было в течение 40 часов то спать по 75 минут, то бодрствовать по 150 минут, притом делать это по расписанию. Такой искусственный режим должен был выявить, насколько сон у людей одной возрастной группы более эффективен, чем у испытуемых из другой группы. Нетрудно догадаться, что молодые во время эксперимента и после него чувствовали себя лучше, чем пожилые, потому что лучше высыпались.
Рисунок 2. Субъективное восприятие качества сна и бодрствования у молодых и пожилых мужчин во время 40-часового эксперимента по лишению сна [5], а также эффективность сна во время эксперимента с множеством эпизодов сна [6]. Пожилые раньше начинают чувствовать сонливость, и субъективно она проявляется сильнее (тёмно-серая линия). Молодые более устойчивы к депривации сна (светло-серая линия). Кроме того, субъективно сон молодых (светло-серые закрашенные области) более эффективен, чем сон пожилых (тёмно-серые закрашенные области).
«Гены циркадных ритмов» и старение
Работа любого органа — это, в конечном счёте, работа его генов. Наши «внутренние часы» — не исключение. В супрахиазматическом ядре экспрессируется ряд генов, малоактивных в других частях мозга и тела вообще. Среди таких генов BMAL1 (он же MOP3 и ARNT3), CLOCK и NPAS2 [7], [8]. Эти гены были выявлены в исследованиях с помощью нокаутных мышей — таких, которым методами генной инженерии нарушили работу одного или нескольких генов.
Как правило, продолжительность жизни у грызунов с одним или несколькими выключенными «генами периодичности» снижена. В частности, мыши с неработающим BMAL1 живут меньше своих собратьев. Под конец жизни у них проявляются все характерные признаки старения: их органы уменьшаются в размерах, теряется мышечная масса и подкожный жир, развивается старческая катаракта, повышается содержание активных форм кислорода в тканях [9]. При постоянной нехватке белков BMAL1 и CLOCK ухудшается память, снижается интеллект: животные хуже обучаются и быстрее забывают новую информацию [10].
BMAL1 и CLOCK действуют по-разному: если «выключить» работу гена CLOCK, не затрагивая BMAL1, жизнь мышей претерпевает менее глобальные изменения. Средний срок жизни грызунов без CLOCK на 15% короче, чем у животных дикого типа, а преждевременное старение проявляется у них только в изменении структуры кожи и развитии катаракты [11].
Вот один из примеров связи циркадных ритмов с обменом веществ в целом: «Найдена связь между обменом веществ и циркадным ритмом» [12].
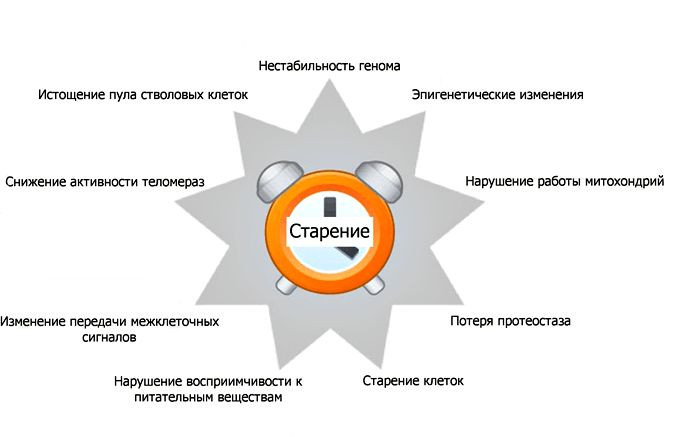
Рисунок 3. Примеры проявлений старения на клеточном уровне. Подробное объяснение этих проявлений дано ниже в тексте в виде нумерованного списка.
Исследования обычно проводятся на больших группах животных, и данные по этим животным усредняются. Но мы-то помним, что каждый организм имеет свой уникальный геном, и от того, как гены в его составе взаимодействуют между собой, зависит очень многое. У двух мышей может быть нарушена работа одного и того же CLOCK, но на уровне отдельных органов и организма в целом это нарушение проявится у них совершенно по-разному. Да даже если с вариантами генов всё в порядке, два организма не будут стариться одинаково. Дело в том, что роль в силе и характере изменений сна с возрастом играет и генотип конкретного организма. Это было подтверждено исследованиями на мышах [23], [24], в которых качество сна грызунов оценивали по элетроэнцефалограммам, а также смотрели, как с возрастом у этих грызунов ухудшается зрение.
У грызунов линии C57BL/6 чаще других с возрастом развивается катаракта, а значит, почти пропадает зрение. Видимо, поэтому под старость (в возрасте примерно год) эти сумеречные животные всё более активны в светлое время суток и всё менее активны в темноте. Кроме того, пожилые C57BL/6 бодрствуют дольше остальных, а AKR/J дольше всех спят. Больше всего времени в стадии REM-сна проводят мыши линии DBA/2J, а меньше всего — AKR/J. Если годовалым мышам этих трёх линий некоторое время мешать спать, а потом дать им возможность выспаться, то быстрее всех к своему обычному режиму возвращаются грызуны C57BL/6.
Сон и метаболизм
Мы выяснили, как нарушение работы «генов циркадных ритмов» влияет на состояние отдельных клеток. А как на них действует нарушения сна, столь частые в преклонном возрасте?
Хотя сон считается временем покоя, во время сна очищение нейронов от «отработанных» продуктов обмена веществ происходит быстрее, чем при бодрствовании [26]. Кстати, ночью очищается не только нервная система. Во время сна также усиливается или ослабевает экспрессия ряда генов. В тканях лёгких экспрессия 3% генов различается во сне и при бодрствовании. В тканях сердца таких «сон-зависимых» генов 6%. Во время сна содержание маркеров клеточного стресса в тканях лёгких, сердца и мозга снижено [27].
Возможно, одна из функций сна — избавление организма от отработанных метаболитов и общее восстановление клеток после стресса. Если это предположение окажется верным, оно сможет объяснить некоторые факты. Например, известно, что независимо от национальности у женщин 46–57 лет, имеющих частые жалобы на качество сна, особенно высок риск метаболического синдрома [28]. Впрочем, последнее может быть связано с тем, что в дополнительные часы бодрствования эти женщины едят [29]. А значит, они потребляют больше калорий в сутки, чем женщины без проблем со сном. В пользу этой гипотезы свидетельствует то, что экспериментальное нарушение сна не вызывало у крыс метаболического синдрома [30].
По данным эпидемиологических исследований, депривация (ограничение времени) сна повышает вероятность дислипидемии, диабета 2 типа и нетолерантности к глюкозе (таб. 1).
| Первый автор статьи, ссылка | Год | Число участников | Продолжительность исследования | Результаты |
|---|---|---|---|---|
| Chaput et al. [32] | 2007 | 740 | 3 года | Регулярный сон длительностью менее 6 часов вызывает нарушение толерантности к глюкозе. |
| Mallon et al. [33] | 2005 | 2663 | 12 лет | У мужчин частые пробуждения и короткий сон связаны с повышенной вероятностью диабета. |
| Nilsson et al. [34] | 2004 | 6599 | 14,8 ± 2,4 года | Нарушения сна повышают риск развития диабета. |
| Tuomilehto et al. [35] | 2008 | 2800 | 2 года | Слишком короткий (≤6 ч) или слишком длинный (≥8ч) сон повышают вероятность развития диабета 2 типа у женщин среднего возраста. У мужчин аналогичного эффекта не нашли. |
| Meisinger et al. [36] | 2005 | 8300 | 11 лет | У людей обоих полов сложности с поддержанием сна (частые просыпания и т.п.) повышают риск развития диабета 2 типа. |
| Hayashino et al. [37] | 2007 | 6509 | 6 лет | У взрослых без серьёзных проблем со здоровьем нарушения засыпания связаны с повышенным риском диабета. |
| Kawakami et al. [38] | 2004 | 2649 | 8 лет | Нарушения сна связаны с повышением риска диабета в 2-3 раза. |
| Choi et al. [39] | 2008 | 4222 | 1 год | И слишком короткий, и слишком длинный сон ассоциируются с повышенным риском метаболического синдрома. |
| Gangwisch et al. [40] | 2007 | 8992 | 10 лет | Кратковременный сон может быть важным фактором риска диабета. |
| Xu et al. [41] | 2010 | 10143 | 10 лет | Короткий ночной сон и частый дневной сон связаны с проявлением диабета. |
| Rafalson et al. [42] | 2010 | 1455 | 6 лет | Короткий ночной сон связан с нарушением содержания глюкозы в крови натощак, вызванным резистентностью к инсулину. |
| Yaggi et al. [43] | 2006 | 1709 | 18 лет | И слишком короткий, и слишком длинный сон повышают риск развития диабета. |
| Hall et al. [44] | 2008 | 1214 | Одномоментное исследование | Продолжительность сна связана со степенью риска метаболического синдрома. |
| Facco et al. [45] | 2010 | 189 | В течение беременности | Малая продолжительность сна связана с нарушением толерантности к глюкозе во время беременности. |
| Qui et al. [46] | 2010 | 1290 | В течение беременности | Гестационный диабет (диабет беременных) и нарушение толерантности к глюкозе чаще развиваются у тех, кто мало спит. |
Помимо нарушений метаболизма, ошибок репликации и повышенным по сравнению с нормой процентом гибнущих клеток [30], депривация сна может повлечь за собой негативные последствия для иммунной системы. У пациентов с постоянным недосыпом днём в крови повышается содержание маркеров воспаления — фактора некроза опухолей (TNF), интерлейкинов 1 и 6, а также кортизола [31], [47]. А ведь воспаление идёт рука об руку с повышенным риском множества заболеваний, начиная от инсульта и заканчивая болезнью Альцгеймера. Например, при последней клетки микроглии (это макрофаги в мозге) выделяют заметные количества интерлейкинов 12 и 23 — одних из важнейших сигналов воспаления. В норме этого, разумеется, не происходит, ведь ни болезни Альцгеймера, ни воспаления нет. Судя по всему, команду микроглии вырабатывать факторы воспаления даёт сам бета-амилоид. Далее, при болезни Альцгеймера астроциты (разновидность глиальных клеток, питают и поддерживают нейроны, направляют их рост у зародышей) становятся восприимчивыми к IL-12 и IL-23 (опять же, в норме такого не наблюдается.) Отложения бета-амилоида увеличиваются в размерах, клеток астроглии становится всё больше, а нейронов рядом с ними — всё меньше [48]. Если снизить выработку IL-12 и IL-23 в клетках глии, патология замедлит своё развитие.
Во взаимосвязях воспаления, выделения интерлейкинов и работы астроцитов при болезни Альцгеймера ещё предстоит разобраться, но уже сейчас ясно, что такие взаимосвязи существуют. На самом деле, подобных корреляций выявили уже немало. А о связи нарушений сна и различных заболеваний (нервных, и не только) будет отдельная статья.