активный хлор что это такое
Концентрация хлора в воде: общего, остаточного, активного, свободного, связанного
Химический элемент хлор (Cl) относится к группе галогенов и в чистом виде представляет собой ядовитый газ жёлто-зелёного цвета. Хлор тяжелее воздуха и обладает характерным резким удушающим запахом.
Хлор в природе и жизни человека
Ввиду своей чрезвычайно высокой химической активности, в естественной среде хлор в чистом виде не встречается. Наибольшие запасы этого элемента сосредоточены в солях морской воды, содержание хлора в которой достигает 19 грамм на литр.
Хлор выполняет важные функции в жизнедеятельности растений и животных. В организме человека хлор обеспечивает поддержание кислотно-основного равновесия (КОР) плазмы крови, также он содержится в лимфе и входит в состав желудочного сока. Основная часть ионов хлора поступает в организм человека в виде хлорида натрия, содержащегося в пище.
Свободный и связанный хлор
Хлор, введённый в воду в целях обеззараживания, немедленно вступает в реакцию с водой и содержащимися в ней компонентами.
Исходя из более высокой химической активности хлорноватистой кислоты и гипохлоритов, хлор, входящий в состав HClO и её солей, а также ту часть элементарного хлора, который не успел вступить в реакцию, принято называть свободным или свободным активным хлором. К хлору, входящему в состав гипохлоритов иногда применяют термин «потенциально свободный хлор». Соответственно хлор, принявший участие в окислении и вошедший в состав органических и неорганических хлораминов, называют связанным, или связанным активным хлором.
Данные определения носят условный характер, так как во всех соединениях, хлор, строго говоря, связан.
Общий, активный и остаточный хлор
Хлор в воде принимает активное участие в реакциях окисления. В результате реакций, в воде остаётся некоторое его количество. Суммарное количество хлора, остающееся в воде в виде различных соединений, принято называть общим хлором. Общий хлор иногда называют также общим остаточным или остаточным активным хлором. Таким образом, используемая терминология не отличается единообразием.
В состав общего хлора входит свободный и связанный активный хлор.
Область применения хлора и хлорамина
Хлор широко применяется в различных отраслях промышленного производства и в быту. Кроме общеизвестной функции хлора, как средства для обеззараживания воды в водопроводах питьевого назначения и бассейнах, существуют другие сферы его применения:
Хлорамин относится к неорганическим соединениям – хлоропроизводное аммиака. Хорошо растворяется в воде. Используют хлорамин для следующих целей:
Соединения хлора входят в состав отбеливателей для белья. Роль хлора в процессе отбеливания заключается в том, что при его вступлении в реакцию с водой высвобождается активный кислород, который и обеспечивает отбеливание.
Сточные и природные воды
Природные воды Земли образуют её естественную гидросферу и подразделяются на поверхностные и подземные. Поверхностными водами заполнены реки, болота, озёра, моря, а также каналы и водохранилища. Подземные воды содержатся в полостях и порах земных недр.
Сточные воды по источникам их происхождения делятся на несколько групп:
Стоки хозяйственно-бытового происхождения загрязнены главным образом органикой, а также содержат моющие средства и бытовую химию. Ливневые воды растворяют загрязнения, находящиеся на поверхности почвы, поэтому их состав может быть разнообразным. В стоках животноводческих ферм содержится высококонцентрированная органика, а поливная вода несёт с полей удобрения и ядохимикаты.
Нормы содержания в питьевой воде
Действующие санитарные нормы и правила устанавливают допустимые пределы концентрации остаточного хлора, содержащегося в питьевой водопроводной воде на уровне 0,3-0,5 мг/л. Наличие остаточного активного хлора считается необходимым для нейтрализации загрязнений, которые могут попасть в воду по пути её движения от очистных сооружений до потребителя. Внутренние поверхности распределительных трубопроводов могут служить местом активного размножения патогенной микрофлоры.
Таким образом, при снижении концентрации активного остаточного хлора в воде ниже допустимого уровня 0,3 мг/л не гарантируется полное её обеззараживание.
Предельно допустимая концентрация
Установленная СанПиН предельная концентрация остаточного хлора в водопроводах питьевого назначения и бассейнах составляет 0,5 мг/л. Превышение установленной нормы приводит к изменению органолептических свойств воды – снижению её прозрачности и ухудшению вкусовых качеств. Кроме этого, превышение предельно допустимой концентрации по хлору может оказывать негативные воздействия на здоровье человека, вызывая:
Кроме этого, доказаны канцерогенные свойства некоторых хлорорганических соединений, которые могут образовываться в ходе реакции хлора с определёнными органическими загрязнителями.
Обеззараживание сточных вод
Сточные воды содержат большое количество органических веществ, которые создают благоприятную среду для развития бактерий, в том числе патогенных. По этой причине обеззараживание сточных вод является обязательной процедурой, обеспечивающей сохранение экологии естественных водоёмов, воздуха и почвы.
Хлорирование относится к наиболее распространённому способу дезинфекции сточных вод. Концентрация хлора, необходимая для полного обеззараживания сточных вод зависит от технологии, применяемой на очистных сооружениях. СНиП 2.04.03-85 устанавливает следующие значения дозы вводимого хлора:
Хлорирование
Хлорирование питьевой воды осуществляется на станциях водоподготовки, куда хлор доставляется в сжиженном виде в специальных контейнерах. Для получения газообразного хлора, который применяется для обеззараживания воды, сжиженный газ пропускается через специальные испарительные устройства. Испарители представляют собой большие цилиндрические ёмкости, установленные вертикально, внутри которых расположены змеевики.
Применение газообразного хлора для обеззараживания воды имеет ряд преимуществ:
Опасна ли водопроводная вода
Водопроводная вода, поступающая в наши квартиры, считается питьевой. Это значит, что в случае соответствия её качества действующим санитарным нормам и правилам, она должна быть полностью пригодна к употреблению без какой-либо дополнительной очистки. Но это в теории. На практике всё не совсем так. Достаточно вспомнить один из распространённых в советское время лозунгов: «Не пей сырую воду!»
Водопроводная вода может быть опасна по нескольким причинам:
Объективный показатель качества водопроводной воды – это лабораторный анализ, проводимый на регулярной основе.
Альтернативные способы
Хлорирование – не единственный метод обеззараживания воды. Среди альтернативных способов дезинфекции воды можно выделить следующие:
Ультрафиолетовое обеззараживание. Принцип этой технологии заключается в облучении водного потока ультрафиолетом. Жёсткое облучение ультрафиолетового спектра способно убивать болезнетворные микроорганизмы. Это свойство УФ-лучей широко используется для дезинфекции помещений лечебных учреждений, предприятий общепита.
Преимущество ультрафиолетового способа обеззараживания перед химическими методами заключается в том, что в воду не вводят реагенты, которые сами по себе могут быть вредными. Однако очищенная таким способом вода может быть вновь загрязнена при транспортировке по водопроводу. Кроме этого, оборудование для УФ – очистки достаточно дорогое и энергоёмкое. Наиболее целесообразно устанавливать такие системы непосредственно у потребителя.
Озонирование. В основе метода – сильные окислительные свойства озона, который вырабатывается специальными установками из воздуха.
Озон является превосходным дезинфектором – не существует устойчивых к озону бактерий, грибков и вирусов. Действие озона происходит в течение нескольких секунд. Недостатки у озонирования те же, что и УФ-метода – высокая стоимость оборудования и низкая остаточная способность к обеззараживанию.
Оценка эффективности
Эффективность применяемой системы очистки воды оценивается по критериям качества, которым соответствует вода, прошедшая ту или иную систему очистки. К таким качествам относятся:
Контроль качества воды
Качество питьевой воды проверяется путём регулярного забора проб и их лабораторного анализа. Методика отбора проб, регулярность их проведения, а также перечень контролируемых показателей качества регламентированы СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества».
Кто осуществляет
Контроль качества питьевой воды осуществляется лабораториями предприятий, эксплуатирующих системы централизованного водоснабжения. Мероприятия по контролю качества выполняются на основании утверждённых рабочих программ.
Методы определения хлора в воде
Для определения содержания хлора в воде используются анализаторы хлора, использующие различные методы измерения:
Фотоколориметрический метод основан на окрашивании раствора при взаимодействии общего хлора со специальными реагентами. Концентрация хлора определяется интенсивностью окраски раствора и её соответствием образцовой цветовой шкале.
В основе йодометрического метода лежит взаимодействие йодида с активным хлором, в результате которого выделяется йод. Титрование йода производится тиосульфатом натрия. По йодометрическому принципу работает анализатор ВАКХ-2000С.
Хемилюминесцентный метод основан на свойстве люминола излучать определённое свечение при воздействии на него хлора в щелочной среде. Концентрация хлора определяется интенсивностью хемилюминесценции. Данный метод реализуется в анализаторе хлора Флюорат-АС-2.
Электрохимические анализаторы измеряют потенциалы электродов, погруженных в исследуемый раствор, которые отображают электрохимические процессы, протекающие в жидкости. На этом методе основаны такие анализаторы как АСХВ/М1031, АХВ-М3, КХВ-2 и другие.
Правовая ответственность
Организации, осуществляющие питьевое водоснабжение обязаны принимать все меры обеспечения потребителей водой надлежащего качества. Оказание услуг этого типа с нарушением требований санитарных правил влечёт за собой административную ответственность, предусмотренную частью 2 статьи 14.4 КоАП РФ. Статья 6.5 того же Кодекса предусматривает ответственность за нарушение санитарно-эпидемиологических требований к воде, правил хозяйственно-бытового водоснабжения.
Гипохлорит: что это такое, применение
Новости
Растворы гипохлорита натрия применяются как дезинфекция и обеззараживание воды около 100 лет. Многолетняя практика использования этого эффективного средства для обработки воды, показывает, что применять его можно при решении задач различного рода, связанных с водоподготовкой:
Использование растворов гипохлорита натрия для обработки питьевой воды предпочтительно на стадии предварительного окисления и для стерилизации воды перед подачей ее в распределительную сеть. Обычно в систему водоочистки растворы вводят после разбавления примерно в 100 раз. При этом, помимо снижения концентрации активного хлора, снижается также величина Ph (c 12-13 до 10-11), что способствует повышению дезинфицирующей способности раствора.
Гипохлорит натрия широко применяется: для обработки бытовых и промышленных сточных вод; для разрушения животных и растительных микроорганизмов; устранения запахов; обезвреживания промышленных стоков, в том числе содержащих цианистые соединения. Он может быть использован также для обработки воды, содержащей аммоний, фенолы и гуминовые вещества.
Гипохлорит натрия также используется для обезвреживания промышленных стоков от цианистых соединений; для удаления из сточных вод ртути и для обработки охлаждающей конденсаторной воды на электростанциях.
Основные свойства гипохлорита натрия
Гипохлорит натрия (натриевая соль хлорноватистой кислоты) – NaClO, получают хлорированием водного едкого натра (NaOH). Промышленностью выпускается в виде водных растворов различной концентрации. Малоконцентрированные растворы получают электролизом раствора хлорида натрия (NaCl) в специальных электрохимических установках, как правило, непосредственно у потребителя.
Дезинфицирующее действие основано на том, что при растворении в воде он точно так же, как хлор, образует хлорноватистую кислоту, которая оказывает непосредственное окисляющее и дезинфицирующее действие.
NaClO + H2O→← NaOH + HClO
Существуют растворы гипохлорита натрия различных марок.
Основные физико-химические показатели растворов гипохлорита натрия выпускаемых в РФ:
Растворы гипохлорита натрия различных марок применяют:
Необходимо отметить, что для изготовления растворов гипохлорита натрия марок А и Б по [3] и растворов марки А по [4] не допускается применение абгазного хлора от хлоропотребляющих органических и неорганических производств, а также едкого натра, полученного ртутным методом.
Растворы марки Б по [4] получают из абгазного хлора органических и неорганических производств и диафрагменного или ртутного едкого натра.
Журнал «Сырье и Упаковка»
Текущий номер
Ближайшие выставки
Партнеры
Гипохлориты и их применение в средствах бытовой химии
30.03.2020
| Д. А. Меркулов, к.х.н., зав. кафедрой фундаментальной и прикладной химии, ФГБОУ ВПО «Удмуртский государственный университет», г. Ижевск |
Введение
Гипохлоритами называют соли хлорноватистой кислоты HClO. Наиболее распространенными из них являются гипохлорит натрия, гипохлорит кальция и гипохлорит калия. Гипохлориты широко применяются для обеззараживания питьевой воды, отбеливания, дегазации и дезинфекции. Гипохлориты являются одними из самых важных химических соединений.
| Систематическое наименование | Традиционное название | Хим. формула | CAS № | М, г/моль |
|---|---|---|---|---|
| Гипохлорит натрия | Хлорноватистокислый натрий, лабарракова вода (гипохлорит натрия в смеси с хлоридом натрия и гидроксидом натрия) | NaClO | 7681–52–9 | 74,44 |
| Гипохлорит калия | Хлорноватистокислый калий, жавелевая вода (гипохлорит калия в смеси с гидрокарбонатом калия и хлоридом калия) | KClO | 7778–66–7 | 90,55 |
| Гипохлорит кальция | Хлорноватистокислый кальций, хлорная известь (гипохлорит кальция в смеси с хлоридом кальция, оксихлоридом кальция и гидроксидом кальция) | Ca(ClO) 2 | 7778–54–3 | 142,98 |
История открытия
В 1774 г. шведский химик Карл Вильгельм Шееле получил хлор (Cl 2 ) в результате взаимодействия оксида марганца(IV) MnO 2 и соляной кислоты (HCl). Позже, в 1785 г. французский химик Клод Луи Бертолле обнаружил, что водный раствор газообразного хлора («хлорная вода»), содержащий хлорноватистую и хлороводородную кислоты, может отбелить белье, и сообщил о своих выводах Французской академии наук.
Cl 2 + H 2 O = HClO + HCl
Знания об отбеливающих свойствах хлора были незамедлительно использованы Джеймсом Уаттом на текстильной фабрике в Глазго. Несмотря на то, что отбеливание с использованием хлора был значительно эффективнее традиционных способов отбеливания солнечным светом, слабыми растворами кислот и щелочей, применение хлора ограничивалось его токсичностью и разрушающим действием на ткани. Для стабилизации раствора газообразного хлора в воде и безопасности его применения, в 1787 г. на Парижском предприятии Societe Javel хлор стали пропускать через водный раствор карбоната калия (поташа)
Cl 2 + K 2 СO 3 = 2KHCO 3 + KClO + KCl.
Глава предприятия Леонард Альбан назвал новый продукт «Eau de Javel» («жавелевая вода»), и вскоре белильная жидкость стала популярной во Франции и Англии.
В 1820 г. француз Антуан Лабаррак усовершенствовал способ получения отбеливателя, заменив поташ на более дешевый гидроксид натрия (каустическую соду). Полученный раствор гипохлорита и хлорида натрия получил название «Eau de Labarraque» («лабарракова вода»).
Cl 2 + 2NaOH = NaClO + NaCl + H 2 O.
Широкое применение гипохлоритов для обеззараживания питьевой воды и дезинфекции стало возможным гораздо позже, в начале XX века, благодаря развитию промышленного производства хлора электролизом поваренной соли.
Физические свойства
Гипохлориты встречаются нам преимущественно в виде водных растворов, хотя некоторые из них можно выделить в твердом виде. Так, известен безводный гипохлорит натрия, который представляет собой неустойчивое бесцветное кристаллическое вещество. Из кристаллогидратов наиболее устойчивой формой является NaClO×5H 2 O. Это соединение представляет собой белые или бледно-зеленые ромбические кристаллы, расплывающиеся на воздухе. При нагревании пентагидрата гипохлорита натрия до температуры 24,4°С, он плавится. Кристаллогидрат NaClO×2,5H 2 O плавится при температуре 57,5°С. Моногидрат крайне неустойчив и разлагается выше 60°С, при более высоких температурах разложение протекает со взрывом.
Таблица 2. Плотности и температуры замерзания водных растворов гипохлорита натрия.
В отличие от гипохлорита калия, известного только в растворах, гипохлорит кальция можно выделить в форме бесцветных кристаллов, устойчивых в сухой атмосфере без углекислого газа. Из водных растворов гипохлорит кальция можно выделить в виде кристаллогидратов Ca(ClO) 2 ×2H 2 O, Ca(ClO) 2 ×3H 2 O, Ca(ClO) 2 ×4H 2 O.
Кислотно-основное равновесие между хлорноватистой кислотой и гипохлорит-ионом описывается обратимой реакцией с константой равновесия Ka = 2,63×10 –8 при 20°С.
Используя константу равновесия Ka, можно рассчитать мольное долевое распределение хлорноватистой кислоты и гипохлорит-ионов в зависимости от рН (рис.1).
Данные свидетельствуют, что при подкислении растворов гипохлоритов увеличивается доля неустойчивой хлорноватистой кислоты. При рН 7,58 существуют преимущественно гипохлорит-ионы.
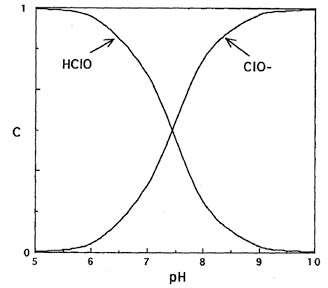
Рис. 1. Мольное долевое распределение хлорноватистой кислоты и гипохлорит-ионов в зависимости от кислотности среды.
Химические свойства
Гипохлориты являются неустойчивыми соединениями, легко разлагающимися с выделением кислорода. Разложение твердых гипохлоритов натрия и кальция можно представить уравнениями
2NaClO = 2NaCl + O 2 ↑ и 2Сa(ClO) 2 = СaCl 2 + O 2 ↑.
Процессы при комнатной температуре происходят медленно, а при нагревании могут протекать со взрывом. Параллельно реакциям, сопровождающимся образованием хлоридов и свободного кислорода, могут протекать реакции диспропорционирования
Разложение гипохлоритов в водных растворах зависит от кислотности раствора и его температуры. В сильнокислых средах при рН ≤ 3 хлорноватистая кислота при комнатной температуре разлагается до хлора и кислорода
4HClO = 2Cl 2 ↑ + O 2 ↑ + 2H 2 O.
Если при подкислении используется соляная кислота или в растворе присутствуют хлориды, образование кислорода не происходит
HClO + HCl = Cl 2 ↑ + H 2 O.
Хлорноватистая кислота очень слабая, поэтому она может быть вытеснена из раствора ее солей действием углекислого газа
ClO – + CO 2 + H 2 O = HCO 3 – + HClO.
В слабокислых и нейтральных средах при 3 2 ↑.
В нейтральных и щелочных растворах имеет место конкурирующая реакция образования хлоридов и хлоратов
При комнатной температуре реакция диспропорционирования протекает медленно, но при температурах выше 70°С эта реакция становится преобладающей.
В щелочных средах при рН > 7,5 в растворах преобладают гипохлорит-ионы, разлагающиеся следующим образом:
Около 95% от общего количества гипохлорит-ионов разлагается в результате последовательных реакций (1) и (2), причем реакция (1) является самой медленной (лимитирующей) и определяет общую скорость процесса. Реакция (3) не является основной, но отвечает за выделение кислорода, количество которого может быть значительным.
В присутствии некоторых ионов металлов, например, меди, никеля, кобальта наблюдается каталитическое разложение гипохлорит-ионов. Ионы железа обладают слабым каталитическим действием и являются сокатализаторами в сочетании с другими ионами металлов. В простейшем случае, при содержании ионов меди(II) в растворе в концентрации 1мг/кг порядки гомогенной реакции по гипохлориту и по меди(II) равны единице.
Гетерогенный катализ металлами и их нерастворимыми соединениями, является сложным и плохо воспроизводимым. Из нерастворимых катализаторов наибольшее мешающее влияние оказывает никель и его оксиды, которые попадают в растворы гипохлоритов при их контакте с легированными никелевыми сталями, используемыми для изготовления трубопроводов и резервуаров.
На константы скорости реакций (1)-(3) большое влияние оказывает ионная сила растворов. Высокие концентрации электролитов уменьшают константы скорости реакций и обеспечивают разумную стабильность при хранении растворов электролитов. Увеличение концентрации гипохлорит-ионов, напротив, уменьшает их стабильность в водных растворах. На рис. 2 показан феномен «кривой пересечения». Растворы гипохлорита натрия с концентрацией 9% и 5% при хранении разлагаются настолько, что через 50 недель показывают одинаковую концентрацию вещества, а через 100 недель первоначально более концентрированный раствор содержит гипохлорит-ионов меньше, чем разбавленный.
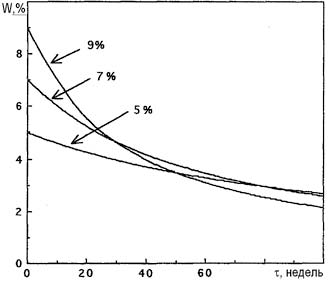
Рис. 2. Разложение гипохлорита натрия различных концентраций при 30°С.
Повышение температуры способствует ускорению процессов разложения гипохлоритов, поэтому целесообразно хранить растворы гипохлоритов в прохладном месте для обеспечения срока годности (рис. 3).

Рис. 3. Влияние температуры на разложение 5%-ного раствора NaClO.
Для стабилизации водных растворов гипохлоритов, а так же продуктов на их основе, каждый производитель применяет собственные методы, которые редко публикуются в виде статей. Однако известны некоторые запатентованные методы, которые, не претендуя на полноту, можно представить следующим списком:
Направление окислительно-восстановительных процессов с участием гипохлорит-ионов и хлорноватистой кислоты обусловлены значениями стандартных электродных потенциалов полуреакций в водной среде:
2HClO + 2H + + 2e – = Cl 2 ↑ + 2H 2 O, E° = 1,630 В,
HClO + H + + 2e – = Cl – + H 2 O, E° = 1,500 В.
в нейтральной и щелочной среде
Таким образом, гипохлорит-ионы и хлорноватистая кислота обладают выраженными окислительными свойствами, причем их окисляющая способность в кислой среде значительно выше, чем в нейтральной и щелочной средах.
Дезинфицирующее действие
Гипохлориты являются одними из лучших антибактериальных средств. Они убивают микроорганизмы очень быстро даже при очень низких концентрациях.
Наивысшее бактерицидное действие гипохлоритов проявляется в нейтральной среде, когда концентрации хлорноватистой кислоты и гипохлорит-ионов приблизительно равны (рис. 1). Образующиеся при разложении гипохлоритов активные частицы (атомарный кислород и хлор) обладают высоким биоцидным действием. Они уничтожают микроорганизмы, взаимодействуя с биополимерами в их структуре, способными к окислению. Аналогичным образом, например, действуют клетки человека нейтрофилы, гепатоциты и др., которые синтезируют хлорноватистую кислоту и сопутствующие высокоактивные радикалы для борьбы с микроорганизмами и чужеродными субстанциями.
Бактерицидная активность гипохлоритов настолько велика, что они способны привести к гибели дрожжеподобных грибов, вызывающих кандидоз, Candida albicans, в течение 30 секунд при действии 5,0 – 0,5%-го гипохлоритного раствора. Патогенный Enterococcus faecalis погибает через 30 секунд после обработки 5,25%-ым раствором и через 30 минут после обработки 0,5%-ым раствором. Грамотрицательные анаэробные бактерии, такие как Porphyromonas gingivalis, Porphyromonas endodontalis и Prevotella intermedia, погибают в течение 15 секунд после обработки 5,0 – 0,5%-м раствором гипохлорит-ионов.
Несмотря на высокую биоцидную активность гипохлоритов, некоторые потенциально опасные простейшие организмы, например, возбудители лямблиоза или криптоспоридиоза, к сожалению, устойчивы к его действию.
При помощи гипохлорит-ионов можно успешно обезвреживать различные токсины (табл. 3).
Таблица 3. Результаты инактивации токсинов при 30-минутной экспозиции различных концентраций гипохлорита натрия («+» – токсин инактивирован; «–» – токсин остался активен).
| Токсин | 2,5% NaClO + 0,25 н. NaOH | 2,5% NaClO | 1,0% NaClO | 0,1% NaClO |
|---|---|---|---|---|
| Т-2 токсин | + | – | – | – |
| Бреветоксин | + | + | – | – |
| Микроцистин | + | + | + | – |
| Тетродотоксин | + | + | + | – |
| Сакситоксин | + | + | + | + |
| Палитоксин | + | + | + | + |
| Рицин | + | + | + | + |
| Ботулотоксин | + | + | + | + |
Методы анализа
Качественными реакциями на гипохлорит-ион могут служить:
Наиболее распространенным методом количественного анализа гипохлорит-иона является титриметрический метод с использованием йодида калия. Для проведения испытания водный раствор или водную суспензию, содержащие гипохлорит-ион, смешивают с избытком раствора йодида калия в сернокислой среде. Выдерживают герметично закрытую смесь в течение 5 минут в темном месте. Выделившийся йод титруют стандартизированным раствором тиосульфата натрия. В качестве индикатора вблизи точки эквивалентности используют крахмальный раствор.
При количественном определении гипохлорит-иона косвенным йодометрическим методом результаты анализа пересчитывают на концентрацию «активного хлора» в ыделившегося при реакции
2H + + ClO – + Cl – = Cl 2 ↑ + H 2 O.
Альтернативным методом количественного определения гипохлорит-иона является потенциометрический анализ с использованием бром-ионселективного электрода. Концентрацию гипохлорит-иона находят методом добавок анализируемого раствора к стандартному раствору или методом уменьшения концентрации анализируемого раствора при его добавлении к стандартному раствору.
Способы получения наиболее важных товарных продуктов
Крупнотоннажными гипохлоритсодержащими продуктами являются гипохлорит натрия и гипохлорит кальция. Их глобальный объем производства превышает 1 млн тонн/год. При этом почти половина этого объема используется в быту, а другая половина в промышленности. Гипохлорит калия, являющийся исторически первым гипохлоритом, нашедшим промышленное применение, производится в ограниченном количестве.
Для промышленного производства гипохлорита натрия используются химический и электрохимический методы. При химическом методе производится хлорирование водных растворов гидроксида натрия. Суть химического превращения не изменилась со времен его открытия и применения Лабарраком
Cl 2 + 2NaOH = NaClO + NaCl + H 2 O.
Существуют две производственные схемы данного метода:
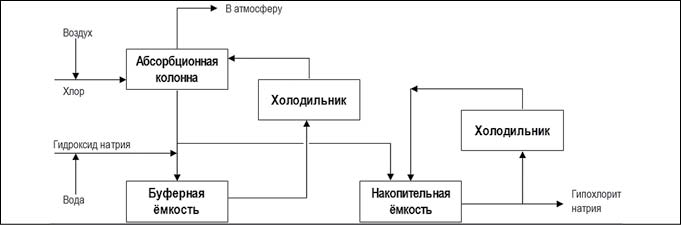
Рис. 4. Химический метод получения гипохлорита натрия основным процессом (рис. с сайта https://ru.wikipedia.org)
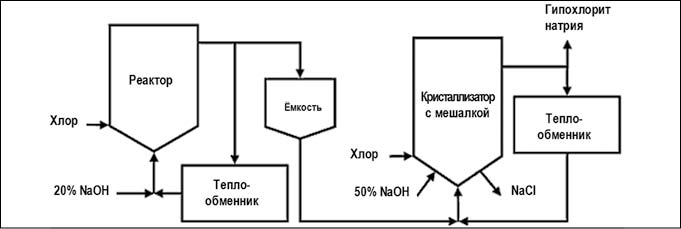
Рис. 5. Химический метод получения гипохлорита натрия концентрированным процессом (рис. с сайта https://ru.wikipedia.org)
При электрохимическом методе получения гипохлорита натрия водный раствор хлорида натрия подвергается электролизу в электролизере с открытыми электродными зонами (бездиафрагменный способ). Гидроксид натрия, образующийся на катоде, и хлор, выделяющийся на аноде, беспрепятственно смешиваются в ходе электрохимического процесса
NaCl + H 2 O = NaClO + H 2 ↑(суммарная реакция).
Гипохлорит кальция производится в виде хлорной извести, представляющей собой смесь целевого продукта с хлоридом кальция и гидроксидом кальция. В качества сырья для получения хлорной извести используется порошкообразный гидроксид кальция (пушенка), содержащий менее 1% свободной влаги и разбавленный влажным воздухом хлор. Небольшая влажность исходных веществ обеспечивает начало реакции гидролиза хлора, сопровождающейся нейтрализацией образующихся кислот известью. Затем реакция продолжается за счет воды, выделяющейся из гидроксида кальция при хлорировании
2Сa(OH) 2 + 2Cl 2 = Сa(ClO) 2 + СaCl 2 + 2H 2 O (суммарно).
Хлорирование пушенки осуществляется в аппаратах непрерывного действия – механических полочных камерах Бакмана.
Таблица 4. Производители гипохлорита натрия в России.
| Название предприятия | Сайт предприятия |
|---|---|
| «Каустик» ЗАО, г. Стерлитамак | www.kaus.ru/ |
| «Каустик» ОАО, г. Волгоград | www.kaustik.ru/ |
| «Новомосковский хлор» ООО, г. Новомосковск | www.hlor.biz/ |
| «Сода-хлорат» ООО, г. Березняки | www.soda.perm.ru/ |
Характеристика товарных гипохлоритов, обращение, хранение и транспортировка
В Российской Федерации гипохлориты производятся в соответствии с ГОСТ 11086–76 «Гипохлорит натрия. Технические условия» и ГОСТ 1692–85 «Известь хлорная. Технические условия». Гипохлорит натрия по назначению и показателям выпускается двух марок «А» и «Б» (табл. 5).
Таблица 5. Физико-химические показатели и назначение гипохлорита натрия по ГОСТ 11086–76