андрогенная алопеция у мужчин что это такое
Андрогенетическая алопеция. Update
Докладчик: Овчаренко Юлия Сергеевна, доцент кафедры дерматовенерологии ХМАПО, член правления Европейского общества исследования волос (EHRS), руководитель клиники «Институт трихологии» (Харьков)
Введение
Андрогенетическая алопеция (АГА) является сложным полигенным мультифакториальным состоянием, которое представляет собой наиболее распространенную форму выпадения волос, поражающую до 80% мужчин и 50% женщин в течение их жизни. АГА развивается с годами и является отражением сегментарного или органоспецифичного преждевременного старения.
Генетические исследования этого заболевания вновь выдвинули на передний план роль наследования. В этой связи недавний анализ опубликованных генетических исследований АГА выявил новую ассоциацию АГА и rs7349332, находящемся на интронном участке WNT10A, тем самым предполагая участие сигнализации WNT в этиологии АГА. В немецком исследовании АГА типа «случай-контроль» было показано, что одной из причин генетического риска развития АГА является выраженный полигенный компонент. Этот факт, вероятно, отражает сложность биологических путей, ассоциированных с АГА
Генетическое тестирование
«Обычно подозреваемым» геном на «андрогенной стороне» в данном случае считается ген андрогенного рецептора (AR), который находится на хромосоме X, что может объяснять передачу AГА от матери. До сих пор неясно, какие гены кроме AR ответственны за АГА. Пациенты должны осознавать, что современное генетическое тестирование основывается на вариациях гена АР, тогда как фактически начало андрогенетической алопеции вызвано полигенным участием других генов или эпигенетических механизмов
Клиническая феноменология
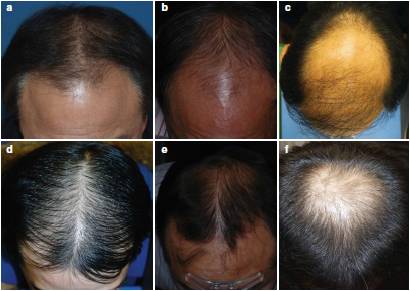
АГА представляет собой непрерывный затяжной процесс, а не серию отдельных фаз заболевания, и у каждого пациента характеризуется широким диапазоном различных признаков. При прогрессировании АГА ведет себя аналогично процессу старения тканей – в волосяных фолликулах, как и в других органах, увеличивается доля клеток, несущих лишь структурную функцию, образуются швы, перетяжки, рубцы, происходит склероз – усиленное развитие компонентов соединительной ткани, что ведет к ослаблению специфических функций, истончению и потере волос
Смещение лобной линии роста назад и облысение макушки – основные признаки мужской андрогенетической алопеции. Кроме того, участки алопеции могут сливаться в единое целое, в результате чего по бокам и на затылке волосистой части головы остается лишь кайма нормального роста волос.
АГА у женщин прогрессирует медленнее, степень ее тяжести меньше, и демонстрирует большее разнообразие ответов на терапию.
У женщин выделяют три различных модели АГА:
диффузное истончение области макушки при сохранении лобной линии роста волос (модель Людвига);
истончение и распространение на центральной части скальпа при нарушении фронтальной линии роста волос (модель рождественской елки);
истончение, связанное с битемпоральными залысинами (модель Гамильтона), чаще, наблюдается у женщин в менопаузе и у женщин с гиперандрогенией.
Андрогенетическая алопеция при синдромах
В редких случаях чрезвычайно тяжелая андрогенетическая алопеция или ее раннее начало может быть симптомом сложного генетического заболевания, как например,
Преждевременное облысение
Андрогенетическая алопеция, клинические признаки которой проявляются в возрасте от 10 до 20 лет, называется преждевременным или ранним облысением. У детей до наступления полового созревания заболевание, как у мальчиков, так и у девочек, проявляется исключительно как облысение по женскому типу.
Дифференциальный диагноз врожденной потери волос включает в себя:
Эволюция классификаций
Определение тяжести андрогенетической алопеции является сложной задачей.
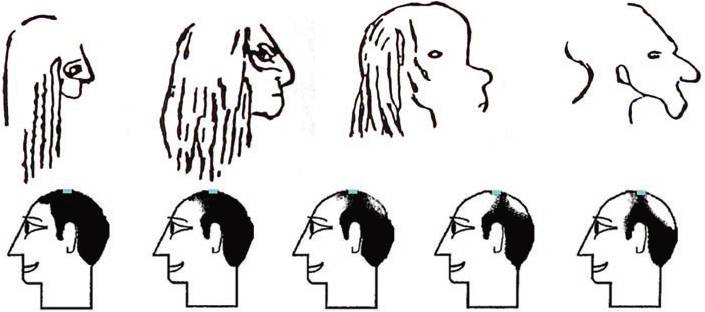
В верхнем ряду представлены четыре рисунка, высеченных на стенах первобытной пещеры. Понадобилось около 30 тысяч лет для классификации типового выпадения волос у мужчин, показанного в нижнем ряду. В настоящее время разработаны и модифицированы различные методы классификации.
Классификации АГА
До недавнего времени общепризнанным стандартом являлись классификация Гамильтона-Норвуда (1951-1975гг) для мужчин и классификация Людвига (1977г) для женщин, подчеркивающих гендерную гетерогенность.
Эволюция или революция?
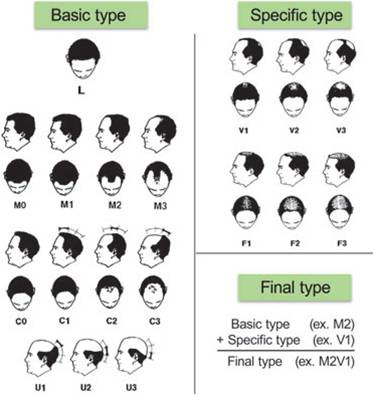
Возникла необходимость усовершенствования существующих классификаций, в результате этого в 2007 году была создана универсальная классификация. В 2007 году Ли (Lee) и соавт. предложили базовую и специфическую (BASP) систему классификации, которая представляет собой усовершенствованный вариант классификации Норвуд-Гамильтона, включает четыре базовых типа (L, M, C, U) и два специфических типа (F и V).
Basic and specific (BASP) classification for pattern hair loss (From: Lee WS, Ro BI, Hong SP et al (2007) A new classification of pattern hair loss that is universal for men and women: basic and specific (BASP) classification. J Am Acad Dermatol 57(1):37–46)
Новая классификация типового выпадения волос является универсальным инструментом, используемым как для мужчин, так и для женщин: базовая и специфическая (BASP) классификация.
С ее помощью можно оценить как дальнейшую степень потери волос, так и ответ на терапию. Благодаря усовершенствованию недостатков существующих классификаций, ее легко запомнить и проще применять в клинических условиях. В классификации Норвуда-Гамильтона не учтены некоторые специфические типы облысения, такие как выпадение волос по женскому типу.
Кроме того, шкала Людвига не может использоваться для классификации облысения по мужскому типу у женщин. BASP независимо от пола или расы позволяет классифицировать все разновидности типов выпадения волос.
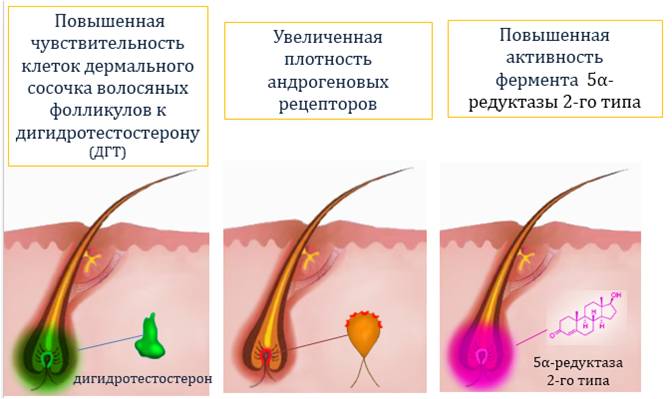
Причины развития АГА
Наиболее значимым фактором у мужчин является повышенная активность фермента 5-альфа- редуктазы II типа, которая в генетически предрасположенных волосяных фолликулах метаболизируют тестикулярный тестостерон в дигидротестостерон (ДГТ).
У женщин, как правило, большую роль играет снижение активности ароматазы, которая преобразует циркулирующий в крови тестостерон яичников в 17 бета-эстрадиол.
Увеличение локальной концентрации ДГТ приводит к прогрессирующему сокращению анафазы за счет более длительной фазы телогена и сопровождается прогрессирующей миниатюризацией ВФ. Миниатюризация ВФ осуществляется за счет относительно резких сокращений количества клеток дермального сосочка и дермальной оболочки. Сопровождается:
Роль перифолликулярного воспаления
В дополнение к андрогензависимым изменениям в патогенезе АГА доказано вовлечение фолликулярного микровоспаления с формированием фиброза, спровоцированн ого присутствующей бактериальной флорой, токсинами и окислительным стрессом.
Новые аспекты патобиологии андрогенетической алопеции
Продолжается поиск механизмов, регулирующих активацию и прогрессирующее развитие АГА. Было установлено, что окислительный стресс является важным фактором, вносящим свой негативный вклад в облысение.
По сравнению с клетками, взятыми из затылочной не пораженной облысением области, клетки дермального сосочка из лысеющего участка мужчин характеризовались значительно большей чувствительностью к окислительному стрессу. А также отличались пониженной пролиферацией и миграцией, сопровождающимися увеличением уровня активных форм кислорода и старением.
АГА – маркер старения?
Некоторые эксперты рассматривают АГА как органоспецифическое сегментарное ускоренное старение с повышенной чувствительностью фибробластов волосяных фолликулов к оксидативному стрессу.
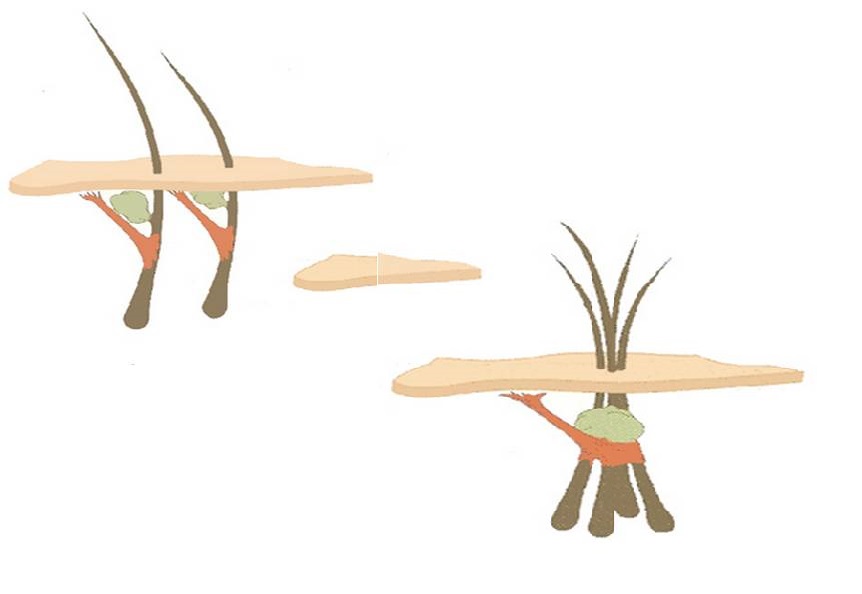
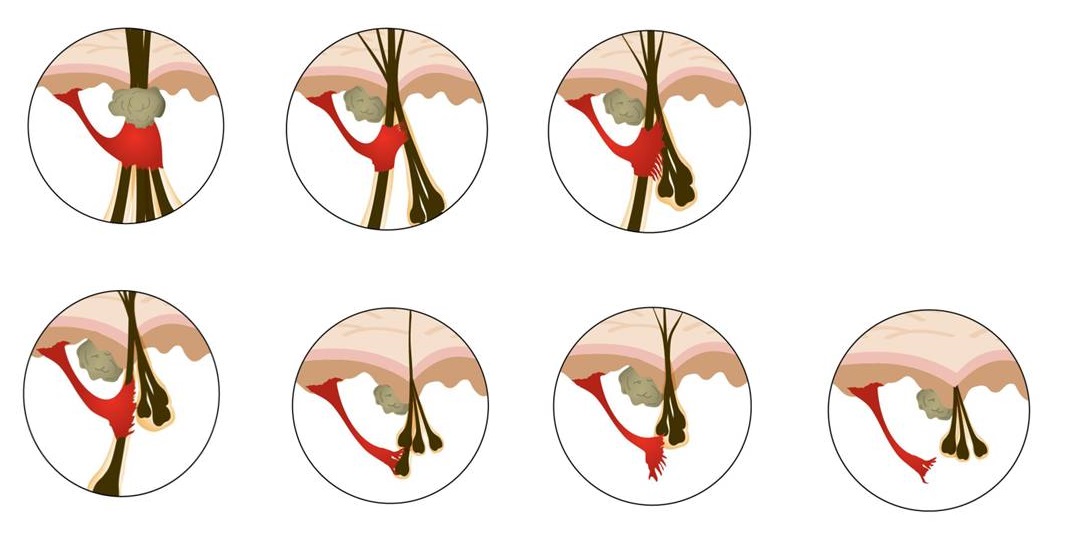
Особое внимание в последнее время уделялось роли дополнительных органов, расположенных в непосредственной близости к волосяному фолликулу. В качестве нового участника патогенеза АГА была выделена мышца, поднимающая волос.
Предложена гипотеза, что потеря соединения мышцы, поднимающей волос, с фолликулярной единицей управляет процессом миниатюризации при АГА и приводит к ее необратимости, в отличие от обратимого процесса, наблюдаемого при гнездной алопеции, при которой соединение мышцы и фолликулярной единицы сохраняется.
| Андрогенетическая алопеция. Гипотеза Высказывалось предположение, что мышца, поднимающая волос, заменяется жировой тканью, и это явление может привести к истощению запасов стволовых клеток или клеток-предшественников в мезенхиме фолликула. |
Также на роль потенциальных факторов в патологии АГА были выдвинуты сальные железы. Было показано, что у пациентов с АГА значительно увеличивается площадь сальных желез при одновременном увеличении количества долей в каждой фолликулярной единице. Высказывалось предположение, что тесная взаимосвязь ДГТ и функциональной активности сальной железы приводит к их расширению, что может спровоцировать ранний переход в фазу катагена или телогена.
ДГТ-зависимые функции клеток определяются наличием слабых андрогенов, их преобразованием в более мощные андрогены под действием 5-альфа-редуктазы, низкой ферментативной активностью дезактивирующих андрогены ферментов и присутствием в больших количествах функционально активных АР.
На предрасположенной к заболеванию волосистой части головы зафиксированы высокие уровни ДГТ и повышенная экспрессия АР.
Ключевая роль отведена превращению тестостерона в ДГТ в дермальном сосочке, тогда как регулируемые андрогенами факторы, вырабатываемые клетками дермального сосочка, предположительно, влияют на рост других компонентов ВФ.
Лишь у части женщин с АГА подтверждается наличие в сыворотке периферической крови патологических изменений в метаболизме андрогенов, а отклонения от нормы часто незначительны. По исследованиям Moltz у 125 женщин с АГА повышение уровня свободного тестостерона обнаружено лишь у 29%.
Описаны при АГА эндокринные нарушениями по другую сторону андрогенного горизонта, характеризующиеся пролактинемией, нарушением тиреостимулирующего гормона (ТСГ), мелатонина, соматотропина. Существует зависимость, связанная со снижением уровня сывороточного ферритина ( A).
Согласно проведенному недавно мета-анализу распространение АГА на макушке связано со значительным увеличением риска развития рака предстательной железы, при этом для других типов распространения АГА значительное увеличение риска рака предстательной железы не характерно.
Терапевтические концепции для реверсирования андрогенетической потери волос
Миноксидил
Миноксидил – универсальный препарат, доступный на отечественном рынке, обладающий широким спектром действия.
| Миноксидил. Клинические исследования • В двух исследованиях с участием 493 женщин раствор 5% сравнивался с раствором 2%. Опираясь на данные подсчета волос, раствор 5% был незначительно более эффективным, чем раствор 2%. • В ходе недавнего сравнительного исследования пены миноксидила 5% и раствора миноксидила 2% у белых пациентов получены схожие результаты. |
Разрабатывается тест для определения ответа на прием миноксидила. Вопрос «предсказуемости» лечения миноксидилом весьма актуален, ведь только 40% пациентов могут похвастаться возобновлением роста волос. При этом для оценки эффективности терапии приходится ждать от 3 до 6 месяцев, все это время принимая лекарство «впустую». Исследователи попробовали использовать определение сульфотрансферазной активности в фолликулах волос для более ранней диагностики эффекта миноксидила.
Суть нового теста основана на следующих наблюдениях. Миноксидил в коже головы под действием фермента SULT1A1 превращается в миноксидил- сульфат. Предполагается, что активность SULT1А1 в волосяных фолликулах коррелирует с эффективностью препарата
Таким образом, использование сульфотрансферазного теста поможет исключить до 95% пациентов, невосприимчивых к терапии
Финастерид и дутастерид
Обнадеживающие результаты в лечении мужской АГА демонстрирует дутастерид, который используется многими дерматологами, несмотря на то, что препарат одобрен для лечения этого состояния только в Корее. Дутастерид характеризуется сходным с финастеридом профилем безопасности.
Гюбелин Харйа (GübelinHarcha) и соавт. в 2014 году опубликовали результаты крупного рандомизированного контролируемого исследования сравнительной эффективности различных доз дутастерида и 1 мг финастерида и плацебо. Авторы установили, что по сравнению с 1 мг финастерида, эффективность приема 0,5 мг дутастерида была значительно выше. Эти результаты дополнительно подтвердили данные о большей эффективности дутастерида (по сравнению с 5 мг финастерида) в увеличении роста волос, полученные в ходе предыдущего рандомизированного контролируемого исследования Олсен (Olsen и соавт. (2006 г)).
Топический финастерид
Ученые из Швейцарии, заботясь о безопасности лечения АГА, разработали новое патентованное средство Р-3074, представляющее собой 0,25% лосьон финастерида для топического применения. Он при клиническом тестировании снижает концентрацию дигидротестостерона в коже волосистой части головы на 40 % сильнее, чем пероральный финастерид. Представляют интерес топические препараты с комбинацией миноксидила и финастерида.
Топический мелатонин
Описанные мощные антиоксидантные свойства мелатонина позволяют рассматривать его как возможный вариант противодействия окислительному стрессу, связанному с инволюционным поредением волос, при АГА и в качестве профилактических мероприятий при поседении.
Недавно на европейский рынок поступили местные препараты мелатонина в качестве косметического средства против старения волос. Доказано, что местный мелатонин подавляет обусловленный УФ-облучением порог эритемы, а также увеличивает долю анагенных волос у женщин с АГА.
Эти данные подкреплены результатами двойного слепого плацебо-контролируемого пилотного исследования, в котором местное применение 1 мл спиртового раствора мелатонина 0,1% у женщин с АГА и диффузной алопецией привело к значительному увеличению анагенных волос после шести месяцев применения по сравнению с плацебо
Пероральные антиандрогены
Альтернативой миноксидила могут служить ципротерона ацетат, спиронолактон и флутамид.
Адьювантные методы лечения АГА и механизмы действия
Стимуляция роста волос
Железосодержащие добавки при отсутствии дефицита
Витамины (биотин, производные ниацина), Кофеин, Мелатонин
Воздействие электромагнитного/статического поля
Улучшение перифолликулярной васкуляризации
Простагландины (випростол, латанопрост), Аминексил, Глицериноксиэфиры и кремний
Минералы, Производные ниацина
Ингибирование действия ДГТ
Цимицифуга рацемоза (Cimicifuga racemosa)
Аминокислоты, Витамины (биотин, производные ниацина)
Микроэлементы (цинк, медь)
Адъювантная терапия
Результаты применения фармакологических средств, одобренных для лечения других заболеваний, таких как пероральные антиандрогены, носят противоречивый характер.
При неэффективности лекарственной терапии рекомендуется хирургическое лечение, хотя и в этом случае наблюдается высокая вариабельность результатов.
Недавно было предложено несколько перспективных методов
Обогащенная тромбоцитами плазма (ОТП)
В отсутствие установленного оптимального уровня концентрации используемый на данный момент метод подготовки ОТП позволяет достичь обогащения на уровне 300-700% (как правило, более 1000000 тромбоцитов/мкл).
Возможное влияние ОТП на рост волос изучается с 2012 года в ходе исследований invitro и invivo у мышей.
Фактические механизмы действия на волосяной фолликул остаются спорными: ОТП invitro активирует пролиферацию клеток дермального сосочка и предотвращает апоптоз, провоцирующий увеличение уровня экспрессии Akt и Bcl-2. Кроме того, ОТП участвует в формировании волосяного эпителия и дифференцировке стволовых клеток в клетки волосяного фолликула. Увеличение уровня экспрессии FGR-7 приводит к продлению фазы анагена в цикле роста волос.
Опубликованные результаты лишь небольшого числа клинических испытаний эффективности ОТП для роста волос не могут считаться объективными. Из 14 клинических испытаний, включенных в систематический обзор Гини (Gkini) и соавт., результаты только 2 исследований, проводимых у женщин, оценивались согласно принципам доказательной медицины
Лазеры
Лазеры и приборы световой терапии используют монохроматические источники света с длиной волны от 600 до 1400 нм в красной/инфракрасной области спектра.
Применение низкоинтенсивной лазерной терапии (НИЛТ), в частности, представляет собой новый подход к лечению отдельных заболеваний волос, в том числе андрогенетической алопеции. Несмотря на отсутствие четкого понимания механизма действия, лазеротерапия стимулирует повторный переход телогенных волосяных фолликулов в фазу анагена, увеличивает продолжительность анафазы, стимулируя эпидермальные стволовые клетки в области выпуклости волосяного фолликула, и предотвращает преждевременное наступление фазы катагена.
Кроме того, было установлено, что этот тип терапии регулирует противовоспалительный и иммунологический ответ.
В 2011 году Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для лечения женской АГА было одобрено применение лазерной расчески Hairmax Lasercomb R, однако опубликованных результатов исследований ее эффективности у женщин нет.
Несмотря на проведение многочисленных исследований, для разработки стандартизированной процедуры лечения необходимы дополнительные данные, в том числе оптимальная длина волны, степень когерентности и дозиметрические параметры.
Безопасность и возможная эффективность НИЛТ как варианта лечения пациентов с АГА, у которых отсутствует ответ на стандартную терапию или отмечена ее непереносимость, должны быть подтверждены в ходе дальнейших клинических испытаний.
Дутастерид в мезотерапии
В ходе недавнего исследования у 126 пациенток изучалась эффективность местных инъекций дутастерида в лечении потери волос по женскому типу. Комбинация 0,5 мг дутастерида, 20 мг биотина, 200 мг пиридоксина и 500 мг D-пантенола в 2 мл растворе вводилась в область макушки интрадермально методом мезотерапии. Инъекции повторяли еженедельно в течение 8 недель, затем через каждые 2 недели в течение 4 недель, на 16-й неделе проводили последний сеанс.
Было установлено, что через 18 недель после начала лечения (по сравнению с группой контроля, получавшей физиологический раствор) такой метод оказал положительное влияние на рост волос у женщин с ПВЖТ. На 18-й неделе у 62,8% больных отмечено зафиксированное на фотографиях улучшение, увеличение диаметра волос и уменьшение их выпадения.
Аналоги простагландинов
Аналоги простагландинов (АПГ), например латанопрост и биматопрост, являются препаратами местного применения для лечения глаукомы и внутриглазной гипертензии. Позже было установлено, что эти вещества способствуют росту и пигментации ресниц. Механизм действия, способствующий возобновлению роста волос, предположительно заключается в стимуляции дермального сосочка, приводящей к активации перехода телогеннных волос в фазу анагена.
Данных о применении АПГ для лечения женской АГА на сегодняшний день нет.
Использование инъекций в кожу головы биматопроста 0,03% раз в неделю в течение 12 недель, а затем раз в две недели в течение 4 недель у 59-летней пациентки с ПВЖТ оказалось безрезультатным.
Микроигольчатая терапия
Исходя из предполагаемого влияния на высвобождение тромбоцитарных факторов роста, активацию стволовых клеток и избыточную экспрессию генов, связанных с ростом волос, в качестве нового лечения АГА предложено использовать микроигольчатую терапию.
Рандомизированное исследование 100 мужчин с АГА легкой и умеренной степени тяжести показало, что эффективность совместного применения дермароллера и лосьона миноксидила 5% в активации роста волос значительно превосходила эффективность применения только миноксидила.
Несмотря на такие многообещающие результаты, использование этого метода в лечении АГА требует подтверждения в ходе клинических исследований.
Трансплантация волос
Если улучшить состояние выпадения волос стандартными методами лечения не удается, как вариант терапии может рассматриваться трансплантация волос. Эта по-прежнему эффективная процедура должна выполняться опытным хирургом, в течение которой отдельные волосяные фолликулы пересаживаются из донорского участка, но, в отличие от мужчин, у женщин из-за диффузного характера выпадения волос площадь такого участка весьма ограничена.
Среди осложнений операции: временное выпадение волос после трансплантации, инфекции, боль и неудачный исход трансплантации.
Новый способ заключается в частичном продольном извлечении фолликулярной единицы, которая может использоваться как полноценная фолликулярная единица для формирования полностью дифференцированного волосяного фолликула. Оставшаяся в дерме на донорском участке частичная фолликулярная единица может выжить и сформировать волос.
Этот метод позволит восстанавливать волосы однократной инъекцией зоны облысения раствором, содержащим выращенные в лабораторных условиях собственные клетки ростковой зоны фолликулов пациента.
Направления будущих исследований
Современными сферами исследований и будущими методами терапевтического воздействия является:
Точная идентификация и эффективная доставка соответствующих защитных и пусковых механизмов, которые будут стимулировать активацию покоящихся стволовых клеток смогут сделать реальными профилактику и обратный ход процесса потери волос.
Записано по материалам доклада Овчаренко Ю.С., доцента кафедры дерматовенерологии ХМАПО, члена правления Европейского общества исследования волос (EHRS), руководителя клиники «Институт трихологии» (Харьков) на VI научно-практической конференции некоммерческого партнёрства «Профессиональное общество трихологов».
Новый взгляд на патогенез и лечение андрогенетической алопеции
Евгений КАРАСЕВ, к. м. н., врач-трихолог, Москва
Татьяна ВИННИК, PhD, врач-дерматовенеролог, трихолог, Астана
Андрогенетическая алопеция (АГА) – сложное мультифакториальное состояние, основным проявлением которого являются истончение и поредение волос в лобно-теменной зоне скальпа как у мужчин, так и у женщин.
АГА развивается с годами и является отражением сегментарного или органоспецифичного преждевременного старения. Рассматривается как неизбежное следствие, так как генетически обусловлена и проявляется у любого человека, как правило, после 30 лет.
«Виновным» геном в данном случае считается ген андрогенного рецептора (AR), который находится на хромосоме X. «Сидит» он латентно, никак себя не проявляя до поры до времени. У каждого индивидуума эта пора своя. Однако, если взглянуть в целом на мужскую половину человечества, в зависимости от активности этого гена их можно разделить на две довольно большие группы: мужчины с высокой активностью АГА-гена и мужчины с невысокой активностью того же гена. У представителей первой группы первые признаки облысения регистрируются в 18–20 лет, когда на лбу появляются ползущие на темя «андрогенетические заливы», формирующие примерно к 30–35 годам отчетливо проглядывающую букву «М». У представителей второй группы происходит то же самое (только с меньшей скоростью!), начинает формироваться примерно в 45 лет. Но финал у всех более или менее одинаковый – лобно-теменное облысение, если не принимать специальных лечебно-профилактических мер. Эволюция клинической картины развивается по сценарию, предложенному в 70-х годах прошлого века Норвудом–Гамильтоном.
Итак, при АГА у мужчин никогда не редуцируются только волосы, образующие узкую кайму на висках и затылке.
Что же касается женской половины человечества, то она в зависимости от активности данного гена распадается на три довольно большие группы: лица с высокой активностью АГА-гена, со средней и с невысокой активностью того же гена. У представительниц первой группы первые признаки облысения регистрируются в 18–20 лет, когда в лобно-теменной зоне начинается постадийный процесс, описанный в 1977 году Людвигом (рис. 2).
У представительниц второй группы то же самое, только с меньшей скоростью, начинает формироваться в 35–40, а у третьей – при наступлении менопаузы, то есть в 50–55 лет.
В редких случаях чрезвычайно тяжелая АГА или ее раннее начало может быть симптомом сложного генетического заболевания, например трихоринофалангеального синдрома, прогерии, синдрома Ларона, миотонической дистрофии Куршмана – Штейнерта – Баттена и пр.
ПРИЧИНЫ РАЗВИТИЯ АГА
В основе развития АГА – генетически обусловленные особенности метаболизма андрогенов в волосяном фолликуле.
Наиболее значимым фактором у мужчин является повышенная активность фермента 5α-редуктазы II типа, которая в генетически предрасположенных волосяных фолликулах метаболизируют тестикулярный тестостерон в дигидротестостерон (ДГТ).
Помимо аналогичных с мужскими локальных метаморфоз андрогенов у женщин в патогенезе АГА, как правило, также большую роль играет снижение активности ароматазы, которая преобразует
циркулирующий в крови тестостерон яичников в 17 бета-эстрадиол.
Увеличение локальной концентрации ДГТ приводит к прогрессирующему сокращению анагена за счет более длительной фазы телогена (рис. 3) и сопровождается прогрессирующей миниатюризацией волосяных фолликулов. Последняя осуществляется за счет относительно резких сокращений количества клеток дермального сосочка и дермальной оболочки.
В дополнение к андрогензависимым изменениям в патогенезе АГА доказано вовлечение фолликулярного микровоспаления с формированием фиброза, спровоцированного присутствующей бактериальной флорой, токсинами и окислительным стрессом.
МЕТОДЫ ЛЕЧЕНИЯ
Лечение АГА прежде всего нацелено на увеличение волосяного покрова кожи головы и предотвращение истончения и поредения волос в будущем. На ранних стадиях оно эффективнее, поскольку изменения волосяных фолликулов не носят необратимого характера.
Существуют как терапевтические, так и хирургические методы восстановления роста волос при АГА: прием модификаторов биологических реакций, гормональных и негормональных антиандрогенов, блокаторов 5α-редуктазы и трансплантация волос.
Так, примером патогенетических средств лечения АГА являются препараты растительного происхождения, получаемые из листьев оливкового дерева, вытяжки из корня лопуха, крапивы двудомной, у женщин – некоторые оральные контрацептивы и спиронолактон.
Радикальным методом восстановления волос при АГА является трансплантация собственных волосяных фолликулов. Принцип хирургического лечения заключается в перемещении андрогеннезависимых терминальных волосяных фолликулов из не подверженной облысению затылочной зоны в участки андрогензависимого поредения. Пересадка волос – это успешный метод лечения АГА с долговременным эффектом. Тем не менее естественное прогрессирование облысения будет продолжаться, и могут потребоваться последующие пересадки, чтобы трансплантированный участок не оказался окруженным кожей, лишенной волос.
Среди наружных методов коррекции АГА упомянем классический миноксидил и ставшие популярными в последнее десятилетие трехфазные комплексы, содержащие «золотую троицу»: вазодилататор эпигенин, трипептидный фактор роста волос и олеаноловую кислоту. Последняя особенно важна при АГА, так как ингибирует 5α-редуктазу. Применяются эти средства по разным схемам в зависимости от стадии процесса. Одним из наиболее терапевтически успешных представителей этого класса препаратов является ДЕКОПИЛЛ™/DEKOPILL™ от медицинской компании Charismo (Даллас, США).
ЭФФЕКТИВНОЕ СРЕДСТВО КОРРЕКЦИИ АЛОПЕЦИЙ
ДЕКОПИЛЛ™ – это новейший запатентованный натуральный биоактивный пептидный комплекс с витаминами, аминокислотами и озонидами, предназначенный для замедления процесса патологического выпадения волос, прошедший испытания и показавший клинически значимые результаты защиты и восстановления фолликулов, а также улучшения структуры и здоровья волоса.
ДЕКОПИЛЛ™ предназначен для устранения основных симптомов патологической утраты волос большинства известных алопеций. Основной результат его действия заключается в продлении фазы роста волоса и улучшении устойчивости к вредному воздействию ДГТ, а также в увеличении кровообращения, усилении витаминизированного питания корней волос и поверхности кожи головы, вследствие чего замедляется процесс старения фолликулов.
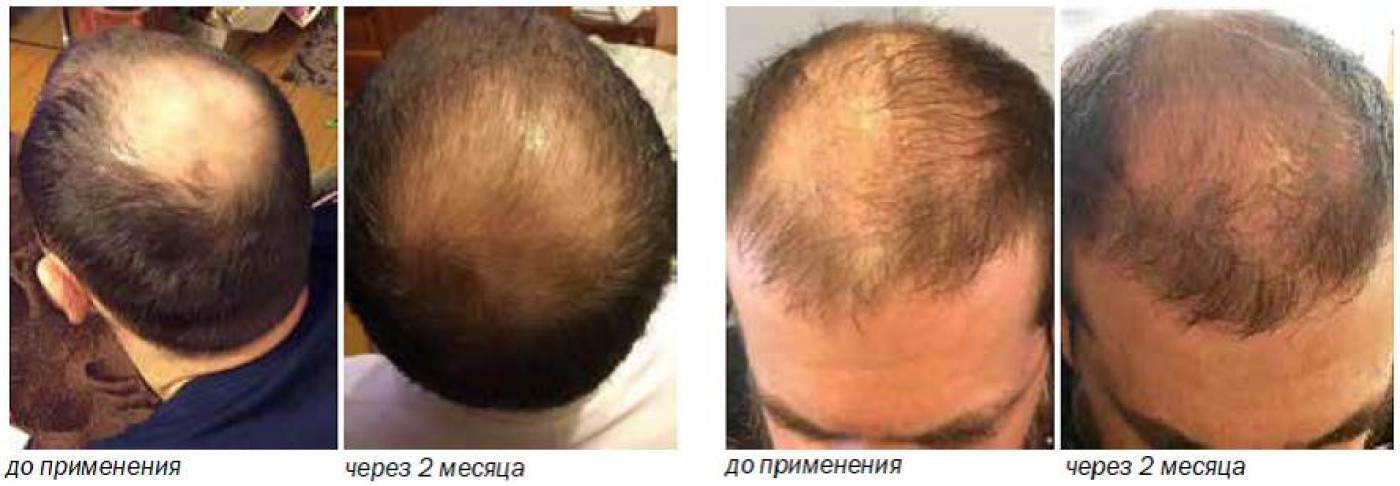
Создатели препарата потратили 10 лет на разработку и клинические испытания, которые показали, что эффекты коррекции алопеций достоверно регистрируются через 30–90 дней от момента начала комплексного лечения.
Быстрое уменьшение количества выпадающих волос (после 30-дневного курса).
Активизация латентно существующих волос (от 0 до 3 мм после 90-дневного курса).
АКТИВНЫЕ КОМПОНЕНТЫ ПРЕПАРАТА:
Доказано, что для эффективного лечебного воздействия при алопециях необходимо стимулировать кровообращение кожи головы не менее 8 часов в сутки. (Для сравнения: перец, горчица, имбирь стимулируют кровообращение не более 1 часа!) Именно этот эффект в препарате достигается с помощью эпигенина неэфиромасличного генеза, что предотвращает любые аллергические реакции.
Возможны покраснения (так как происходит поверхностное расширение сосудов) при протекании на кожу лица или утром при споласкивании волос, которые исчезают через 5–10 минут.
Противопоказания: беременность, онкология в активной форме, частые эпилептические припадки.
ОСНОВНЫЕ ТЕРАПЕВТИЧЕСКИЕ ЭФФЕКТЫ ПРЕПАРАТА:
СПОСОБ ПРИМЕНЕНИЯ ПРЕПАРАТА
Каждый вечер наносите от 5 до 9 полных пипеток лосьона на сухую поверхность кожи головы, мягко промассируйте голову и затем вымойте руки. Оставьте нанесенный лосьон как минимум на 8 часов. На следующее утро допустимо мытье или ополаскивание головы водой.
Минимальный курс применения – 30 дней, наиболее часто рекомендуемый курс применения – 90 дней.
1 упаковка рассчитана на 30-дневный курс – 120 мл (4 флакона х 30 мл).
Для наиболее быстрого и стойкого лечебного эффекта возможно применение лосьона ДЕКОПИЛЛ™ с другими терапевтическими методами:
ЭПИЛОГ
В заключение хотелось бы сделать особый акцент на двух аспектах.
Во-первых, применение всех вышеперечисленных методов лечения не меняет генетическую программу волосяных фолликулов, поэтому терапевтические успехи данных мероприятий носят временный характер и их следует регулярно повторять в течение всей жизни пациента. Также необходимо исключать внутренние факторы (например, железодефицитную анемию, эндокринные заболевания и пр.), совместно с АГА ухудшающие состояние волос и приводящие к их хроническому диффузному поредению.
Во-вторых, для скептиков отметим, что инновационный ДЕКОПИЛЛ прошел строгий дерматологический контроль в клиниках Европы и США, показав при этом свою эффективность и безопасность в результате клинических тестов, которые объективно выявили: