как повысить миелин в мозге
Миелин и его роль в работе нейрона

Миелин – это вещество, образующее миелиновую (мякотную) оболочку, которая отвечает за электроизоляцию нервных волокон и скорость передачи электрического импульса.
Анатомия миелина в строении нерва
Главная клетка нервной системы – нейрон. Тело нейрона называется сома. Внутри нее находится ядро. Тело нейрона окружено короткими отростками, которые называются дендриты. Они отвечают за связь с другими нейронами. От сомы отходит один длинный отросток – аксон. Он несет импульс от нейрона к другим клеткам. Чаще всего на конце он соединяется с дендритами других нервных клеток.
Всю поверхность аксона покрывает миелиновая оболочка, которая представляет собой отросток клетки Шванна, лишенный цитоплазмы. По сути, это несколько слоев клеточной мембраны, обернутые вокруг аксона.
Шванновские клетки, обволакивающие аксон, разделяются перехватами Ранвье, в которых отсутствует миелин.
Функции
Основными функциями миелиновой оболочки являются:
Как работают импульсы
Нервные клетки изолированы благодаря своей оболочке, но все же взаимосвязаны между собой. Участки, в которых клетки соприкасаются, называются синапсы. Это место, где встречаются аксон одной клетки и сома или дендрит другой.
Электрический импульс может передаваться внутри одной клетки или от нейрона к нейрону. Это сложный электрохимический процесс, который основан на перемещении ионов через оболочку нервной клетки.

Изменение напряжения из-за движения ионов калия и натрия называется «потенциал действия». Он распространяется медленно, но миелиновая оболочка, обволакивающая аксон, ускоряет это процесс, препятствуя оттоку и притоку ионов калия и натрия из тела аксона.
Проходя через перехват Ранвье, импульс перескакивает с одного участка аксона на другой, что и позволяет ему двигаться быстрее.
После того, как потенциал действия пересекает разрыв в миелине, импульс останавливается, и возвращается состояние покоя.
Такой способ передачи энергии характерен для ЦНС. Что касается вегетативной нервной системы, в ней часто встречаются аксоны, покрытые малым количеством миелина или вообще не покрытые им. Скачки между шванновскими клетками не осуществляются, и импульс проходит гораздо медленнее.
Состав
Миелиновый слой состоит из двух слоев липидов и трех слоев белка. Липидов в нем гораздо больше (70-75%):
Большое содержание жиров обусловливает белый цвет миелиновой оболочки, благодаря чему нейроны, покрытые ей, называются «белым веществом».
Белковые слои тоньше липидных. Содержание белка в миелине – 25-30%:
Существуют простые и сложные белки нервной ткани.
Роль липидов в строении оболочки
Липиды играют ключевую роль в строении мякотной оболочки. Они являются структурным материалом нервной ткани и защищают аксон от потери энергии и ионных потоков. Молекулы липидов обладают способностью восстанавливать ткани мозга после повреждений. Липиды миелина отвечают за адаптацию зрелой нервной системы. Они выступают в роли рецепторов гормонов и осуществляют коммуникацию между клетками.
Роль белков
Немаловажное значение в строении миелинового слоя имеют молекулы белков. Они наряду с липидами выступают в роли строительного материала нервной ткани. Их главной задачей является транспортировка питательных веществ в аксон. Также они расшифровывают сигналы, поступающие в нервную клетку и ускоряют реакции в ней. Участие в обмене веществ – важная функция молекул белка миелиновой оболочки.
Дефекты миелинизации

Почему происходит разрушение
Наиболее частыми причинами разрушения мякотной оболочки являются:
Заболевания вследствие демиелинизации
Демиелинизирующие заболевания центральной нервной системы:
Демиелинизирующие заболевания периферической нервной системы:
Это лишь часть заболеваний, возникающих из-за разрушения миелинового слоя. Симптомы в большинстве случаев схожи. Точный диагноз можно поставить лишь после проведения компьютерной или магнитно-резонансной томографии. Немаловажную роль в постановке диагноза играет уровень квалификации врача.
Принципы лечения дефектов оболочки
Заболевания, связанные с разрушением мякотной оболочки, очень сложно лечить. Терапия направлена в основном на купирование симптомов и остановку процессов разрушения. Чем раньше диагностировано заболевание, тем больше шансов остановить его течение.
Возможности восстановления миелина
Благодаря своевременному лечению можно запустить процесс восстановления миелина. Однако, новая миелиновая оболочка не будет так же хорошо выполнять свои функции. Кроме того, болезнь может перейти в хроническую стадию, а симптомы сохранятся, лишь слегка сгладятся. Но даже незначительная ремиелинизация способна остановить ход болезни и частично вернуть утраченные функции.
Современные лекарственные средства, направленные на регенерацию миелина более эффективны, но отличаются очень высокой стоимостью.
Терапия
Для лечения заболеваний, вызванных разрушением миелиновой оболочки, используются следующие препараты и процедуры:
Прогноз по заболеваниям
В настоящее время лечение демиелинизации не дает стопроцентного результата, но учеными активно ведутся разработки лекарственных средств, направленных на восстановление мякотной оболочки. Исследования проводятся по следующим направлениям:
Возможно, в скором времени заболевания, связанные с разрушением миелина, перестанут быть неизлечимыми.
Миелиновая защита нейрона: всё начинается до рождения
Александра Коростышевская, Андрей Савелов, Ирина Приходько, Яна Исаева, Василий Ярных
«Наука из первых рук» № 3(88), 2020
С детства мы слышим, что нервные клетки не восстанавливаются. И хотя вопрос о возможности образования новых нейронов во взрослом мозге до сих пор открыт, уже есть данные, что процесс нейрогенеза у человека продолжается до глубокой старости. Любые нарушения в развитии нервных клеток могут приводить к серьезным, иногда необратимым патологиям. Одним из таких нарушений являются дефекты в защитной изоляционной оболочке (миелине) отростков нервных клеток, которые могут формироваться у человека еще до его рождения. Их практически невозможно диагностировать с помощью традиционных методов визуализации.
Об авторах
Александра Михайловна Коростышевская — доктор медицинских наук, ведущий научный сотрудник лаборатории МРТ-технологий, заведующая диагностическим отделением института «Международный томографический центр» Сибирского отделения РАН. Автор и соавтор более 70 научных работ.
Андрей Александрович Савелов — кандидат физико-математических наук, старший научный сотрудник лаборатории МРТ-технологий института «Международный томографический центр» Сибирского отделения РАН. Автор и соавтор более 90 научных работ.
Ирина Юрьевна Приходько — инженер-программист лаборатории МРТ-технологий института «Международный томографический центр» Сибирского отделения РАН. Автор и соавтор 3 научных работ.
Яна Олеговна Исаева — студентка Института медицины и психологии им. В. Зельмана Новосибирского государственного университета.
Василий Леонидович Ярных — кандидат химических наук, заведующий лабораторией отделения радиологии, профессор университета Вашингтона (Сиэтл, США) и Томского государственного университета. Автор и соавтор более 70 научных работ, в том числе 5 патентов.
В мозге человека в среднем содержится около 100 млрд нейронов, которые принимают, хранят, обрабатывают и передают информацию с помощью электрических и химических сигналов. Взаимодействие между нейроном и другими нервными клетками и органами происходит с помощью коротких (дендриты) и длинного (аксон) отростков.
Каждый аксон, подобно проводу, покрыт изоляционным материалом — миелиновой оболочкой, которая обеспечивает более высокую скорость прохождения нервных импульсов и защищает нервные волокна от повреждений. Кроме того, эта оболочка несет опорную функцию, а также, по последним данным, служит для аксона, нуждающегося в большом количестве энергии, своего рода «заправочной станцией».
Аксон — главный «кабель» нейрона, покрытый миелиновой оболочкой. Он отдаленно напоминает линию электропередач с цепочкой изоляторов. Цель оболочки, которую формируют специальные обслуживающие клетки (олигодендроциты либо клетки Шванна), — обеспечить передачу электрических импульсов без потерь и с максимальной скоростью. © Servier Medical Art. Слева — аксоны седалищных нервов мыши (красные), обернутые клетками Шванна (зеленые, ядра — синие). Фото A. Alvarez-Prats и T. Balla. © Eunice Kennedy Shriver / National Institute of Child Health and Human Development / NIH
Все повреждения миелиновой оболочки или дефекты, возникшие в период ее формирования, приводят к серьезным, иногда неизлечимым заболеваниям. Среди них наиболее известен рассеянный склероз — хроническое аутоиммунное заболевание, поражающее преимущественно молодых людей.
Разрушается миелин и при инсультах, которые встречаются не только у взрослых (в первую очередь, как принято считать, у пожилых людей), но и у детей, включая нерожденных. Внутриутробный инсульт чаще всего случается после 28-й недели беременности, у детей — через месяц после рождения. Инсульт у плода приводит к развитию пороков головного мозга, а у детей может вызвать детский церебральный паралич в раннем возрасте.
При этом о «качестве» миелинизации головного мозга конкретного человека мы сегодня судим лишь по косвенным клиническим симптомам или данным магнитно-резонансной томографии (МРТ), с помощью которой обычно удается обнаруживать дефекты миелина уже на поздней, часто необратимой стадии.
В головном мозге миелиновую оболочку создают олигодендроциты, в периферической нервной системе — клетки Шванна. Каждый олигодендроцит образует несколько «ножек», которые неоднократно «оборачиваются» вокруг части какого-нибудь аксона (внизу). В результате один олигодендроцит оказывается связан с несколькими нейронами. © Servier Medical Art. Вверху — олигодедроциты в культуре (красные, ядра — сиреневые). © jakeyoung64
Не все знают, что миелин — это множество слоев клеточной мембраны, много раз «намотанных» на аксон. Формируется миелин плоскими выростами «служебных» глиальных клеток, цитоплазма в которых практически отсутствует. Миелиновая оболочка не непрерывна, а дискретна, с промежутками (перехватами Ранвье). Поэтому аксон обладает более быстрой скачкообразной проводимостью: скорость прохождения сигнала по волокнам с миелином и без него может отличаться в сотни раз. Что касается молекулярного состава «изолятора», то он, как и все клеточные мембраны, состоит преимущественно из липидов и белков.
Дефекты нервной «изоляции»
Развитие мозга плода — сложный процесс, при котором происходят быстрые перестройки морфологии и микроструктуры нервной ткани. В некоторых зонах мозга процесс формирования миелина начинается уже с 18–20-й недели беременности, а продолжается приблизительно до десятилетнего возраста.
Именно нарушения миелинизации часто лежат в основе задержек физического и умственного развития ребенка, а также служат причиной формирования ряда неврологических и психиатрических патологий. Помимо заболеваний, таких как инсульт, задержки развития головного мозга плода с нарушением миелинизации иногда наблюдаются и при многоплодной беременности. При этом десинхронизацию в развитии мозга близнецов оценить «на глаз» довольно сложно.
Но как выявить дефекты миелина в период внутриутробного развития? В настоящее время акушеры-гинекологи пользуются только биометрическими показателями (например, размером мозга), однако они обладают высокой изменчивостью и не дают полной картины. В педиатрии даже при наличии явных функциональных отклонений в мозговой деятельности ребенка традиционные изображения МРТ или нейросонографии (ультразвукового исследования головного мозга новорожденных) часто не показывают структурные отклонения.
Поэтому поиск точных количественных критериев оценки формирования миелина во время беременности является актуальной задачей, которую к тому же нужно решить с помощью неинзвазивных диагностических методов, уже апробированных в акушерстве. Специалисты из новосибирского Международного томографического центра СО РАН предложили использовать для этих целей новый метод количественной нейровизуализации, уже адаптированный для дородовых (пренатальных) исследований.
На обычном томографе
Любая патология головного мозга плода, которую подозревают врачи во время ультразвукового обследования беременной, обычно является показанием к проведению МРТ; подобные исследования проводятся в МТЦ СО РАН уже более десяти лет. Результаты МРТ могут подтвердить, уточнить, опровергнуть либо вообще изменить предварительный диагноз и, соответственно, тактику ведения беременности.
Дело в том, что количество миелина и размеры отдельных структур головного мозга у эмбриона настолько малы, что любые измерения очень сложны и трудоемки. К тому же плод постоянно шевелится, что очень затрудняет получение качественных изображений и достоверных количественных данных. Поэтому нужна технология, позволяющая получать изображения быстро и с высокой разрешающей способностью даже на маленьких объектах.
Именно таким оказался метод быстрого картирования макромолекулярной протонной фракции (МПФ) — биофизического параметра, который описывает долю протонов в макромолекулах тканей, вовлеченных в формирование МРТ-сигнала, тогда как обычно источником сигнала являются протоны, содержащиеся в воде (Yarnykh, 2012; Yarnykh et al., 2015).
Метод макромолекулярной протонной фракции (МПФ) основан на эффекте переноса намагниченности, когда протоны свободной воды «обмениваются» намагниченностью с протонами малоподвижных макромолекул, таких как белки. Скорость этого процесса влияет на величину детектируемого сигнала МРТ и зависит от площади взаимодействия макромолекулярной фракции и воды
В основе метода лежит специализированная процедура математической обработки МРТ-изображений, которая позволяет вычленить компоненты сигнала, связанные с МПФ клеточных мембран. А в головном мозге человека и животных основная их часть содержится именно в миелине. Реконструируются карты МПФ на основе исходных данных, которые могут быть получены практически на любом клиническом томографе.
Для реконструкции карт МПФ используются четыре исходных изображения, полученные различными традиционными методами МРТ. Правильность такого подхода подтвердили результаты его апробации на лабораторных животных в Томском государственном университете: у мышей, которым вводили раствор, вызывающий разрушение миелина, результаты МПФ-картирования совпали с данными гистологического исследования тканей (Khodanovich et al., 2017).
Миелин — в норме и патологии
Пилотные исследования, выполненные в рамках клинических диагностических МРТ-обследований эмбрионов возрастом от 20 недель и старше, показали, что новая технология позволяет за небольшое (менее 5 мин.) время сканирования выявить очень малые количества миелина.
Они также подтвердили способность метода надежно оценивать пространственно-временные «траектории развития» миелина в различных структурах мозга. Судя по результатам исследования, в центральных структурах (стволовых, таламусе, мозжечке) процесс миелинизации начинается раньше, а ее степень пропорциональна возрасту. При этом в белом веществе полушарий головного мозга миелин в дородовом периоде практически не обнаруживается (Yarnykh, Prihod’ko, Savelov et al., 2018). Полученные новым неивазивным методом результаты хорошо согласуются с уже известными патоморфологическими данными.
Карта МПФ (д) реконструируется с помощью специальной математической программы из четырех видов исходных изображений: в режиме переноса намагниченности (а) и протонной плотности (б), референсного (в) и анатомического (г), которые можно получить на обычном томографе
Кроме того, оказалось, что изображения, полученные с помощью новой технологии, являются наиболее информативными для внутриутробной диагностики одного из видов медуллобластомы — врожденной злокачественной опухоли мозжечка. У плода опухоль не удалось отчетливо выявить с помощью традиционного МРТ-обследования, однако она хорошо прослеживалась с использованием количественного метода МПФ.
Дело в том, что у плода показатель МПФ для ткани медуллобластомы вдвое выше значений для окружающей здоровой ткани из-за более высокого содержания в опухоли фибриллярного белка коллагена соединительной ткани, которая широко представлена в этом виде опухоли. После рождения и до полутора лет эти различия сглаживались из-за нарастающей миелинизации мозжечка, в то время как значения МПФ в опухоли оставались практически неизменными.
Наиболее высокие значения МФП и, соответственно, степени миелинизации выявлены в стволовых структурах головного мозга плода. Меньшие значения МПФ обнаружены в таламусе и мозжечке, а минимальные — в полушариях головного мозга. При этом количество миелина в центральных мозговых структурах стабильно увеличивается с эмбриональным возрастом
Эти результаты говорят о том, что диагностическая значимость метода МПФ наиболее высока именно во внутриутробном периоде. И это очень важно, так как после рождения ребенка арсенал МРТ (в том числе с использованием контрастирующих средств), который позволяет визуализировать все детали злокачественного поражения, значительно расширяется (Korostyshevskaya, Savelov, Papusha et al., 2018).
В течение последнего десятилетия для изучения внутриутробного периода созревания мозга использовались различные количественные методы МРТ. Но оказалось, что среди всех известных на сегодня методов наиболее чувствительным к содержанию миелина в мозге взрослого человека и плода оказался метод картирования МПФ.
Медуллобластома — злокачественная опухоль центральной нервной системы, развивающаяся из эмбриональных клеток и локализующаяся преимущественно в мозжечке. Она составляет пятую часть всех опухолей головного мозга у детей. Формирование у ребенка врожденной медуллобластомы удалось проследить с внутриутробного периода. На традиционных МРТ-изображениях головного мозга (карте коэффициента диффузии воды — а и анатомических изображениях с различным контрастом — б, в) опухоль можно диагностировать после рождения: например, она хорошо видна в возрасте 4 месяцев. Однако в последнем семестре беременности опухоль не выделяется на фоне окружающей ткани, но ее можно увидеть на МПФ-карте, потому что медуллобластома содержит большое количество коллагена, влияющего на величину детектируемого сигнала МРТ. Справа — МРТ-изображение нервной системы больного в возрасте 4 месяцев, полученное при обычном сканировании с контрастным усилением. В возрасте 5,5 месяцев ребенку была сделана оперативная резекция опухоли. Внизу — гистологические срезы опухолевых фрагментов, окрашенных гематоксилин-эозином (а) и импрегнированных серебром (б), на которых видны множественные слившиеся опухолевые узлы, окруженные фиброзными волокнами, в состав которых входит коллаген. Фото из архива НМИЦ детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева (Москва)
С его помощью новосибирским специалистам впервые удалось разработать количественные критерии нормальной внутриутробной миелинизации, на основании которых можно оценить своевременность формирования внутренней структуры мозга от второго триместра до рождения ребенка. Эти критерии в дальнейшем можно использовать в клинической практике. Кроме того, в некоторых случаях новый метод помогает диагностировать врожденный порок развития головного мозга еще до рождения, что бывает затруднительно с использованием только традиционных методов МРТ.
Исследование поддержано Министерством образования и науки Российской Федерации (госзадание 18.2583.2017/4.6.), Российским научным фондом (проект № 19-75-20142) и Национальными институтами здравоохранения США (National Institutes of Health, NIH).
Литература
1. Коростышевская А. М., Савелов А. А., Цыденова Д. В и др. Количественный анализ структурной зрелости головного мозга плода по данным диффузионно-взвешенной МРТ // Вест. Новосиб. гос. ун-та. Серия: Биология, клиническая медицина. 2015. Т. 13. № 4. С. 27–32.
2. Коростышевская А. М., Василькив Л. М., Цыденова Д. В. и др. Количественный анализ пре- и постнатальной структурной зрелости головного мозга в норме и при вентрикуломегалии по данным диффузионно-взвешенной МРТ // Мультидисциплинарный научный журнал «Архивариус». 2016. Т. 22. № 10(14). С. 33–41.
3. Korostyshevskaya A. M., Prihod’ko I. Y., Savelov A. A. et al. Direct comparison between apparent diffusion coefficient and macromolecular proton fraction as quantitative biomarkers of the human fetal brain maturation // J. Magn. Reson. Imaging. 2019. N. 50. P. 52–61. DOI: 10.1002/jmri.26635.
4. Korostyshevskaya A. M., Savelov A. A., Papusha L. I. et al. Congenital medulloblastoma: fetal and postnatal longitudinal observation with quantitative MRI // Clinical imaging. 2018. N. 52. P. 172–176.
5. Yarnykh V., Korostyshevskaya A. Implementation of fast macromolecular proton fraction mapping on 1.5 and 3 Tesla clinical MRI scanners: preliminary experience // J. Phys.: Conf. Ser. 2017. V. 886. P. 1–5.
6. Yarnykh V. L., Savelov A., Prihod’ko I. Y. et al. Quantitative assessment of normal fetal brain myelination using fast macromolecular proton fraction mapping // Am. J. of Neuroradiology. 2018. V. 39(7). P. 1341–1348.
Как толщина миелина и эпигенетика помогают устойчивости к стрессу
Результаты экспериментов Валентины Боннефил и коллег показывают, что толщина миелина влияет на устойчивость к стрессу — истончение волокна ведет к социальному поражению у мышей
Автор
Редакторы
Статья на конкурс «био/мол/текст»: В недавней работе Валентины Боннефил и коллег были получены новые данные касательно молекулярных и опосредованных ими морфологических различий в мозге. По предположениям исследователей, именно они обусловливают различия реакций на сильный стресс. Для изучения этого явления была использована модель социального поражения, когда к испытуемой мыши подводят агрессивную мышь. После десяти дней исследуемые грызуны начинают вести себя по-разному — одни продолжают проявлять интерес к общению с другими особям, в то время как другие «замыкаются» в себе. Авторы работы показали, что вторая группа мышей характеризуется более высоким уровнем нарушений в нервной ткани из-за медленного ее восстановления, что, по-видимому, связано с эпигенетическими особенностями.
Конкурс «био/мол/текст»-2019
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2019.
Генеральный спонсор конкурса и партнер номинации «Сколтех» — Центр наук о жизни Сколтеха.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступила компания BioVitrum.
Согласно опросу 2017 года, проведенному Американской психологической ассоциацией, три из четырех американцев сообщают о симптомах стресса в течение тридцати дней, предшествующих опросу [1]. Мы сталкиваемся со всевозможными стрессами — личными, финансовыми, карьерными, новостными и т.д. — все чаще и чаще. Более того, с популярностью интернета появляются и новые виды потребностей и связанных с ними стрессов, например, в 2016 году было проведено исследование по изучению «синдрома упущенной выгоды» (fear of missing out) у подростков. Результаты показали, что увеличившаяся потребность в популярности связана с возросшим использованием Facebook и что эта связь опосредована страхом пропустить какое-либо событие. Появление этого страха, в свою очередь, вызывает повышение уровня стресса [2].
Но растет научное понимание влияния избыточного стресса в долгосрочной перспективе. Исследования показывают, что воздействие стрессовых факторов, начиная от физического насилия и заканчивая социальными конфликтами, значительно увеличивает риск возникновения нарушений психики, таких как депрессия или посттравматическое стрессовое расстройство (ПТСР).
Однако люди по-разному реагируют на один и тот же уровень стресса: некоторые могут проявить устойчивость и быстро восстановиться, в то время как другие борются за выживание и ощущают себя подавленными и потерянными. Механизмы этого различия всё еще вызывают вопросы. Кроме того, исследователи всё еще оценивают, как развиваются долгосрочные последствия индивидуального воздействия стресса.
В работе Валентины Боннефил и коллег 2019 года показано, что поведение, характерное для депрессии, может быть выявлено после социального поражения (рис. 1) в виде повторных атак агрессивных мышей по пять минут в день в течение десяти дней, а также после очаговой демиелинизации в медиальной префронтальной коре [3].
Миелин — защитное покрытие из отростков ненервных клеток (олигодендроцитов), которое изолирует нейроны, а также способствует увеличению скорости проведения сигнала между ними. Разрушение миелина (иначе — демиелинизация) связывают с прогрессией нарушения координации и равновесия и многими другими заболеваниями. Подробнее можно почитать в статье на «Биомолекуле» «Обертка для аксона» [4].
Рисунок 1. Модель социального поражения основана на различной реакции мышей на агрессора.
иллюстрация автора статьи
Ученые, в основном сосредоточившись на роли нейронов, давно проводят исследования того, как различия в реакции на стресс могут найти объяснение в биологических процессах. Тем не менее нейроны представляют собой только один тип клеток головного мозга, и появляется все больше доказательств того, что взаимодействия между нейронными и ненейронными клетками играют важную роль в ответе на стресс.
Исследования выявили, что умеренный уровень ацетилирования гистонов требуется для дифференцировки олигодендроцитов, в то время как высокие уровни ацетилирования гистонов связаны с нарушением миелинизации (из-за отсутствия молодых олигодендроцитов, создающих миелин) [5], [6]. Позднее обнаружили, что уровень миелинизации связан с приспосабливаемостью к изменяющимся условиям (в статье — к социальной изоляции) [7]. В той же работе показано, что истончение миелина связано с незрелым ядерным хроматином, а также повышенным уровнем ацетилирования и пониженным уровнем метилирования. Все изменения в данном исследовании были зафиксированы в префронтальной коре.
Что было сделано?
Сотрудники Центра перспективных научных исследований (ASRC) выяснили, что олигодендроциты, которые образуют миелиновые оболочки в центральной нервной системе, являются ключевыми факторами, определяющими, влияет ли на нас стресс. Эпигенетика позволяет объяснить всё больше вещей, которые ранее не смогла объяснить генетика (подробнее в статье «Эпигенетика: невидимый командир генома» [8]). И дифференцировка олигодендроцитов может зависеть от понижения уровня метилирования (а конкретно, метки H3K9me3 — метилирования гистона H3 в положении 9), сопряженного с разрыхлением (снижением плотности) хроматина и запуском экспрессии генов, специфичных для взрослых олигодендроцитов [9].
Исследователи подвергли мышей (10 — в экспериментальной группе; и 8 — в контрольной) воздействию социального поражения [3]. В итоге мышь либо оставалась социально вовлеченной (активно контактировала с другими особями) и потому была классифицирована как «устойчивая», либо избегала социальных контактов после встречи с агрессором, что позволяло отнести ее к группе «восприимчивых» животных. При этом невосприимчивые мыши были практически неотличимы от контрольной группы, которая не контактировала с агрессором.
Пристальное внимание было уделено прилежащему ядру (NAc) и медиальной префронтальной коре (mPFC), поскольку результаты предыдущих исследований свидетельствуют, что именно эти зоны определяют реакцию на стресс [10].
Что это за области мозга и что про них известно?
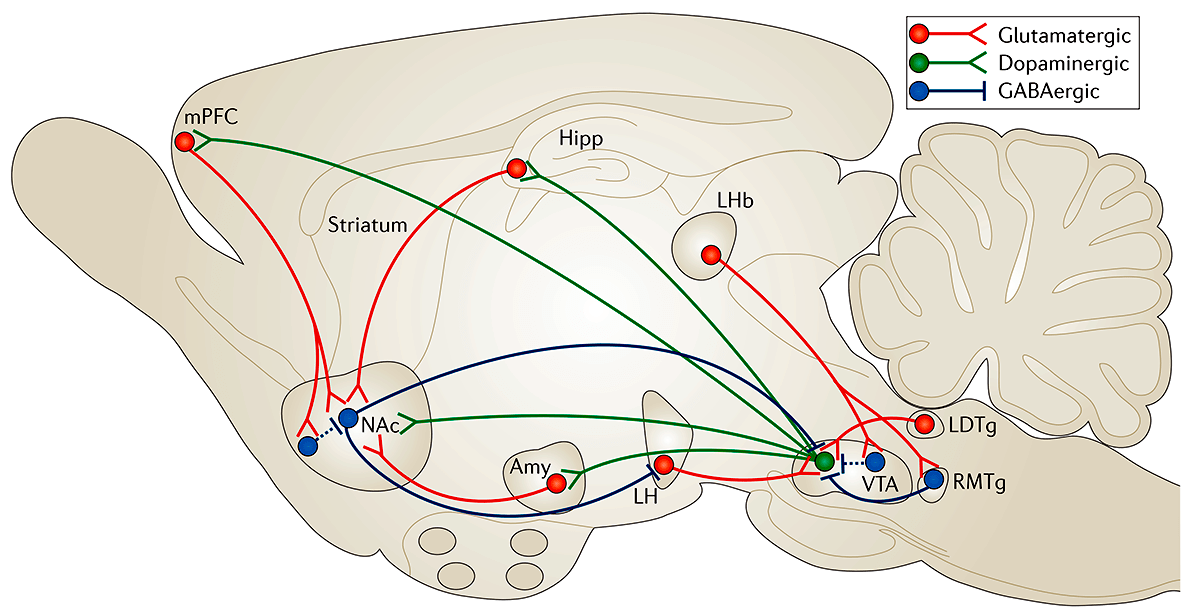
Прилежащее ядро является частью взаимосвязанной системы вентральной области — прилежащего ядра (VTA—NAc). Эта система имеет решающее значение для получения «наград» за счет выделения дофамина. VTA-дофаминергические нейроны также иннервируют несколько областей префронтальной коры (PFC), центральной миндалины, базолатеральной миндалины (BLA) и гиппокампа, а также другие области (рис. 2). Все эти так называемые области вознаграждения мозга сложным образом взаимосвязаны: например, NAc получает плотную глутаматергическую иннервацию из PFC, миндалины и гиппокампа; PFC, миндалина и гиппокамп образуют взаимные глутаматергические связи друг с другом. Функциональный выход каждой из этих областей модулируется несколькими типами ГАМКергических интернейронов.
Рисунок 2. Схема системы вознаграждения вентральной области — прилежащего ядра (VTA—NAc). Упрощенная схема основных дофаминергических, глутаматергических и ГАМКергических связей вокруг вентральной области (VTA) и прилежащего ядра (NAc) в головном мозге грызунов. Первичная схема системы вознаграждения включает дофаминергические связи из VTA в NAc, которые высвобождают дофамин в ответ на стимулы, связанные с вознаграждением (и в некоторых случаях стимулы, связанные с отвращением). Есть также ГАМКергические проекции от NAc до VTA; NAc также получает плотную иннервацию из глутаматергических моносинаптических контуров медиальной префронтальной коры (mPFC), гиппокампа (Hipp) и миндалины (Amy), а также из других областей. VTA получает глутаматергические стимулы от латерального дорсального сегмента (LDTg), латерального поводка эпиталамуса (LHb) и латерального гипоталамуса (LH). Эти различные глутаматергические входы контролируют аспекты восприятия и памяти, связанные с вознаграждением. Пунктирные линии показывают внутренние тормозные проекции. Красные линии — глутаматергические связи; зеленые — дофаминергические; синие — ГАМКергические.
Выделение дофамина в прилежащее ядро — это способ, с помощью которого мозг получает сигналы удовольствия. Чувство удовольствия побуждает нас повторять поведение, жизненно важное для выживания [11], а нарушения в получении дофаминовой награды связаны с такими симптомами, как ангедония и нарушение восприятия и воспоминаний, связанных с вознаграждением [12].
Медиальная префронтальная кора — часть префронтальной коры, которая также связана с системой вознаграждений, как было показано выше. Согласно результатам исследований, пациенты с депрессией имеют меньший объем коры, включая уменьшенный объем белого вещества в этой области, что и ведет к нарушению восприятия событий, которые раньше приносили радость [13].
Что обнаружили и какие сделали выводы?
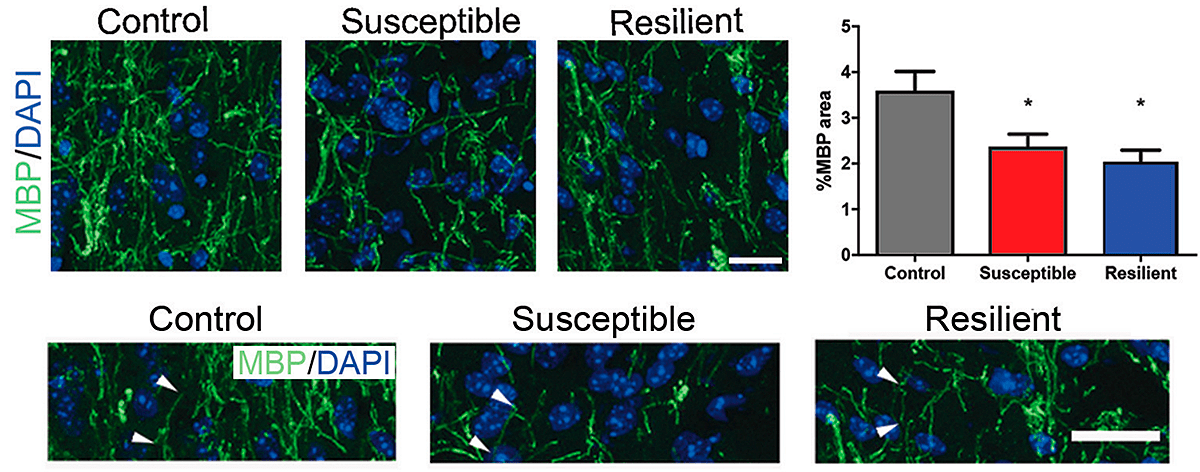
В обсуждаемой работе было показано, что поведение, связанное с социальным избеганием, может быть выявлено после социального поражения, а также после очаговой демиелинизации в mPFC, и поэтому может быть вызвано гипомиелинизацией. Обнаружили также, что миелин в прилежащем ядре истончается у обеих групп мышей (рис. 3). Но только у «восприимчивых» мышей выявили меньшее количество зрелых олигодендроцитов, а охват миелином оказался короче и тоньше.
Рисунок 3. Изображения с конфокального микроскопа и количественные оценки, показывающие иммуногистохимию основного белка миелина (МВР), контрастирующего с DAPI (4′,6-диамидино-2-фенилидолом, флюоресцентным красителем), 20-кратное увеличение. Control — контрольная группа; susceptible — «восприимчивая» группа; resilient — «устойчивая» группа. Статистический анализ проведен по одностороннему ANOVA с тестом Тьюки.
Более того, исследователи обнаружили снижение уровня метилирования гистонов (а именно метки H3K9me3, связанной с дифференцировкой незрелых олигодендроцитов) в предшественниках олигодендроцитов у «восприимчивых» мышей.
Метилирование гистонов представляет собой присоединение метильных групп к положительно заряженной аминокислоте лизину или аргинину с целью нейтрализации заряда. Связывание происходит с помощью фермента гистонметилтрансферазы. Это универсальный эпигенетический механизм, так как он приводит к активации или репрессии гена в зависимости от функции последнего. Метилирование гистонов в разных остатках служит маркером для связывания различных белковых активаторов/репрессоров, которые регулируют экспрессию гена.
Снижение уровня метилирования гистонов у предшественников олигодендроцитов, по-видимому, указывает на то, что эпигенетическая модификация может быть как причиной нарушения программы дифференцировки, так и ее следствием. Полученные данные позволяют нам говорить только о корреляции этих двух наблюдений, но не о причинно-следственной связи. Авторы говорят о возможности существования механизма эпигенетического переключения. Согласно этой концепции, стресс способен влиять на эпигенетическую модификацию предшественников олигодендроцитов, контролируя их развитие, а также отражается в миелиновых паттернах человека. В пользу этого говорит тот факт, что при образовании нового миелина его характеристики возвращаются к норме. Это свидетельствует о том, что изменения в результате этого стресса зачастую не вызывают повреждения ДНК, а только (обратимые) эпигенетические изменения.
Лизолецитин (иначе — лизофосфатидилхолин) является сильнодействующим растворяющим мембрану химическим веществом, которое обычно вводят в белое вещество мозга в виде 1%-ного раствора, чтобы вызвать очаговую демиелинизацию. В 1972 г. Сьюзан Холл была первой, кто продемонстрировал использование лизолецитина для создания демиелинизирующих поражений в белом веществе спинного мозга взрослой мыши [14].
Таким образом, мы можем говорить о том, что дефектная миелинизация воспринимается как дезадаптивный механизм (нарушение адаптации), возникающий только у «восприимчивых» мышей после воздействия повторяющегося социального стресса. Ранее было обнаружено, что дефекты миелинизации появляются у социально изолированных взрослых мышей еще до проявлений поведения социального избегания, что связано с нарушениями в системе получения удовольствия, вплоть до ангедонии [7].
Ангедония — неспособность чувствовать удовольствие, по определению французского физиолога Теодюля Рибо [15]. Сейчас определение включает также пониженную мотивацию к действиям, которые раньше вызывали радость [16]. Это различие важно, например, для животных моделей ангедонии, в которых эмоциональный опыт удовольствия сложно измерить, но мотивацию получения вознаграждения гораздо легче исследовать [17]. Ангедонию встречают у людей с различными психическими заболеваниями и состояниями — депрессией, шизофренией, болезнью Альцгеймера; она также играет важную роль в посттравматическом стрессовом синдроме и расстройствах пищевого поведения.
Почему у мышей различная устойчивость к стрессу?
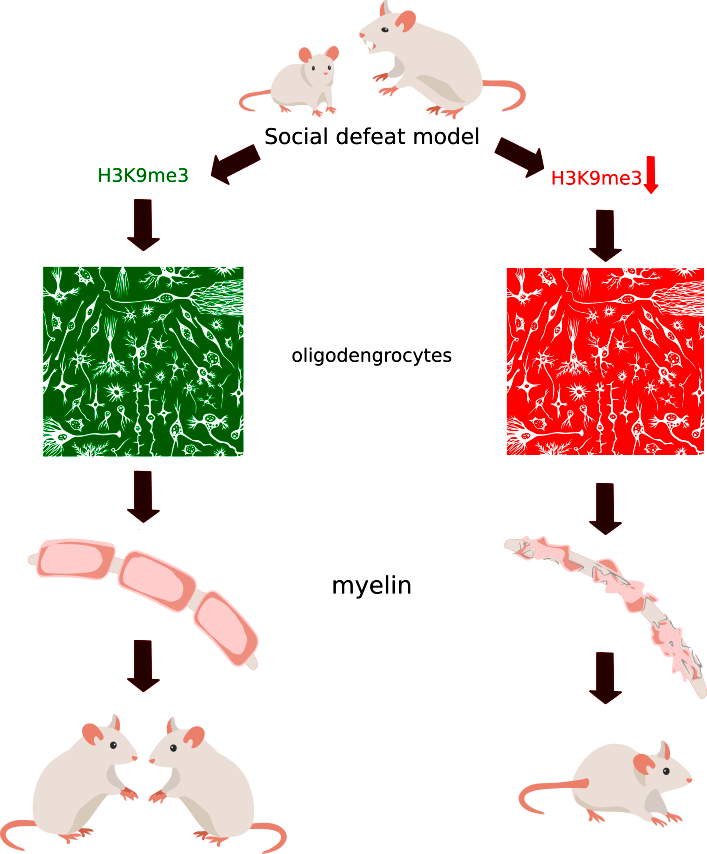
По-видимому, потому что у них различно число зрелых олигодендроцитов. Снижение уровня метилирования гистонов в предшественниках олигодендроцитов связано с нарушением дифференцировки (превращению в функциональные клетки), которая связана (коррелирует, по неподтвержденной гипотезе, ведет к) с истончением миелиновых волокон, что, в свою очередь, приводит к отсутствию адаптации к стрессу. Вот картинки с одной из гипотез о том, как все устроено (рис. 4).
Рисунок 4. Возможная схема различий реакции на социальное поражение, когда у одних мышей наблюдается пониженный уровень метилирования гистона H3 в положении 9, сниженный уровень зрелых олигодендроцитов и истончение миелина, а потому и избегание контактов с другими особями. В это же время другие мыши имели неотличимый от контрольных уровень метилирования гистона, их миелин не подвергся сильным изменениям, и они продолжали выражать интерес к общению с другими мышами. Social defeat model — модель социального поражения; oligodendrocytes — олигодендроциты; myelin — миелин.
иллюстрация автора статьи
Устойчивость к стрессу может возникнуть в результате активных стратегий преодоления, а не пассивного бездействия, определяемого как отсутствие адаптивного ответа. Одна из возможностей образования нового миелина в качестве стратегии преодоления связана с повышенной нейронной активностью у устойчивых мышей в нейронах префронтальной коры после социального поражения. Было показано, что оптогенетическая стимуляция префронтальной коры помогает формированию «устойчивого» фенотипа у мышей с социальным поражением.
Оптогенетическая стимуляция — использование света для контроля клеток на участке нервной ткани. Подконтрольные клетки предварительно генетически модифицированы для экспрессии светочувствительных ионных каналов. Метод позволяет осуществить оптическую модуляцию нейронной активности с высокой временной и пространственной разрешающей способностью, доходящей до размера единичного нейрона.
В то же время снижение качества и количества олигодендроцитов не является постоянным. Это говорит о том, что также вовлечен какой-то другой механизм, помимо обусловленного генетически, который централизованно регулирует развитие олигодендроцитов.
Глия — ненейронные клетки нервной системы, осуществляющие поддержание гомеостаза нейронов, обеспечивая их защиту и питание, а также формирование миелина. В центральной нервной системе к глиальным клеткам относят, например, олигодендроциты, астроциты и микроглию.
А что про воспаление, связанное со стрессом?
Альтернативный механизм может быть основан на различиях в воспалительных компонентах между двумя группами. Изучение интерлейкинов при расстройствах настроения ведется уже более двадцати лет [20]. Центральный вопрос заключается в том, в какой из частей нервной системы — периферической или центральной — синтезируются цитокины, играющие главную роль в формировании воспалительного компонента расстройств настроения.
Интерлейкины — группа цитокинов, изначально известных как часть иммунного воспалительного ответа; но также найдено, что они регулируют нейронную функцию в центральной и периферической нервных системах.
Анализ маркеров периферического воспаления последовательно выявляет увеличение интерлейкинов-6 (IL-6), интерлейкинов-1β (IL-1β) и фактора некроза опухолей-α (TNFα) у пациентов с расстройствами настроения. Измененные центральные уровни этих факторов также были определены.
Известно, что снижение уровня синтеза IL-6 во всем организме или только в лейкоцитах способствует развитию «устойчивого» фенотипа [21]. Используя компьютерное моделирование, Скотт Руссо с коллегами показал, что одновременная тревожность, уменьшение объема гиппокампа и повышение уровня системного интерлейкина-6 характеризовали восприимчивый фенотип, у которого развились поведенческие и нейробиологические нарушения после социального поражения [22].
Транскрипционный фактор — белок, связывающий ДНК в особых участках и регулирующий или инициирующий транскрипцию гена.
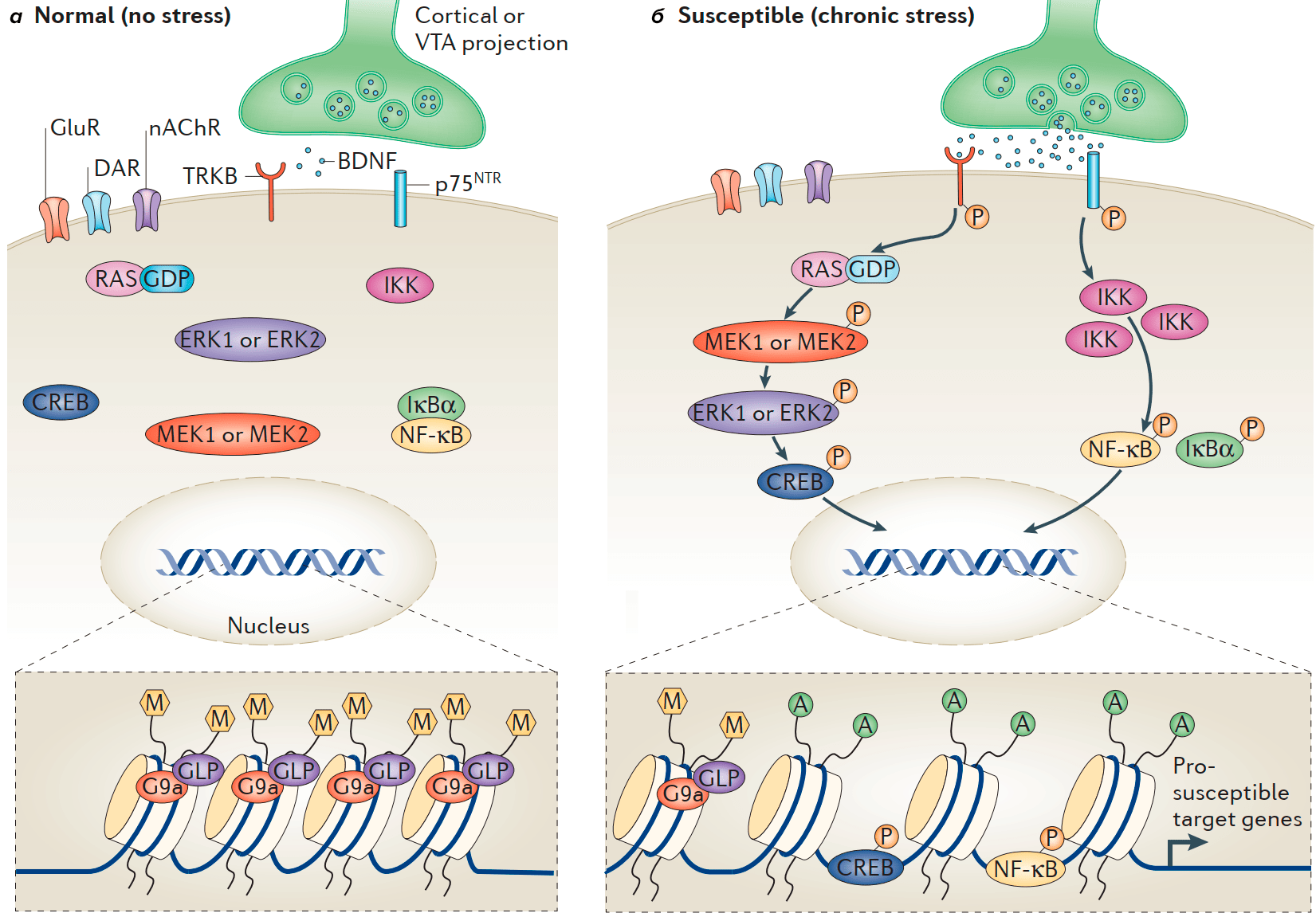
Например, в гиппокампе активация NF-κB участвует в нарушении нейрогенеза и индукции ангедонии [25]. В NAc хронический стресс после социального поражения увеличивает уровни киназы ингибитора NF-κB (IKK), что способствует активации NF-κB, который связывается с ДНК и изменяет транскрипцию группы генов. Одновременно меняется и эпигенетика — снижается уровень метилирования и повышается уровень ацетилирования. Это стимулирует образование новых незрелых шипиков на дендритах NAc. Данный процесс происходит только у восприимчивых животных, но не наблюдается у устойчивых особей (рис. 5). Прямое ингибирование IKK в NAc «обрезает» эти новые синапсы и обращает вспять связанные с ними депрессивные фенотипы [26]. Текущие исследования фокусируются на внутриклеточных сигнальных путях, посредством которых цитокины регулируют активность NF-κB, связанную со стрессом, а также нацелены на выявление транскрипционных мишеней NF-κB, которые опосредуют эти эффекты.
Шипики — выросты мембраны дендритов, играют важную роль в формировании и регуляции глутаматного синапса.
Другим механизмом, связывающим воспаление с развитием депрессивной симптоматики, является влияние цитокинов на гипоталамо-гипофизарную ось (HPA). Цитокины могут действовать на глюкокортикоидные рецепторы и косвенно активировать синтез кортикотропин-рилизинг-гормона (CRH), адренокортикотропного гормона (ACTH) и кортизола [27]. Степень, в которой цитокины индуцируют высвобождение ACTH и кортизола, является прогностическим фактором развития симптомов депрессии [28]. Это означает, что чувствительность оси HPA к воспалительной стимуляции особенно важна для развития аффективно-когнитивных симптомов депрессии.
Заключение
Отцом исследований стресса считают Ганса Селье, который определял стресс как «неспецифическую реакцию организма на любую потребность» и впервые предположил о наличии связи между стрессом и развитием заболеваний. Сейчас исследования стресса базируются на стыке фармакологии, патологии и нейронаук и направлены на изучение на молекулярном уровне.
Понимание изменений, которые вызывают стресс в организме, позволяет исследователям начать составлять карту потенциальных клинических вмешательств с конечной целью снижения его негативных последствий и предотвращения психических расстройств. Большинство современных методов лечения фокусируются на здоровье нейронов, но это исследование подтверждает возможность вмешательства в глиальные клетки, по крайней мере, в случае психических заболеваний, связанных со стрессом.
Несмотря на то, что данная статья добавляет ясности в наше понимание формирования двух групп в реакциях на социальное поражение, при переносе результатов на людей мы должны помнить о невозможности полностью смоделировать депрессию у животного по ряду причин. Во-первых, депрессия у людей — это не одно заболевание, а очень неоднородный синдром. Во-вторых, ключевые симптомы человеческой депрессии (то есть вина, суицидальность и грусть) не могут быть оценены (и могут не существовать вовсе в зависимости от того, как мы эти эмоции определяем [29]) у животных. И в-третьих, биология, лежащая в основе многих типов человеческой депрессии, остается плохо изученной. Однако ясно, что воздействие стресса увеличивает риск депрессии у людей, и, следовательно, большинство моделей депрессии грызунов полагаются на стрессовые факторы окружающей среды, чтобы вызвать симптомы, подобные депрессии, которые можно изучать механически.
Важное предостережение в отношении работы, описанной в этой статье (и в большинстве работ, использующих мышиные модели), заключается в том, что было использовано небольшое количество мышей, недостаточное для высокой достоверности результатов. Более того, исследование проводили исключительно на самцах грызунов, несмотря на тот факт, что в человеческом мире женщины в два раза чаще страдают расстройством настроения, чем мужчины [30]. И модели грызунов демонстрируют, что особи женского пола испытывают более депрессивное поведение после хронического стресса [31]. Было высказано предположение, что различия в развитии связанных с вознаграждением нейронных цепей могут предрасполагать женщин к депрессии [32]. Кроме того, прямое воздействие циркулирующих половых гормонов на систему вознаграждения может изменить чувствительность женщины к стрессу во время менструального цикла [33]. Исследования на грызунах действительно показали, что гормоны яичников изменяют пороги вознаграждения за стимуляцию мозга, что означает, что во время определенных фаз эстрального цикла женщины более склонны к ангедонии [34]. Это должно быть чрезвычайно высоким приоритетом для будущих исследований; мы должны определить, в какой степени рассмотренные выше механизмы применимы к моделям женской депрессии.
Важно также помнить, что наши реакции часто обусловлены опытом наших предков, который закодирован в эпигеноме (на «Биомолекуле» этому посвещена статья «Эпигенетика поведения: как бабушкин опыт отражается на ваших генах» [35]), что позволяет напомнить о важности поддержания психического здоровья во всех поколениях. И самый простой, ставший почти скучным совет (который все еще работает): достаточное количество сна, отдых и режим питания — это то, что мы уже сейчас можем сделать для улучшения своей эпигенетики.