как повысить норадреналин в мозгу
Тайны голубого пятна
Норадреналин. Гормон и нейромедиатор. Характер совсем не нордический: слывет «медиатором бодрствования», зачинщиком реакций «бей или беги» (черта семейная, брателло Адреналин способен на худшее).
Автор
Редакторы
«В глубине души» — это выражение мы используем в случае, когда говорим о каких-то представлениях, лежащих в основе нашего мировосприятия. Порой мы не всегда готовы с ними согласиться, но знаем, что они верны и влияют на нашу жизнь. В глубине нашего мозга находится скопление нервных клеток, которое влияет на нас: изменяет память, внимание, поведение. Отростки этих нейронов устремляются к различным отделам коры, чтобы на месте из синапсов выделилось вещество со знакомым нам названием — норадреналин.
Знакомая схема
Рисунок 1. Норадренергические волокна головного мозга. Из ряда глубоких структур мозга отростки норадреналиновых нейронов направляются в мозжечок, миндалевидное тело, кору и таламус.
Раньше я уже писал про дофамин [1] и серотонин [2]. Теперь настало время норадреналина (международное непатентованное наименование — норэпинефрин, у нас используется название из Британской фармакопеи). Это вещество не часто появляется в научных новостях, так что будем исправлять эту несправедливость. Не бывает неинтересных нейромедиаторов — бывает мало доступного материала.
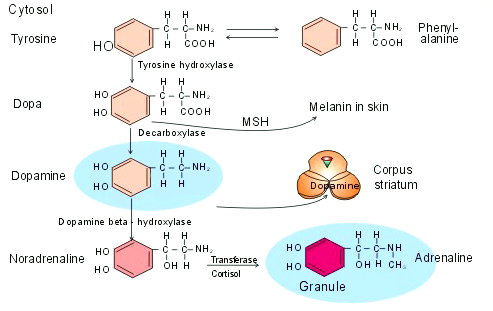
Источником норадреналина в организме всех млекопитающих, в том числе и человека, является образование в глубоких отделах головного мозга, которое носит довольно необычное название — голубое пятно. Из голубого пятна множество отростков разбегается в различные отделы головного мозга: мозжечок, таламус, миндалевидное тело и кору (рис. 1). Подобная организация путей в мозге характерна для серотониновой и дофаминовой систем. По широте распределения связей норадреналиновые пути особенно напоминают серотониновую систему. Если рассматривать синтез норадреналина, то мы увидим, что для образования дофамина и норадреналина необходимы одни и те же реакции: дофамин является предшественником норадреналина (рис. 2).
Рисунок 2. Синтез норадреналина. На схеме также показаны пути синтеза других нейромедиаторов.
учебник «Новая физиология человека», ошибка на рисунке исправлена
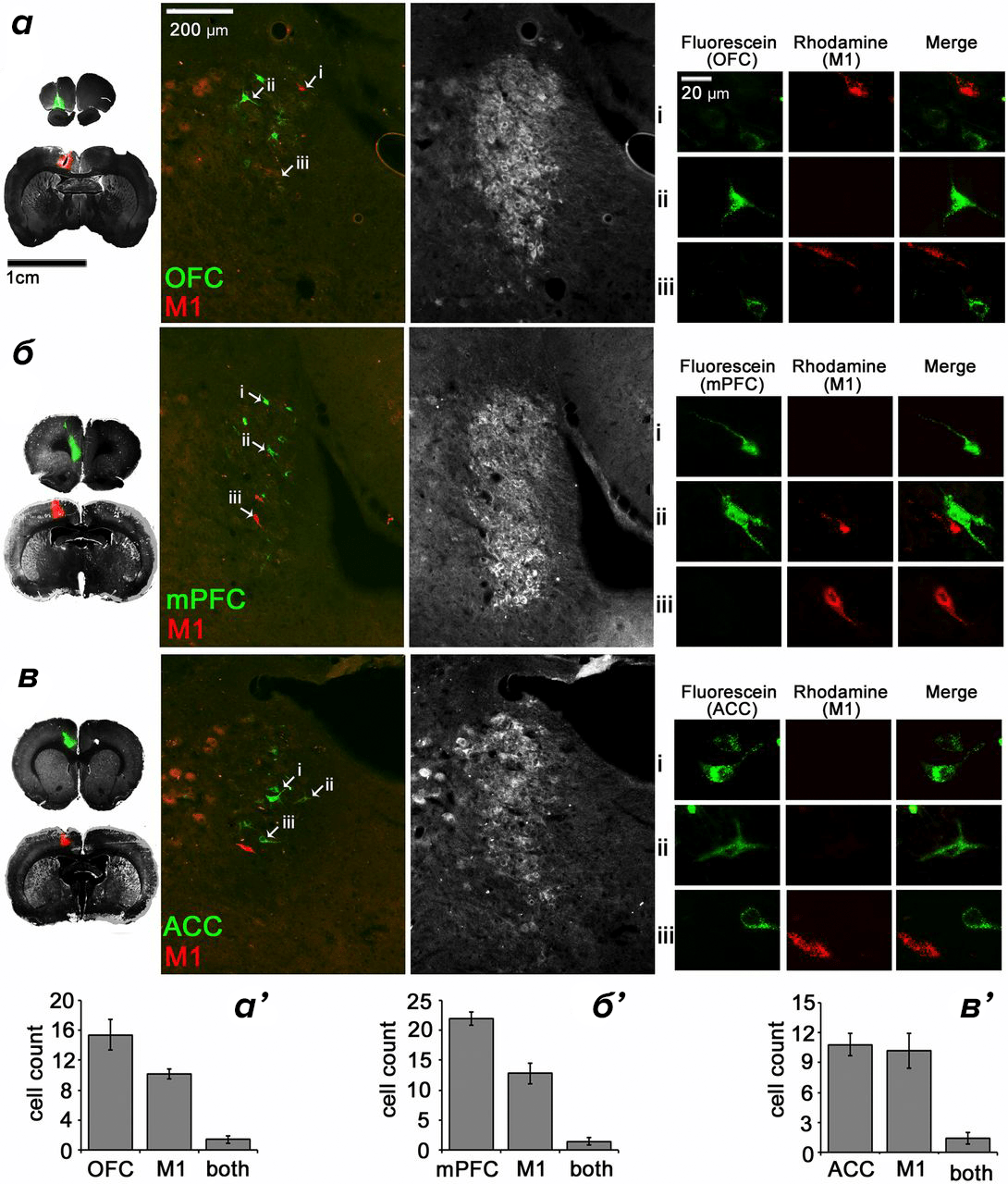
В самόм голубом пятне существует четкое разделение нейронов по функциям, по тем отделам головного мозга, куда идут отростки норадренергических нейронов [3]. Для изучения такой функциональной специализации ученые вводили в моторную область и другие участки коры крыс специальный флуоресцирующий реагент, способный к ретроградному перемещению в клетках. Оказавшись в коре, вещество по аксонам мигрирует в голубое пятно, где можно будет распознать отдельные нейроны на срезах нервной ткани. В эксперименте сравнивали количество «прокрашенных» нейронов при парных инъекциях: одна инъекция проводилась в область моторной коры, локализация другой менялась в зависимости от изучаемого участка. Оказалось, что в среднем только около 5% нейронов, находящихся в голубом пятне, имели проекции в оба изучаемых участка, и отдельные участки коры получали сигналы преимущественно от «своих» норадренергических нейронов (рис. 3). Также различные популяции нейронов в голубом пятне отличались по биохимическим показателям и по электрической активности в зависимости от того, в какие участки коры направлялись их отростки. Это говорит о довольно сложной организации голубого пятна.
Рисунок 3. Различные популяции норадренергических нейронов в голубом пятне крысы. На рисунке изображены нейроны, отростки которых связаны с различными отделами головного мозга. М1 — моторная кора; OFC — орбитофронтальная кора, mPFC — срединная префронтальная кора; ACC — передний отдел поясной извилины.
Одна из главных функций норадренергической системы — регуляция активности организма. Работа голубого пятна связана с такими процессами, как сон и бодрствование [4]. При спокойном бодрствовании голубое пятно генерирует электрические импульсы с частотой 1–3 Гц (1–3 импульса в секунду). При предъявлении важных стимулов частота импульсов увеличивается до 8–10 Гц. Во время фазы медленного сна активность голубого пятна постепенно снижается, а фаза быстрого сна характеризуется почти полной инактивацией норадренергической системы. Кроме голубого пятна в регуляции цикла бодрствования задействованы и другие структуры глубоких отделов головного мозга — вместе они образуют целую систему регуляции активности нервной системы. Однако главный заводила в этой системе — голубое пятно [5].
Внимание! Внимание!
Голубое пятно входит в сложную сеть отделов нервной системы, которая регулирует внимание. Кроме норадреналиновых структур внимание зависит от серотониновых нейронов ядер шва и холинергических клеток, находящихся, например, в базальном ядре Мейнерта. Волокна голубого пятна, идущие в таламус и кору, больше всего влияют на поведение и внимание. Связи, соединяющие голубое пятно с гиппокампом (центром памяти) и миндалиной (центром эмоциональных реакций), оказывают влияние на процессы запоминания и — как следствие — на обучение.
Могло сложиться впечатление, что голубое пятно работает только на «выход», а не на «вход», но это не так: сигналы от сенсорных систем также приходят в него и меняют его активность. Входящие сигналы, не связанные с наказанием или наградой, вызывают небольшое повышение активности голубого пятна, но она быстро возвращается к прежнему уровню. Более важные события, оказывающие негативное или положительное влияние на организм, меняют активность голубого пятна значительно. Учитывая огромное количество связей этого отдела нервной системы с другими ее частями, будет меняться и активность связанных с ним отделов. Поступающая сенсорная информация будет модулировать активность головного мозга, не приводя к конкретным действиям. Это то, что ученик академика Павлова Пётр Степанович Купалов назвал усеченными условными рефлексами: реакция нервной системы на входящий стимул в виде изменения своей активности, без конкретных действий. По-видимому, подобные рефлексы осуществляются через голубое пятно.
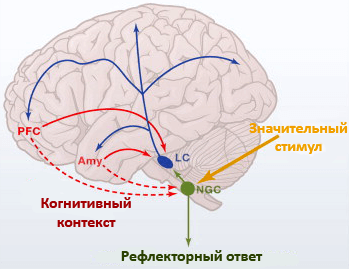
Рисунок 4. Схема переключения внимания и его регуляции. LC (locus coeruleus) — голубое пятно; PFC (prefrontal cortex) — префронтальная кора; Amy — миндалина; NGC (nucleus gigantocellularis) — гигантоклеточное ядро ретикулярной формации; влияние норадреналина показано синими стрелками. Несмотря на то, что сигналы, входящие с периферии в голубое пятно (желтые и зеленые элементы), способны переносить фокус нашего внимания на какие-то объекты, сознательная активность (красные элементы) также позволяет нам произвольно регулировать внимание.
Приблизительная схема работы головного мозга при установлении фокуса внимания на какой-то задаче или определенном предмете может выглядеть так. Сенсорная информация приходит в голубое пятно из более глубоких отделов. Оттуда по норадренергическим волокнам сигналы отправляются в другие отделы мозга, отвечающие за мышление и поведенческие реакции — префронтальную кору и миндалевидное тело (рис. 4). Их активность, измененная под воздействием норадреналина, приводит к смещению внимания или конкретным действиям. Эти действия могут основываться на условных или безусловных рефлексах, что в принципе не так уж и важно. Однако активность лобной коры и миндалевидного тела может влиять на состояние голубого пятна: мы способны сознательно игнорировать поступающие извне сигналы. Например, углубляться в чтение книги при работающем телевизоре [6].
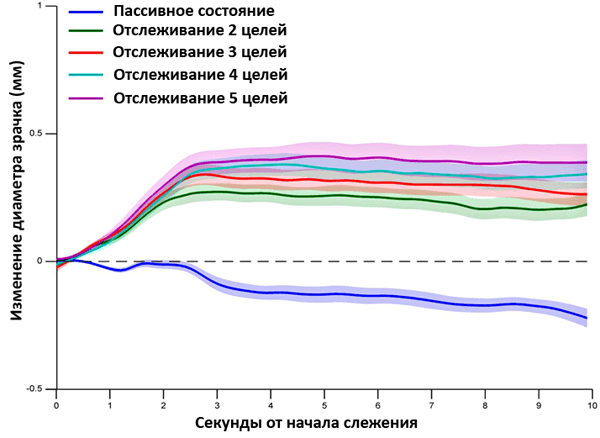
Уделяемое той или иной проблеме внимание сложно измерить напрямую. Существуют когнитивные тесты, используемые в психологии и медицине, но биологов обычно интересуют показатели, которые напрямую связаны с физиологическими изменениями. Для изучения внимания таким показателем стал размер зрачка [7]. В одном исследовании, проведенном норвежско-британским коллективом, учитывались изменения в размере зрачков и активности голубого пятна при отслеживании разного количества движущихся точек [8]. Размер зрачка регистрировался при помощи пупиллометрии: этот метод позволяет с большой точностью отследить изменения диаметра отверстия, которое пропускает свет на сетчатку глаза. Активность мозга считывалась при помощи одного из самых популярных методов в функциональной нейробиологии — функциональной магнитно-резонансной томографии (фМРТ). При проведении фМРТ учитывается сигнал от насыщенного кислородом гемоглобина: чем больше такого гемоглобина в определенной части мозга, тем активнее она работает. После обработки данных стало ясно, что:
Эти результаты демонстрируют, что изменение активности голубого пятна у человека связано с изменением объема и направленности его внимания.
Рисунок 5. Корреляция между размером зрачков и количеством отслеживаемых движущихся точек.
Важно помнить
Память — это основа нашей личности, но запоминаем мы не каждый день своей жизни. В памяти чаще всего запечатлевается эмоционально окрашенная информация. Однажды я прочел частное жизнеописание одной женщины, составленное родственниками с ее слов. Тогда меня удивило, что бόльшую часть текста составляли события времен Великой Отечественной войны. Она мало говорила про свою жизнь и жизнь семьи после 1945-го года, хотя жила она долго. Можно бесконечно спорить, что запоминается лучше — хорошее или плохое (об экспериментах, посвященных механизмам запоминания мошенников и добропорядочных граждан, например, рассказано в статье [9]). Сейчас же нас интересует, как в человеческом мозге осуществляется избирательное запоминание.
При эмоциональном возбуждении в нашем организме вырабатываются адреналин и кортизол — широко известные гормоны стресса. Интересно, что их воздействие на память осуществляется не в момент совершения действия или обучения, а уже после их завершения. Например, введение кортикостерона (аналог человеческого кортизола) мышам в гиппокамп улучшает запоминание правильного способа выполнения задания [10], но использование адреноблокаторов — препаратов, мешающих связыванию адреналина с рецепторами, — ухудшает запоминание [11]. Скорее всего, глюкокортикоидные гормоны могут улучшить запоминание, если миндалевидное тело (центр эмоционального реагирования в нашем мозге) активировано при помощи норадренергической системы. Основной объем работы производят усеченные условные рефлексы, которые настраивают память на запоминание тех или иных событий или деталей.
Интересно, что при помощи фМРТ можно выявить отдельные функциональные сети в мозге, которые активируются при успешных и неуспешных действиях человека [12]. Успешные действия вызывают активацию голубого пятна и дорсолатеральной префронтальной коры, а ошибочные — системы «голубое пятно — поясная кора» (поясная кора — центр определения ошибок нашего мозга). Первая связь может напрямую влиять на принятие решений путем выработки поведенческих стратегий и их коррекции.
Больше или меньше
Очень близким понятием к вниманию и возбуждению в биологии поведения является стресс. Мы привыкли к тому, что термин «стресс» несет негативный смысл, но в широком смысле стресс — это реакция на новое. Как мы уже знаем, появление чего-то нового в нашем поле восприятия меняет активность мозга, что происходит путем перестройки работы голубого пятна. Стрессовая реакция запускается после возбуждения голубого пятна и ряда дополнительных, не входящих в него, норадренергических структур. Активность норадренергической системы может быть повышена (гиперфункция) и вызывать тревогу и стресс, но также существуют состояния ее пониженной функции (гипофункция), что приводит к соответствующим эффектам (табл. 1).
| Повышенная активность НАС | Сниженная активность НАС | |
|---|---|---|
| Возбуждение | Повышенная возбудимость | Заторможенность |
| Сон | Бессонница | Сонливость |
| Эмоции | Страх, тревога, агрессия | Притупление чувств, апатия |
| Дефицит норадреналина приводит к затормаживанию, снижению интенсивности всех психических процессов. В случае с избытком всё происходит с точностью до наоборот. | ||
Если посмотреть на таблицу, то можно сообразить, что все психические расстройства могут быть поделены на две группы в зависимости от того, в каком состоянии — гипо- или гиперфункции — находится норадренергическая система нашего организма. Повышенная активность этой системы наблюдается при психических нарушениях, которые сопровождаются тревогой и возбуждением: посттравматическом стрессовом расстройстве, панических атаках и маниакальных состояниях. С депрессией и шизофренией дело обстоит сложней. В случае депрессии существуют широко известные варианты болезни с подавленностью и сниженным настроением. Однако есть клинические случаи депрессии, при которых серьезную часть симптоматики представляют тревога и возбуждение. В первом случае активность норадренергической системы будет снижена, а во втором — наоборот [13].
Шизофрения, как я рассказывал ранее в материале про дофамин [1], представляет собой комплекс симптомов, которые могут быть поделены на три группы — позитивные (бред, галлюцинации), негативные (уменьшение яркости эмоций, снижение активности) и когнитивные (нарушение обработки информации). Как уже можно было догадаться, негативная симптоматика связана с гипоактивацией норадренергической системы, а позитивная вызывается ее повышенной активностью [14].
На этом описание норадренергической системы можно считать законченным, хотя и не полным. В целом картина с тремя основными нейромедиаторами выглядит следующим образом. Дофаминовая система — это генеральный директор компании «Мозг». Он управляет общим вектором развития, и его решения порой могут иметь не самые рациональные основания. Серотониновая система — менеджеры и управляющие, на долю которых выпала организация и упорядочивание всей работы. Норадреналин в этой фирме — исполнительный директор, щедро раздающий указания и распределяющий ресурсы. Совместная деятельность этих «управленцев» создает нашу психику, наше «Я», которое напрямую зависит от генов, задействованных в работе этих систем, и структуры самого мозга, которая меняется на пути индивидуального развития каждого человека.
Биомаркеры расстройств тревожного спектра
Биомаркеры определяются как анатомические, биохимические или физиологические признаки, специфичные для определенных расстройств или синдромов. В настоящее время ни один из предполагаемых биомаркеров не является достаточным и специфичным в качестве диагностического инструмента, однако, в литературе накопилось множество высококачественных исследований, которые должны улучшить наше понимание нейробиологических причин расстройств тревожного спектра.
Биохимические биомаркеры
Плазма крови, по-видимому, является рациональным источником протеомных, липидомных и других метаболических нарушений, возникающих при психических расстройствах, поскольку она легко доступна, причем, несколько молекул из мозга переходят через гематоэнцефалический барьер и достигают периферического кровообращения. Люмбальная пункция является инвазивным методом, а состав спинномозговой жидкости (CSF) не отражает точно нейрохимию в клетках головного мозга.
Целенаправленное поведение стимулируется дофамином (DA), и дофаминовые нейроны считаются субстратом для внутримозговой самостимуляции. Норадреналин (норадреналин; NE) связан с «эмоциональной памятью» и консолидацией и восстановлением эмоционального возбуждения, вызванного определенным поведением. Нейроны NE регулируют уязвимость к социальному поражению посредством ингибирующего контроля нейронов DA вентрально-сегментарной области.
Серотонин
Было обнаружено, что уровни 5-НТ в плазме, измеренные с помощью высокоэффективной жидкостной хроматографии, были значительно ниже у пациентов с PDA по сравнению с контрольными добровольцами. Кроме того, в исследовании мужчин с PDA концентрации 5-HT в сыворотке крови измеряли с помощью иммуноферментного анализа. Авторы сообщили о более низком уровне 5-НТ в сыворотке у пациентов по сравнению с контрольной группой на начальном этапе, который после лечения с применением селективного ингибитора обратного захвата серотонина (СИОЗС) пароксетина еще больше снизился, хотя наблюдались улучшения симптомов.
Другой подход к измерению нарушения 5-НТ заключается в измерении антител, направленных на систему 5-НТ, таких как анти-серотониновые и 5-НТ антиидиотипические антитела (направленные на рецепторы серотонина). Используя этот подход, Coplan et al. (1999) показали значительно повышенные уровни анти-серотониновых и серотониновых антиидиотипических антител в плазме у пациентов с паническим расстройством по сравнению с контрольной группой. Эти данные свидетельствуют о аутоиммунном механизме, нарушающем 5-HT систему в PDA.
γ-аминомасляная кислота
Нейропептиды.
В некоторых исследованиях изучалось влияние лечения на ось HPA у пациентов с PDA. Ночная экскреция кортизола с мочой не менялась во время лечения пароксетином по сравнению с плацебо в сочетании с релаксационными тренировками или аэробными упражнениями. Напротив, тренировка с физической нагрузкой была связана с пониженным уровнем кортизола в слюне у пациентов с паническим расстройством.
Глюкокортикоиды
Лечение глюкокортикоидами, по-видимому, резко уменьшает симптомы специфической фобии и может иметь пролонгированный эффект в отношении исчезновения страха, особенно в сочетании с терапией психотерапевтического воздействия. Таким образом, у субъектов с фобией паука повторное пероральное введение кортизона (25 мг) за 1 ч до экспонирования на фотографиях паука значительно уменьшило фобическую (но не общую) тревогу по сравнению с плацебо, и этот эффект сохранялся в течение 2 дней. Кроме того, пациенты, опасающиеся высоты, которые проходили три сеанса воздействия в виртуальной реальности после приема кортизола (20 мг) за 1 час до каждого сеанса, продемонстрировали значительное снижение страха, а также снижение острой тревоги и проводимости кожи во время воздействия фобии. стимулы.
Нейротрофины
После вливания апоморфина, а также вливания солевого раствора у пациентов с ОКР наблюдалось более высокое повышение уровня кортизола, чем у здоровых контроля. Реакции кортизола на введение солевого раствора и клонидина были одинаковыми у пациентов и контрольной группы. В исследовании молодых людей, страдающих ОКР были обнаружены более высокие ранние утренние значения кортизола по сравнению со здоровыми контролями. Уровни кортизола в группе ОКР снижались в ответ на психологический стрессор (воздействие опасного стимула или пожарной тревоги), в то время как у здоровых контролей было обнаружено увеличение кортизола.
В исследовании, использующем глубокую стимуляцию головного мозга для ОКР, увеличение обсессивно-компульсивных и депрессивных симптомов сильно коррелировало с повышением уровня свободного кортизола в моче после выключения устройства DBS.
Синдром постравматического стрессового расстройства
Нейрохимические процессы
Многие нейробиологические теории возникновения депрессии, на протяжении последних 40 лет большое значение уделяли дефициту различных медиаторов — химических веществ, с помощью которых передается по сетям нейронов возбуждение от одной нервной клетки к другой. В настоящее время известно более 30 медиаторов, главное отношение к депрессии имеют три — норадреналин, серотонин и дофамин.
Норадреналин проявляет свою активность, в первую очередь, в области гипоталамуса и других структур лимбической системы. С его действием обычно связывают реакцию на стресс, физиологические влечения, эмоции, некоторые процессы памяти. Серотонин перемещается по тем же нервным волокнам, но образуется в нейронах, имеющих отношение к чувству тревоги и нарушениям сна. Дофамин главным образом связан с эмоциональной сферой человека.
Связи между нейронами мозга обусловлены особой пластичностью нервной системы и зависят от наследственных факторов, личностных особенностей человека и тех ситуаций стресса, которые имели место в его прошлом опыте. Между отростками нейронов существует узкий промежуток — щель или синапс, через который и передается нервный импульс. Перемещение нервного импульса через синапс от одной нервной клетке к другой осуществляется с помощью медиаторов. Прежде чем медиатор проявит свою активность сообщение должно изменить свою форму: из электрического импульса перейти в химический сигнал. Медиаторы накапливаются в аксоне, высвобождаются из него и через щель синапса поступают к другому нейрону. Каждый медиатор имеет свою химическую структуру, обладающую определенным тропизмом к специфическим рецепторам — воспринимающий сигнал области другого нейрона (один медиатор может подходить к различным типам рецепторов). После передачи сообщения от одного нейрона к другому медиатор открепляется от рецептора и возвращается в щель синапса, где он либо разрушается с помощью фермента (моноаминооксидаза), либо обратно включается в передающий нейрон (обратный захват).
В последнее время в патогенезе депрессии особое значение придается уменьшению плотности и чувствительности постсинаптических рецепторов норадренергических и серотонинергических систем.
Среди биологических теорий происхождения депрессии — моноаминовая теория является ведущей (Мосолов С.Н., 2002). Данная теория связывает развитие депрессии с дефицитом одного из трех основных биогенных аминов — норадреналина, серотонина, дофамина и связывает с ликвидацией этого дефицита механизм действия современных лекарственных средств, предложенных для лечения депрессии антидепрессантов.
Серотонин
В 70-х годах ХХ века получила развитие серотонинергическая теория возникновения депрессии (Лапин И.П., Оксенкруг Г.Ф., 1969, Coppen A. с соавт., 1976). Согласно данной теории, серотонин рассматривался как биологически активное вещество (биогенный амин) — медиатор, отвечающий за повышение настроения (тимоаналептический эффект), обеспечивающий контроль за уровнем агрессивности, внезапно возникающими влечениями (включая сексуальное), регуляцию аппетита, цикл «сон — бодрствование» и чувствительность к боли.
Ряд клинических наблюдений свидетельствовал о снижении уровня 5-ОИУК (5-гидроксииндолуксусной кислоты) — конечного продукта окисления серотонина в церебральной жидкости депрессивных больных (Murphy D., с соавт., 1978, Goodwin F., с соавт., 1978). Однако, степень редукции 5-ОИУК не коррелировала с выраженностью симптомов депрессии. Причем у большинства пациентов терапевтический эффект амитриптилина был значительно выше, чем мелипрамина, а после купирования симптомов депрессии содержание 5-ОИУК повышалось (Asheroft G. с соавт., 1966; Mendels J. с соавт., 1975, Murphy D. с соавт., 1978).
Было отмечено, что многие антидепрессанты, особенно СИОЗС и МАО уменьшаются содержание 5-ОИУК,возможно по механизму обратной связи за счет увеличение в синаптической щели серотонина.
В процессе исследования депрессии было выявлено заметное снижение уровня серотонина у лиц, склонных к самоубийству и людей с выраженными симптомами тревоги.
На основе гипотезы, предполагающей нарушения обмена серотонина, предпринимались попытки лечения депрессии с помощью его предшественников — триптофана и 5-гидрокситриптофана. Данный подход к лечению депрессии также базировался на том факте, что симптомы депрессии обычно обостряются при дефиците в диете триптофана (Murphy D. et al., 1972).
Результаты терапии триптофаном были неоднозначны. В одних случаях подтверждалась высокая эффективность триптофана, не уступающая эффективности лечения депрессии такими мощным антидепрессантом, как имипрамин (Михаленко И.Н., 1973, Van Praag H., 1981). Другие исследования свидетельствовали лишь о незначительных улучшениях состояния больных после приема триптофана (Murphy D. et al., 1974, Bowers M., 1974). Кроме того, некоторые авторы подчеркивали нестойкость положительного эффекта в результате его приема (Бовин Р.Я., Аксенова И.О., 1982).
Ряд исследователей приводил факты, заставляющие сомневаться в верности серотониновой гипотезы происхождения депрессии. Так, в частности, было обнаружено снижение показателей выделения серотонина как во время депрессии, так и в период повышенного настроения. Так Coppen A. et al. (1976) обнаружили снижение показателей экскреции серотонина как во время депрессии, так и в период мании. Кроме того, было отмечено снижение показателей метаболизма серотонина и в период клинического улучшения при лечении антидепрессантами (Bowers M., Lumbar G., 1974, Лапин И.П., 1989).
Существующие в литературе противоречия можно объяснить тем, что содержание 5-ОИУК скорее отражает периферическое звено метаболизма серотонина (Zis A., Goodwin F., 1982). Возможно, что нарушения метаболизма серотонина имеет место лишь у определенной части больных депрессией, в частности обусловленной внутренними нейроэндокринными факторами (Clure D., 1971, Asberg M., 1978, Gastpar M., 1978). Не исключалось участие в патогенезе депрессии индоламинов и других медиаторов (Shaw D. et al., 1977, Bunney W. et al, 1970).
В пользу серотонинергической гипотезы развития депрессии также свидетельствуют данные, касающиеся снижения плотности белков-транспортеров, осуществляющих обратный захват серотонина через пресинаптическую мембрану нервной клетки.
Исследователи полагают, что некоторое клиническое сходство тревоги и депрессии подразумевает одни и те же изменения нейробиологического субстрата. Предполагается, что тревога, связана с повышенной активностью систем мозга, чувствительных к серотонину. При тенденции к затяжному течению тревоги чрезмерная активность данных систем может привести к снижению уровней не только серотонина, но и норадреналина, что в конечном итоге приведет к развитию депрессии. Развитием данной модели можно считать теорию развития тревожно-агрессивной депрессии, провоцируемой стрессом, вызванной кортизолом и связанной с серотонином. Согласно этой теории к тревожно-депрессивному комплексу в данном случае присоединяется и агрессия.
У больных с повышенным уровнем тревоги и агрессивностью окончания нервных клеток мозга, чувствительные к серотонину функционируют на минимально допустимом уровне. В нормальных условиях слабость этой системы компенсируется. Однако, при стрессе она начинает проявляться, прежде всего, ограничением способности контролировать тревогу и агрессивность. Когда люди с признаками тревожно-агрессивной депрессией попадают в психотравмирующую ситуацию, у них возникает чувство напряженности и дискомфорта; активируется деятельность эндокринных органов (гипоталамус — гипофиз — надпочечники) и усиливается выделение гормона стресса — кортизола. При этом угнетение тканей нервной системы, чувствительных к серотонину под действием кортизола происходит быстрее и сильнее, чем у здорового человека. В результате больной теряет способность управлять тревогой и агрессивностью. Усиленная тревога и агрессивность в свою очередь влияют на настроение, обусловливая дальнейшее развитие депрессии.
С точки зрения некоторых ученых депрессия напрямую связана с направленной на себя агрессивностью. Было установлено, что при депрессии показатели агрессивности значительно превышают норму и доминируют над показателями состояния агрессии, направленной во вне. На основании вышесказанного, был сделан вывод о взаимосвязи между тревогой, агрессией и депрессией, как поступательно обусловленными феноменами. Биологическими основами подобной взаимосвязи могут быть изменения концентрации продуктов распада серотонина, в связи с изменением уровня агрессии, направленной на самого себя.
Катехоламины
В середине ХХ века J. Shildkraut (1961) была сформулирована, так называемая, катехоламиновая теория происхождения депрессии. Данная теория предполагала нарушение регуляции системы мозга, чувствительной к норадреналину в качестве одного из важных звеньев патогенеза депрессии во время депрессии (Praag H., 1994; Ашмарин И.П., с соавт., 1999).
В настоящее время известно, что содержание норадреналина в клетках мозга контролируется особыми окончаниями нервной клетки — пресинаптическими адренорецепторами. Стимуляция этих рецепторов тормозит высвобождение норадреналина, что в свою очередь, приводит к его недостатку в синапсе и уменьшению нейротрансмиссии. Блокада данных рецепторов антидепрессантами, напротив, приводит к усилению процесса выделения норадреналина.
Фундаментальные исследования ретикулярной формации мозга показали, антидепрессанты, действие которых направлено на изменения содержания норадреналина, обладают общим активирующим или психостимулирующим эффектом. Эти препараты поддерживают уровень бодрствования, способствуют улучшению процессов восприятия, мышления, памяти и повышают концентрацию внимания. Однако, несмотря на то, что прием антидепрессантов практически сразу же повышает уровень норадреналина, клинический эффект препарата проявляется значительно позже.
Согласно катехоламиновой гипотезе J. Schildkraut. (1978) развитие депрессий, особенно эндогенных, обусловлено снижением содержания катехоламинов, главным образом норадреналина, в определенных структурах мозга. Также предполагалось, что функциональную активность норадренергических систем во время депрессии можно косвенно оценить по содержанию в моче такого метаболита норадреналина, как МОФЭГ (З-метокси-4-оксифенилэтилленгликоль).
На основании целого ряда наблюдений (Schildkraut J., 1978, Beckmann H., Goodwin F., 1980), было высказано предположение, что уровень МОЭФГ может служить предиктором эффективности терапии для различных антидепрессантов. У депрессивных больных с более низким содержанием МОФЭГ возможен положительный терапевтический эффект от имипрамина и дезипрамина, но они устойчивы к терапии амитриптилином.
Было высказано предположение, что у данной группы больных первично доминируют нарушение метаболизма норадреналина. Напротив, депрессивные больные с высоким суточным уровнем экскреции МОФЗГ лучше реагируют на терапию амитриптилином. В то же время, было показано, что у психически здоровых людей суточная экскреция МОФЭГ колеблется в четыре раза, и эти колебания перекрывают параметры сдвигов, отмеченных у пациентов, страдающих депрессией (Hollister L. с соавт., 1978). Кроме того, было выявлено, что в период клинической ремиссии обнаруженные у больных депрессией сдвиги катехоламинов не нормализуются и даже во время тяжелой депрессии содержание катехоламинов может быть в пределах нормы. (Cazzulo С., Sacchetti E. с соавт., 1982).
На основе данных, полученных J. Costa, E. Silva (1980) возникла теория предполагающая наличие двух вариантов возникновения депрессии, один, связанный с истощением норадреналина и более чувствительный к лечению одними антидепрессантами (дезимипрамин или имипрамин) и другой — связанный с дефицитом серотонина и реагирующий на терапию другими препаратами (амитриптилин). Допускалось, что антидепрессанты оказывают свое терапевтическое влияние путем облегчения передачи, как норадреналина, так и серотонина (Haefely W., 1985).
Последние исследования в области физиологии мозга показали, что система мозга, чувствительная к норадреналину обладает выраженным влиянием на систему, чувствительную к серотонину. Оказалось, что нервные клетки, чувствительные к норадреналину контролируют скорость высвобождения серотонина посредством влияния на окончания нейронов, расположенных на телах серотонинергических нейронов. Увеличение же возбудимости серотонинергических нейронов в свою очередь усиливает выброс серотонина в нервных окончаниях (De Boer T., с соавт., 1994).
Дофамин
В основе патогенеза депрессии может также лежать недостаток еще одного биологического вещества, в какой-то мере, являющегося предшественником норадреналина — дофамина. Предполагается, что он принимает участие в регуляции функции моторной сферы, обладает психостимулирующим эффектом и отвечает за формирование определенного поведения (Мосолов С.Н., 2002). Доказательством этой гипотезы служит способность препарата L-ДОФА,являющегося предшественником дофамина и норадреналина, способствовать переходу депрессии в состояние повышенной активности (Bunney W. С соавт., 1970; Van Praag H., 1977). При использовании L-ДОФА у пациентов, страдающих депрессией, достаточно часто отмечался положительный эффект в виде изменения активности. Так, в частности, Р.Я. Бовин, И.О. Аксенова (1982) при использовании L-ДОФА у терапевтически-резистентных депрессивных больных отметили положительный эффект в виде повышения психомоторной активности в 25% случаев.
Кроме того, к депрессии может привести прием медикаментов, понижающих содержание дофамина, например, препаратов раувольфии. Снижение уровня дофамина наблюдается при ряде неврологических и соматических заболеваний, также сопровождающихся депрессией, например, таких как болезнь Паркинсона.
Эндорфины и другие нейромедиаторы
Кроме медиаторов при депрессии могут быть изменения со стороны эндорфинов — нейропептидов, биологически активных веществ, обладающих свойствами гормона и медиатора одновременно. Эндорфины отвечают за восприимчивость человека к болевым ощущениям. Низкое содержание эндорфинов при дистимии объясняет плохую переносимость боли у людей, страдающих депрессией.
При расстройствах депрессивного спектра выявляются нарушения синаптической передачи, преимущественно относящиеся к тормозным ГАМК-эргическимсистемам мозга (отмечено снижение гамма-аминомасляной кислоты во время депрессии). Выделяясь в кровь гамма-аминомасляная кислота понижает уровень тревоги. Она также принимает участие в регуляции потока нервных импульсов, блокируя высвобождение других медиаторов, например, дофамина и норадреналина. Вследствие этого, происходит дезорганизация взаимодействия нервных клеток, осуществляющих обработку сенсорной (экстра- и интероцептивной) информации и интеграцию моторной и регуляторной активности. При этом возникают различные расстройства психической деятельности с соответствующими неврологическими и вегетативными проявлениями (Экклс Дж., 1971; Гусельников В.И., Изнак А.Ф., 1983; Глезер В.Д., 1985).
При депрессии происходит изменение концентрации биологически активных веществ не только между нервными клетками, но и внутри нейронов. Эти вещества в стенке нервной клетки расщепляются на более мелкие составные части, которые повышают активность нейронов, путем изменения направления движения медиаторов к центру нейрона, к его ядру.