какая информация необходима продолговатому мозгу для управления процессом вдоха и выдоха
«Ни один из вдохов не похож на другой»: как мозг регулирует работу легких
Теории и практики
Сердечный ритм, терморегулирование, секреция желез и работа многих других систем организма не зависит от нашего сознательного участия. Но, в отличие от всех этих процессов, дыхание бывает как произвольным, так и автономным, и отвечают за это разные участки мозга. Иногда даже в одном конкретном цикле дыхания происходит разделение труда: автономный вдох и произвольный выдох. С дыханием связаны и другие интересные вопросы. Почему выдох почти в два раза длиннее, чем вдох? Для чего мы зеваем и отчего икаем? Каковы причины синдрома внезапной детской смерти? И зачем дышать в пакет, если у вас паника? Обо всем этом — в отрывке из книги «Захватывающий мир легких» пульмонолога Кая-Михаэля Бе.
Захватывающий мир легких
Кай-Михаэль Бе
Попурри. 2019
пока больной находился в сознании, у него было регулярное глубокое дыхание, а стоило ему уснуть, как оно останавливалось, словно кто-то выдернул шнур из розетки.
Но следующего ночного эпизода и очередной комы пациент уже не перенес. На фоне кислородного голодания у него случился инфаркт, и вскоре он умер. Поразило его «проклятие Ундины».
Американские врачи впервые описали этот редкий и загадочный случай в 1962 году. Вскоре феномен повторился у трех пациентов, перенесших операцию на мозге: в состоянии бодрствования все они дышали совершенно нормально, но, как только наступала ночь и они засыпали, дыхание останавливалось. Если их вовремя не будили, возникал серьезный дефицит кислорода, угрожавший жизни. Такая непроизвольная потеря организмом своих функций напомнила врачам легенду о русалке Ундине: для обеспечения верности любимого, жившего на суше, она заколдовала его таким образом, чтобы в случае измены он утрачивал контроль над вегетативными жизненными функциями. Поэтому врачи, описывавшие случаи непроизвольной ночной остановки дыхания, назвали это заболевание «проклятием Ундины». Персонаж Ундины вдохновил Ханса Кристиана Андерсена на написание сказки «Русалочка», а Уолт Дисней снял на ее основе мультфильм. Разумеется, в нем не было ни смертей, ни остановок дыхания и все жили счастливо до скончания веков!
Что же кроется за этим «проклятием»?
Мозг управляет как произвольным, так и автономным дыханием, но отвечают за это разные его участки.
Главный дыхательный центр человека находится в глубине головного мозга неподалеку от его перехода в спинной мозг. Это так называемый продолговатый мозг, а точнее говоря, его часть, носящая название «мост». Здесь находятся нервные клетки, которые, подобно метроному, регулярно посылают импульсы, активизирующие дыхание, что обеспечивает спокойный равномерный ритм дыхания, составляющий от 10 до 15 вдохов в минуту, в том числе и во сне. Командный центр в продолговатом мозге связан нервными волокнами спинного мозга с дыхательными мышцами. Эти волокна на уровне третьего шейного позвонка отходят от спинномозгового канала, образуя правый и левый диафрагмальные нервы, которые спускаются через грудную полость к диафрагме. Поэтому повреждения шейного отдела позвоночника всегда несут в себе угрозу для жизни. В отличие от поперечного поражения спинного мозга в грудном или шейном отделе, при котором наступает паралич, здесь речь идет о полном отказе дыхания. Неконтролируемое возбуждение этих нервов выражается в таком неприятном явлении, как икота. Ее причиной становятся внезапные подергивания диафрагмы под влиянием случайных нервных импульсов.
Но дыхательный центр представляет собой не только передающую, но и принимающую станцию, которая также важна для регулирования дыхания. В частности, он должен реагировать на изменения потребности организма в воздухе в зависимости от физической нагрузки и соответствующим образом регулировать частоту дыхания. Эту информацию дыхательный центр в первую очередь получает от так называемых хеморецепторов — датчиков, которые расположены на стенках аорты и в самом продолговатом мозге и которые реагируют на изменения содержания углекислого газа и кислорода в крови. Кроме того, в крупных группах мышц существуют датчики растяжения, передающие в мозг сигналы об усиленной деятельности мышц, чтобы тот повысил частоту дыхания. Возникает своего рода замкнутая цепь автоматического регулирования. При повышении активности мышц увеличивается расход кислорода для восполнения энергии, а за счет этого растет выработка углекислого газа. Совместно с другими отходами производства в мышцах, такими, например, как соединения молочной кислоты, углекислый газ вызывает повышение кислотности крови. Оба фактора — высокое содержание углекислого газа и изменение показателя рН — активизируют датчики в аортах и мозге, а тот, в свою очередь, увеличивает частоту импульсов дыхания. Диафрагма совершает более глубокие и частые движения, вследствие чего из организма выводится больше углекислого газа, а в него поступает больше кислорода. Уровень рН нормализуется. Регулирующая цепь замыкается, и частота дыхания вновь снижается.
Как ни странно, дыхательный центр буквально помешан на углекислом газе.
Как бы ни был важен кислород для выработки энергии и поддержания жизнедеятельности органов, все датчики центра дыхания заботятся исключительно об удалении отходов, реагируют только на изменения концентрации углекислого газа и показателей кислотности крови. Колебания содержания кислорода их абсолютно не волнуют, и на это есть веская причина: почти все процессы обмена веществ в организме протекают только при определенных показателях рН. Так что поддержание их стабильности — главная задача продолговатого мозга.
Кроме того, дыхательный центр получает нервные импульсы от других областей мозга, в частности от гипоталамуса. Это приводит к тому, что характер дыхания непроизвольно меняется под влиянием таких эмоций, как грусть, радость, возбуждение, гнев, агрессия, влюбленность. Произвольное управление дыханием осуществляется в коре головного мозга. Она способна вносить изменения в основной ритм, задаваемый продолговатым мозгом, когда дыхание требуется для других процессов, обычно для речи. Но если кора мозга отдыхает (например, во сне), то командование автоматически берет на себя продолговатый мозг.
Иногда даже в одном конкретном цикле дыхания происходит разделение труда: автономный вдох и произвольный выдох.
Ведь, в отличие от вдоха, который осуществляется за счет активного сокращения диафрагмы и расширения грудной клетки, выдох почти всегда является чисто пассивным процессом: легкие, грудная клетка и диафрагма просто возвращаются в исходное состояние, словно растянутая пружина, с которой сняли нагрузку. На этот возврат мозг отводит определенное время. У здоровых людей выдох длится примерно вдвое дольше, чем вдох. Если процесс затягивается (например, из-за снижения эластичности легких вследствие заболевания), мозг включает режим активных усилий для выдоха, чтобы оставаться «в графике». То же самое происходит и при высокой частоте дыхания, когда организм работает под нагрузкой, — в этой ситуации продолжительность обычного пассивного выдоха была бы слишком большой. Однако при всей гармонии бесспорным остается одно: автономная составляющая контроля дыхания играет доминирующую роль. Попробуйте сами задержать дыхание, насколько возможно. В итоге все равно победит продолговатый мозг.
Нарушения в работе дыхательного центра — это всегда тяжелейшие заболевания.
У пациентов с «проклятием Ундины» структуры продолговатого мозга, контролирующие непроизвольное дыхание во сне, полностью или частично разрушены, например в результате инсульта.
Могут сказаться также травмы, новообразования и инфекции. Существует и врожденная форма «проклятия». Если кора мозга исправно выполняет свои функции, то в состоянии бодрствования она подменяет продолговатый мозг. Чтобы не лишать пациентов сна, по ночам их приходится подключать к аппарату искусственной вентиляции легких или устанавливать электрический стимулятор работы диафрагмы.
Бесперебойная работа продолговатого мозга важна еще и потому, что он не только управляет вегетативными функциями во сне, но и контролирует их. Едва возникают экстренные ситуации (снижение артериального давления, болевые импульсы из различных частей тела, изменение содержания углекислого газа в крови), он тут же поднимает по тревоге кору головного мозга, и человек моментально просыпается. К сожалению, эта хитроумная система «сдержек и противовесов» не всегда работает идеально. Как и все сложные процессы управления центральной нервной системой, она нуждается в развитии и обучении.
Особенно трагичным примером сбоя в системе является синдром внезапной детской смерти. У малышей по неизвестной причине оказывается нарушена система аварийной сигнализации при отказе дыхания.
Паузы в дыхании, которые у младенцев возникают регулярно и являются признаком «обучения» дыхательного центра, внезапно перестают давать мозгу сигнал к пробуждению, и ребенок умирает во сне без видимых причин. Это кошмар для любого родителя.
Источник: A24 / giphy.com
Другое, значительно более частое, но в большинстве своем не опасное нарушение контрольных функций дыхания носит название гипервентиляционного синдрома. Эмоциональное или психическое возбуждение, вызванное, к примеру, страхом либо паникой, приводит к чрезмерной стимуляции дыхательного центра в продолговатом мозге.
Глубокое ускоренное дыхание снижает уровень углекислого газа в крови, а показатель рН растет, создавая щелочную реакцию. Следствием становятся судороги, головокружение и помрачение сознания.
Эти симптомы дополнительно усиливают ощущение страха в гипоталамусе, и возникает заколдованный круг. Если пациент не может успокоиться самостоятельно, то нормализовать его состояние помогает повторное вдыхание выдыхаемого углекислого газа (для этого достаточно приложить ко рту полиэтиленовый пакет и подышать из него). Симптомы исчезают, и эмоциональное возбуждение затихает. Таким образом, если у вашей начальницы опять начинается «гипервентиляция», отнеситесь к этому снисходительно — возможно, все дело в гипоталамусе. В таких случаях достаточно энергичного возгласа: «Задержи дыхание!» Подобный приказ должен восприниматься не как неуместная дерзость, а как ценная медицинская рекомендация, заменяющая применение полиэтиленового пакета: благодаря этому углекислый газ временно перестает удаляться из организма, его содержание в крови нормализуется, а состояние опять приходит в норму. Кора мозга вмешивается в процесс, разрывая цепь между гипоталамусом и продолговатым мозгом. Данный пример демонстрирует, что, когда речь идет о вегетативных последствиях эмоционального всплеска, не надо безучастно наблюдать за происходящим. Вы можете взять на себя командные функции нервной системы и повлиять на ситуацию. Тесная связь эмоций, автономной нервной системы и произвольного контроля дыхания открывает широкие возможности. По крайней мере, один из элементов этой цепи находится под вашим личным контролем! Необходимо только освоить приемы, с помощью которых можно влиять на собственное самочувствие, сознательным усилием успокаивать вегетативную нервную систему. […]
Что же передают легкие по своим каналам? Пустые сплетни? Или мы имеем дело с неиспользуемыми избыточными мощностями? Отнюдь, от легких поступает не меньше информации, чем от органов чувств, но все эти сведения перерабатываются мозгом в подсознании. Правда, есть исключение: раздражение, приводящее к рефлекторному кашлю, или нехватка воздуха воспринимаются напрямую, как и сигналы от органов чувств. Но информация, обрабатываемая подсознанием, влияет на другие автономные функции организма, например на артериальное давление, сердечный ритм, пищеварение, потоотделение, проявление эмоций… А также на психические процессы.
Какую же информацию посылают легкие, если речь не идет об оптических и акустических сигналах, болевых либо тактильных ощущениях? Почти все эти сигналы имеют химическую или физическую природу. Хотя процесс дыхания и выглядит монотонным, ни один из 15 вдохов, которые мы делаем в минуту, не похож на другой, ведь каждый литр вдыхаемого воздуха особенный. Легкие относятся к воздуху не как потребитель, а как тонкий ценитель. Подобно сомелье, который находит в крошечном глотке вина привкусы дубовой бочки, земли, абрикоса, персика, сигары и мокрой кожи, легкие во вдыхаемом воздухе выделяют такие параметры, как температура, влажность, содержание солей, показатель рН, состав газов. Кроме того, воздух может содержать раздражающие и вредные вещества, чужеродные частицы, аллергены.
В легких, как и на языке и в носу, имеются вкусовые сосочки и рецепторы запахов.
Они могут выявлять продукты бактериального обмена веществ и определять на вкус многие яды. У них есть такие же рецепторы, которые в носу и во рту воспринимают, к примеру, освежающий аромат растительных эфирных масел. Но поскольку обработка сигналов от этих рецепторов в легких происходит без участия сознания, то мы можем только догадываться, какой эффект раздражители оказывают на дыхательные пути и автономную нервную систему. Бесспорно лишь то, что для распознавания, различения и измерения всех этих компонентов нужны очень чувствительные нервы. А их в легких хватает.
Чувствительные нервные волокна легких начинаются там, где можно собрать максимум информации: в бронхиальных мышцах, железах, альвеолах и, прежде всего, в эпителии. Здесь происходят главные события. Зачем же прокладывать линии передач от клеток соединительной ткани, в которых ничего не случается, если рядом бурлит жизнь? Эпителий дыхательных путей предлагает самую лучшую и разнообразную программу. Там регулярно происходят неприятности и скандалы, обеспечивающие самый высокий зрительский рейтинг! Не все волокна передают сенсации из эпителия, некоторым приходится довольствоваться скучной, но важной работой датчиков растяжения тканей. Их сигналы имеют большое значение, потому что они в буквальном смысле защищают легкие от разрывов. Когда легкие под воздействием диафрагмы достигают определенной степени растяжения, датчики посылают в дыхательный центр продолговатого мозга сигнал стоп. Мозг в свою очередь прекращает сокращение диафрагмы и подает сигнал на начало выдоха. Главное — ничего не порвать.
Спортсмены знают, насколько важна растяжка как средство профилактики травм. Легкие тоже время от времени осуществляют спонтанную растяжку — во время зевания.
Если дыхание на протяжении длительного времени носит спокойный и поверхностный характер, то датчики растяжения начинают скучать и вызывают зевательный рефлекс. Точно так же как мы устраиваем дома сквозняк, чтобы быстро проветрить комнаты.
Но вернемся к нервным окончаниям эпителия дыхательных путей. Здесь размещается густая сеть рецепторов, реагирующих на химические и физические раздражители, которыми могут быть частицы пыли, вещества, растворенные в водяных парах, продукты жизнедеятельности бактерий, соляная кислота, капсаицин, отвечающий за жгучий вкус перца чили, слизь, а также сигнальные вещества иммунной системы, выделяемые при воспалениях, и даже холод и тепло. Нервы сообщают обо всем, что оказывает на них воздействие. В здоровом состоянии их чувствительные окончания защищены эпителием дыхательных путей, но, если он поврежден, окончания лишаются защиты, выступают над поверхностью и начинают реагировать на раздражения. Самыми частыми причинами повреждений эпителия являются простудные вирусы и воспаления, возникающие, к примеру, в результате аллергии, инфекции или контакта с вредными веществами. В этом случае чувствительные нервные окончания посылают мозгу сигналы тревоги, который отвечает на них защитными рефлексами бронхов, устраняющими причину раздражения или предотвращающими его распространение на более глубокие участки дыхательных путей. К таким рефлекторным реакциям относятся кашель, выработка слизи и спазм бронхиальных мышц.
Чувствительные нервные окончания эпителия особенно интересны в плане изучения хронических заболеваний дыхательных путей. По своим функциям в бронхах они удивительно напоминают рецепторы, фиксирующие повреждения кожи, — ноцицепторы. Задача последних заключается в том, чтобы предупреждать мозг о грозящих повреждениях кожи в результате внешнего воздействия. Создавая болевое ощущение, они провоцируют немедленную реакцию, например отдергивание руки от горячей кухонной плиты. В дыхательных путях в таких случаях вместо боли возникает кашель.
Как и болевые рецепторы кожи, чувствительные нервные окончания в легких могут подвергаться постоянному раздражению. Если в первом случае отмечаются хронические боли, то во втором — хронический нескончаемый кашель, который может продолжаться несколько месяцев.
Пока неясно, каким образом можно нормализовать нарушенный рефлекс кашля. Но то, что существует принципиальная возможность манипулировать степенью возбудимости нервных окончаний, доказывают курильщики. Первоначальный рефлекторный кашель со временем исчезает, в противном случае все бы закончилось уже на первой сигарете. Обращает на себя внимание и еще один аспект, наблюдаемый у начинающих курильщиков: несмотря на сильный кашель, возникающий при курении первой сигареты, спазматического сужения бронхов практически не бывает. Таким образом, необязательно могут появляться все три рефлекторные реакции, иногда они делят обязанности между собой. Это подтверждается и повседневными наблюдениями практикующих врачей: лишь немногие астматики наряду с сужением бронхов страдают и сильным кашлем. При заболевании бронхитом у одних пациентов отмечается сухой кашель, а у других происходит чрезмерное образование слизи. Почему так бывает, нам пока неизвестно. […]
В рубрике «Открытое чтение» мы публикуем отрывки из книг в том виде, в котором их предоставляют издатели. Незначительные сокращения обозначены многоточием в квадратных скобках.
Мнение автора может не совпадать с мнением редакции.
Какая информация необходима продолговатому мозгу для управления процессом вдоха и выдоха
3.1 Нервная регуляция дыхания
Дыхательный центр представляет собой совокупность нейронов продолговатого мозга, обладающих ритмической активностью и определяющих ритм дыхательных движений. Бульбарный дыхательный центр выполняет две основные функции:
1) регуляцию двигательной активности дыхательных мышц (двигательная функция);
2) гомеостатическую, связанную с изменением характера дыхания при сдвигах газового состава и кислотно-основного равновесия в крови и тканях.
Двигательная функция дыхательного центра заключается в генерации дыхательного ритма и его паттерна (длительности вдоха, выдоха, величины дыхательного объема).
Нейроны дыхательного центра расположены в дорсомедиальной и вентролатеральной областях продолговатого мозга, образуя так называемую дорсальную и вентральную дыхательные группы. В указанных дыхательных группах расположены следующие виды нейронов:
1) ранние инспираторные, максимальная частота разряда которых приходится на начало инспирации;
2) поздние инспираторные нейроны, максимальная частота разряда – в конце инспирации;
3) полные инспираторные нейроны, характеризующиеся постоянной активностью в течение фазы вдоха;
4) постинспираторные нейроны, максимальный разряд которых обнаруживается в течение выдоха;
5)экспираторные нейроны, активность которых возрастает во второй части выдоха;
6) преинспираторные нейроны, максимальный пик активности проявляют перед началом вдоха.
В структурах бульбарного дыхательного центра различают так называемые респираторно-связанные нейроны, активность которых совпадает с ритмом дыхания, но они не иннервируют дыхательные мышцы, а обеспечивают иннервацию верхних дыхательных путей.
В соответствии с локализацией нейронов бульбарного дыхательного центра, различают дорсальную дыхательную группу (ДДГ) и вентральную дыхательную группу (ВДГ). Нейроны дорсальной дыхательной группы получают афферентные сигналы от легочных рецепторов растяжения по волокнам n. Vagus. Только часть инспираторных нейронов дорсальной группы дыхательного центра связана аксонами с дыхательными мотонейронами спинного мозга, преимущественно с контрлатеральной стороной.
Вентральная дыхательная группа расположена латеральнее обоюдного ядра продолговатого мозга, подразделяется на ростральную и каудальную части. Причем, ростральная часть вентральной дыхательной группы представлена ранними, поздними, полными инспираторными и постинспираторными нейронами.
Дорсальная и вентральная группы нейронов в правой и левой половинах продолговотого мозга взаимосвязаны как в пределах одной половины, так и с нейронами противоположной стороны. В синхронизации деятельности контрлатеральных нейронов бульбарного дыхательного центра участвуют проприобульбарные нейроны и экспираторные нейроны комплекса Бетцингера.
Таким образом, нейроны бульбарного дыхательного центра в зависимости от их значимости в регуляции внешнего дыхания разделяют на три группы:
1) нейроны, иннервирующие мышцы верхних дыхательных путей и регулирующие поток воздуха в дыхательных путях;
2) нейроны, синаптически связанные с мотонейронами спинного мозга и регулирующие активность мышц вдоха и выдоха;
3) проприобульбарные нейроны, участвующие в генерации дыхательного ритма, аксоны которых обеспечивают связь только с нейронами продолговатого мозга.
Подобно многим физиологическим системам контроля, система управления дыханием организована как контур отрицательной обратной связи.
Афферентация с различных рецепторных зон интегрируется в бульбарном дыхательном центре. Последний, в свою очередь, генерирует импульсацию к мотонейронам спинального отдела дыхательного центра, регулирующего сократительную активность дыхательной мускулатуры.
Важная роль в регуляции внешнего дыхания отводится центрам варолиева моста, в частности, пневмотаксическому центру. Последний включает медиальное, парабрахиальное ядро и ядро Келликера. В парабрахиальном ядре находятся преимущественно инспираторные, экспираторные и фазопереходные нейроны. Ядро Келликера содержит инспираторные нейроны.
Дыхательные нейроны моста участвуют в механизмах смены фаз дыхания, регулируют величину дыхательного объема.
Непосредственными регуляторами сократительной способности дыхательных мышц являются спинальные мотонейроны, получающие информацию по нисходящим ретикулоспинальным путям от бульбарного дыхательного центра.
Как известно, нейроны диафрагмального нерва расположены узким столбом в медиальной части вентральных рогов от СIII до CV. Подавляющее количество волокон диафрагмального нерва являются аксонами α-мотонейронов, а меньшая часть представлена афферентными волокнами мышечных и сухожильных веретен диафрагмы, а также рецепторов плевры, брюшины и свободных нервных окончаний самой диафрагмы.
Мотонейроны, иннервирующие межреберные мышцы, расположены в передних рогах спинного мозга на уровне TIV-TX, из них часть нейронов регулирует сокращения межреберных мышц, а другая часть – их позно-тоническую активность.
Обращает на себя внимание тот факт, что активность спинальных мотонейронов, обеспечивающих регуляцию двигательной активности межреберных мышц и диафрагмы, в свою очередь, находится под контролем инспираторных нейронов спинного мозга, расположенных на уровне СI-CII вблизи латерального края промежуточной зоны серого вещества.
В обеспечении дыхания, особенно в условиях патологии, участвуют мышцы брюшной стенки, получающие иннервацию от мотонейронов спинного мозга на уровне TIV-LIII.
Двум фазам внешнего дыхания (вдоху и выдоху) соответствуют три фазы активности бульбарного дыхательного центра: инспирация, пассивная контролируемая экспирация и активная экспирация. Во время фазы инспирации диафрагма и наружные межреберные мышцы увеличивают силу сокращения, активируются мышцы гортани, расширяется голосовая щель, снижается сопротивление потоку воздуха. В постинспираторную фазу дыхания происходит медленное расслабление диафрагмы, сокращение мышц гортани, выход воздуха в окружающую среду.
В фазе экспирации – экспираторный поток усиливается за счет сокращения внутренних межреберных мышц и мышц брюшной стенки.
Рефлекторная регуляция дыхания обеспечивается за счет афферентной импульсации в бульбарный дыхательный центр с различных рецепторных зон. Мощной рефлексогенной зоной является слизистая оболочка полости носа, где расположены различные типы механорецепторов, в том числе ирритантные, растяжения, а также болевой чувствительности, обоняния.
Возбуждение этих рецепторов возникает в момент каждого вдоха и приводит к формированию потока афферентной импульсации в ретикулярную формацию ствола мозга с последущей активацией бульбарного дыхательного центра, сосудодвигательного центра, гипоталамических и корковых структур мозга.
Раздражение ирритантных рецепторов слизистой оболочки носа приводит к рефлекторному сужению бронхов, голосовой щели, остановке дыхания на выдохе, развитию брадикардии, а в ряде случаев прекращению сердечных сокращений и другим изменениям (тормозной тригемино-вагусный рефлекс Кречмера ).
Слизистая трахеи и бронхов является слабой рефлексогенной зоной. В стенке крупных внелегочных бронхов и трахеи имеются высокопороговые, низкочувствительные медленноадаптирующиеся, быстроадаптирующиеся и промежуточные механорецепторы, в норме их роль в регуляции дыхания минимальна.
Чувствительность этих рецепторов возрастает при развитии воспалительного процесса в бронхолегочной системе инфекционной или аллергической природы, когда освобождаются медиаторы воспаления и аллергии: гистамин, кинины, лейкотриены, простагландины и др.. Возбудимость рецепторов трахеи и бронхов возрастает и в случае застойных явлений в малом кругу кровообращения, когда прежние объемы воздуха сильно растягивают стенки воздухоносных путей. Афферентация с рецепторов трахеи и бронхов направляется в бульбарный дыхательный центр по чувствительным волокнам n. Vagus, модулируя глубину и частоту дыхательных движений.
Мощной рефлексогенной зоной является паренхима легких, обеспечивающая не только альвеолярное дыхание, но и рефлекторную регуляцию внешнего дыхания.
Основные типы легочных вагусных афферентов включают: медленноадаптирующиеся рецепторы растяжения альвеол, быстроадаптирующиеся рецепторы, С-волокна.
Многочисленные быстроадаптирующиеся рецепторы (БАР) находятся в эпителии внутрилегочных бронхов и бронхиол. Эти рецепторы наиболее чувствительны к следующим типам раздражителей: ирритантным воздействиям, повреждению паренхимы и механическому раздражению дыхательных путей. Возбуждение БАР возникает также при глубоком дыхании, легочной эмболии и капиллярной гипертензии. Афферентация с этих рецепторов распространяется по чувствительным маломиелинизированным волокнам n. Vagus в ретикулярную формацию ствола мозга и бульбарный дыхательный центр, вызывая бронхоконстрикцию, тахипноэ, развитие кашля и тахикардии. Возбуждение этих рецепторов может быть клинически значимым в патогенезе бронхиальной астмы и нарушениях реактивности дыхательных путей.
По данным ряда авторов в паренхиме легких выделяют и БАР рецепторы спадения, реагирующие на спадение альвеол под воздействием внутрилегочных и внелегочных факторов. Афферентация с этих рецепторов поступает в бульбарный дыхательный центр по маломиелинизированным волокнам n. Vagus и обеспечивает развитие тахипноэ.
Медленноадаптирующиеся рецепторы растяжения – важная группа механорецепторов c вагусной афферентацией, расположенных в гладких мышцах воздухоносных путей. Частота импульсов с этих рецепторов возрастает по мере растяжения альвеол вдыхаемым воздухом и распространяется по толстым миелинизированным α-волокнам n. Vagus в бульбарный дыхательный отдел, обеспечивая формирование рефлекса Геринга-Брейера. Последний контролирует частоту и глубину дыхания, имеет физиологическое значение при дыхательных объемах превышающих 1 л (у взрослых при физической нагрузке). Рефлекс Геринга-Брейера более важен для регуляции дыхательного акта у новорожденных, а также в условиях патологии как один из механизмов реализации инспираторной, экспираторной и смешанной одышек.
Третьей группой легочных механорецепторов являются С-волокна – тонкие миелинизированные вагусные афференты. С – волокна оканчиваются в паренхиме легких, в бронхах и кровеносных сосудах, активируются экзогенными раздражителями и медиаторами альтерации. Активация С-волокон приводит к тахипноэ, брадикардии, гиперсекреции слизи. В состав С-волокон входят J-рецепторы, расположенные в альвеолярных перегородках в контакте с капиллярами (юкстакапиллярные рецепторы), чувствительные к интерстициальному отеку, легочной венозной гипертензии, микроэмболии, раздражающим газам и ингаляционным наркотическим веществам. Активация J-рецепторов вызывает закрытие гортани и апноэ, за которыми следует частое поверхностное дыхание, гипотензия и брадикардия.
Важная роль в рефлекторной регуляции дыхания отводится проприорецепторам суставов грудной клетки, межреберных мышц, диафрагмы, сухожильным рецепторам. Недостаточное укорочение инспираторных или экспираторных мышц усиливает импульсацию от мышечных веретен, которая через α-мотонейроны повышает активность α-мотонейронов и дозирует таким образом мышечное усилие.
В регуляции активности бульбарного дыхательного центра и внешнего дыхания принимает участие и афферентация с висцеральных рецепторов и рецепторов кожи, о чем свидетельствует развитие гипервентиляции легких при болевом и термическом раздражении.
3.2. Механизмы гуморальной регуляции дыхания
Важная роль в регуляции дыхания отводится хеморецепторам.
Изменения газового состава крови (РаО2, РаСО2) влияют на активность дыхательного центра путем возбуждения хеморецепторов каротидных и аортальных телец (периферические рецепторы), а также хеморецепторов вентральной зоны продолговатого мозга и дорсального дыхательного ядра (центральные рецепторы). Периферические хеморецепторы (рис.5) обеспечивают регуляцию частоты дыхательных движений. Адекватным раздражителем для них является уменьшение РО2 артериальной крови, в меньшей степени – увеличение РСО2 и снижение рН. Периферические хеморецепторы расположены у бифуркации общих сонных артерий на внутреннюю и наружнюю. Несмотря на свой миниатюрный размер, каротидные тельца интенсивно кровоснабжаются (1,4-2 л/мин на 100 г ткани). Этот орган особенно чувствителен к колебаниям кислорода в артериальной крови. При Ра О2 в пределах 60-80 мм рт. ст. наблюдается слабое усиление вентиляции, при Ра О2 ниже 50 мм рт. ст. возникает выраженная гипервентиляция легких. Ра СО2 и рН крови потенцируют эффекты гипоксемии на артериальные хеморецепторы и не являются адекватными раздражителями для этих рецепторов. После двустороннего удаления каротидных телец гипоксический вентиляторный ответ у человека исчезает. При отсутствии хеморецепторной стимуляции, например, при глубокой гипокапнии, повреждении синокаротидной зоны (опухоли, коллагенозы, травмы) ритмогенез дыхания снижается и полностью прекращается.
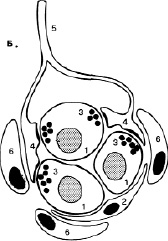
Рис. 5. Каротидное тельце: 1-хеморецепторные клетки; 2-поддерживающие клетки; 3-синаптические пузырьки; 4-чувствительные нервные окончания; 5-нервное волокно
Центральные хемочувствительные клетки реагируют на отклонения РСО2 и [H+] во внеклеточной жидкости внутримозгового интерстициального пространства, регулируют глубину вдоха. Гиперкапния и ацидоз стимулируют, а гипокапния и алкалоз тормозят центральные хеморецепторы.
Одной из причин высокой скорости вентиляторного ответа на гиперкапнию является легкость диффузии СО2 через барьерную систему кровь-головной мозг. Более того, повышенное РСО2 вызывает расширение сосудов, особенно церебральных, способствуя тем самым усилению диффузии СО2 через гемато-энцефалический барьер.