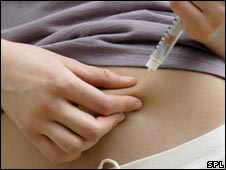
колоть гормон роста перед тренировкой
Курс гормона роста
Содержание
Курсы гормона роста [ править | править код ]
Данный курс гормона роста человека составлен в помощь начинающим атлетам для получения рельефной фигуры. Дозировки и комбинации взяты из научной литературы, они систематически используются атлетами различных видов спорта на практике и признаны наиболее эффективными и рациональными.
Кому подходят эти курсы гормона роста?
Гормон роста может применяться как мужчинами, так и женщинами в возрасте старше 20 лет (у более молодых людей может наблюдаться несимметричное развитие костей) для усиления рельефности мускулатуры. Общая масса увеличивается незначительно, это происходит в результате крупных потерь жира.
Побочные эффекты в ходе и после курса практически не наблюдаются, все они как правило носят обратимый характер.
Сертифицированные в РФ препараты гормона роста: (в порядке снижения популярности)
Прочие препараты гормона роста:
Курс №1: Гормон роста [ править | править код ]
Цель: Достижение рельефа, при наличии достаточной мышечной массы. Эффект омоложения, повышение упругости мышц, улучшение свойств кожи.
Курс: Гормон роста + Стероиды [ править | править код ]
Цель: Достижение рельефа и набор мышечной массы. Эффект омоложения, повышение упругости мышц, улучшение свойств кожи.
Альтернативным решением является применение гормона роста сразу после курса анаболических стероидов (как на массу, так и на сушку). Это позволяет максимально сохранить мышечную массу и дополнительно повысить рельефность.
Курс: Гормон роста + Жиросжигатели [ править | править код ]
Эффект: Сжигание жира, с получением рельефной фигуры. Эффект омоложения, повышение упругости мышц, улучшение свойств кожи.
Как разводить гормон роста [ править | править код ]
Гормон роста может быть только в виде сублимированного порошка. Количество порошка должно быть указано на ампуле. Количество может быть указано либо в единицах (ед.) или в миллиграммах (мг). Если количество указано в миллиграммах, то его можно перевести в единицы по формуле 1мг =
3 ед. (более точно 1мг=2,7ед.). Мы же в наших описаниях будем пользоваться формулой 1мг = 3 ед., потому что именно эта формула используется большинством производителей препарата.
Разведение [ править | править код ]
Как делать инъекции гормона роста [ править | править код ]

Предупреждение [ править код ]

Гормон роста для мужчин – за и против, зачем нужен, как влияет на мышцы и здоровье
Гормон роста – самый популярный препарат у профессионалов и любителей спорта. Касательно приема и его эффекта есть масса мнений: одни считают его одним из самых эффективных средств для продления жизни, другие утверждают, что он очень вреден для нашего организма. Давайте разбираться.
Механизм действия гормона роста
Гормон роста (соматотропин) – это белок, состоящий из 191-ой аминокислоты. Выработка и секреция данного гормона происходит в передней доле гипофиза (в эндокринной железе). В организме гормон роста производится в наибольшем количестве, чем все существующие гормоны гипофиза (тропные гормоны, стимулирующие синтез и секрецию гормонов периферических эндокринных желёз). Процесс производства длится на протяжении всей жизни: после 20 лет продукция гормона роста начинает уменьшаться на 15% в десятилетие. Уровень гормона достигает пика в раннем детстве, а секреция – в подростковый период (половое созревание, интенсивный линейный рост).
Основные функции гормона роста
Гормон роста ускоряет выработку факторов роста и мышечную массу, а также активно регулирует метаболизм костной ткани человека.
Гормон служит неким дежурным-доктором внутри организма, который угнетает активность ферментов, оказывающих разрушающее действие на аминокислоты. Также регулирует синтез коллагена в костной ткани и коже. Гормон роста увеличивает размер и количества клеток щитовидной железы, надпочечников, печени, половых желёз, вилочковой железы и мышц.
Еще препарат действует на распад жиров, что влияет на рост жирных кислот в крови, которые подавляют влияние инсулина на мембранный транспорт глюкозы.
Физиологические эффекты гормона роста
Гормон роста препятствует развитию большого количества разрушительных процессов в организме человека и стимулирует восстановительные. Многие авторитетные учёные заявляют, что под действием гормона роста происходит омоложение организма на 10-20 лет:
Но если ваша цель – это большой прирост мышечной массы, то понадобится максимальная стимуляция, а это значит, что одного гормона – не хватит. Нужен комплекс препаратов, который помогут не только усилить эффект гормона проста, но и безопасность тела. Существует определённая схема препаратов: гормон роста – анаболические и андрогенные стероиды – инсулин – гормоны щитовидной железы. Запомните: любой прием гормона и подбор препаратов должен проходить под наблюдение профессионального тренера!
Дозировки
Гормон роста является сильнейшим действующим препаратом для активного роста мышечной массы и быстрого уменьшения жировых отложений. Но, чтобы достичь желаемых результатов от приёма данного препарат, обязателен ряд условий, придерживаться которых может не так много людей (достаточно жёсткий график питания, тренировок и инъекций). Итак, что представляет собой курс гормона роста? Конечно же, курс препарата и его дозировка зависят от тяжести физических нагрузок и вида спорта, к примеру, дозировки легкоатлетов достигают 8 ЕД в сутки, что является недостаточным для эффективного набора мышечной массы тяжелоатлета.
Гормон роста – сильнейший действующий препарат для роста массы и сжигания жира. Для наилучшего эффекта нужно придерживаться курсу, распорядка дня, питания и тренировок. Дозировка зависит от тяжести нагрузок и вида спорта. Например, легкоатлеты достигают 8 единиц за сутки, чего мало для набора массы, а для физических показателей как выносливость – вполне достаточно.
Для качков-культуристов минимальная дозировка должна составлять 12-16 единиц, а курс должен быть не менее 3х месяц. Им нужна большая дозировка, потому что рецепторы довольно быстро привыкают к препарату, поэтому колоть его долгое время не следует. После проведённого курса терапии необходим перерыв, равный длине курса.
Конечно же гормон роста не запрещается принимать на протяжении 6 месяцев и более, но исключительно в маленьких дозировках 2-4 единицы в сутки. Однако, добиться при таком режиме гипертрофии и гиперплазии мышечных клеток почти невозможно.
Гормон роста, относясь к анаболическим средствам, способствует более интенсивному протеканию обменных процессов и производству свободных радикалов в организме,
Есть мнение, что прием препарата приводит к сокращению жизни и возникновению массы заболеваний: инфаркт, инсульт, рак и т.д. Что никак не доказано. Многие голливудские звезды такие как Дженифер Энистон (50 лет), Сандре Буллок (55 лет), Деми Мур (56 лет), колют его для омоложения – эффект на лицо.
Чтобы было понятнее мужиком, вот Сильвестер Сталлоне и Жан-Клод Ван Дамм
А вот побочные эффекты вполне реальны: тошнота, головная боль, гипергликемия, повышение внутричерепного давления, развитие сахарного диабета, чрезмерный рост хрящевых костей, что приводит к укрупнению черт лица и увеличению нижней и верхней челюсти. Чтобы избежать местных реакций, следует менять места подкожных инъекций, так как со временем может развиться липоатрофия – сгорание жировой ткани. При открытых зонах роста (до 25 лет) не исключён факт линейного роста тела.
Гормон роста у взрослых: функции соматотропина, нормы и нарушения
» data-image-caption=»» data-medium-file=»https://unclinic.ru/wp-content/uploads/2019/05/gormon-rosta-somatotropin-u-vzroslyh-900×600.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2019/05/gormon-rosta-somatotropin-u-vzroslyh.jpg» title=»Гормон роста у взрослых: функции соматотропина, нормы и нарушения»>
Юлия Гаврилова, гинеколог-эндокринолог. Редактор А. Герасимова
Это вещество вырабатывается передней долей гипофиза – придатка мозга, расположенного в углублении черепа – турецком седле. Гипофиз можно назвать «царем гормонов», поскольку он руководит их выработкой и сам синтезирует несколько гормональных веществ, в том числе гормон роста (соматотропный, или соматотропин). Это вещество обеспечивает рост и развитие опорно-двигательного аппарата, а также регулирует углеводный, белковый и жировой обмен.
Наибольшая концентрация соматотропина наблюдается в детском возрасте, когда организм растет, но он нужен и взрослым. Гормон улучшает состояние костей, мышц, хрящей, сосудов, участвует в обменных процессах и даже замедляет старение.
Какие функции выполняет гормон роста во взрослом организме и как его «приручить»
Однако если плотно покушать перед сном, особенно сладкого, или лечь спать на полный желудок, соматотропин не выделится, поскольку организму и так будет достаточно питательных веществ.
Поэтому, чтобы гормон выделился и расщепил жиры, нужно:
Однако, чтобы похудеть с помощью гормона, не стоит перед походом в тренажерный зал или занятиями физическими упражнениями есть шоколад, пить сладкий чай и кофе. В этом случае организму хватит углеводов и он затормозит выработку гормона роста.
Еще одна важная функция соматотропина – регулировка жирового обмена. Это вещество снижает образование «плохого» холестерина, откладывающегося на стенках сосудов и приводящего к формированию холестериновых бляшек. Поэтому достаточный уровень гормона роста – отличная профилактика атеросклероза, инфарктов, инсультов, сосудистых нарушений.
Соматотропин также участвует в синтезе ДНК, делении клеток и усиливает выработку молока в период кормления. Он помогает расщеплять глюкозу, превращая ее в гликоген – вещество, используемое для энергетической подпитки органов и тканей.
Что такое инсулиноподобный фактор роста и для чего он нужен
Хотя этот белок назван инсулиноподобным фактором (ИФР-1), прямого отношения к поджелудочной железе и диабету он не имеет. Просто эти два вещества схожи строением и способностью воздействовать на углеводы.
Это белковое вещество играет роль посредника между соматотропным гормоном и тканями, на которые он воздействует. Инсулиноподобный фактор образуется в печени в ответ на действие соматотропина и распространяется по всему организму. Затем он связывается с тканями клеток и передаёт команды, подаваемые соматотропным гормоном.
Инсулиноподобный фактор влияет на выработку соматотропного гормона – снижение его концентрации заставляет мозг вырабатывать соматотропин, а повышение – блокирует этот процесс. Такой механизм регуляции позволяет поддерживать оптимальный гормональный уровень.
Но в некоторых случаях этот процесс сбивается. Например, при сахарном диабете 2 типа ткани утрачивают способность связываться с ИФР-1 и поэтому невосприимчивы к соматотропину.
Не работает это вещество и при диабете 1 типа, а также при других заболеваниях, сопровождающихся высоким уровнем глюкозы в крови. При этих болезнях в крови содержится много глюкозы, поэтому организм не считает нужным брать углеводы ещё откуда-то. В результате гормон просто не выделяется, и его положительные качества не проявляются. Не работает инсулиноподобный фактор и при некоторых генетических нарушениях.
Анализ концентрации инсулиноподобного фактора роста проводится вместе с определением уровня соматотропного гормона. Это позволяет более объективно оценить результаты лабораторной диагностики.
Анализы на гормон роста и инсулиноподобный фактор
Для этих обследований берётся кровь из вены натощак через 8 часов после последнего приема пищи. За полчаса до взятия материала нельзя курить и подвергать организм эмоциональным нагрузкам.
Концентрация соматотропного гормона у взрослых
| Категория | Уровень гормона, мкг/л |
| Женщины | До 8 мкг/л |
| Мужчины | До 3 мкг/л |
Такой разброс обусловлен периодичностью выработки гормона, который может отсутствовать в организме во время взятия крови.
Увеличенная концентрация соматотропного гормона чаще всего указывает на наличие опухолей гипофиза, вызывающих выработку огромного количества соматотропина.
При резком увеличении концентрации соматотропина возникает тяжелое заболевание – акромегалия. При этой болезни усиливается тканевой рост. Но поскольку во взрослом возрасте костные структуры уже не растут, у больного начинают разрастаться хрящи и мягкие ткани. В результате увеличивается размер ладоней, ступней, ушей, носа, языка.
Изменяется тембр голоса, становится тяжело разговаривать. От этих последствий не удастся избавиться, даже нормализовав гормональный уровень. Поэтому при возникших изменениях черт лица, увеличении размера рук и ног нужно сразу обращаться к врачу и сдавать анализы.
Уровень инсулиноподобного фактора роста изменяется с возрастом. Его концентрация у взрослых составляет:
| Возраст, лет | Концентрация, нг/мл |
| 16-19, девушки | 176-249 |
| 16-19, юноши | 57-425 |
| 19-22 | 105-345 |
| 23-25 | 107-367 |
| 26-30 | 88-537 |
| 31-35 | 41-246 |
| 36-40 | 57-241 |
| 41-45 | 43-210 |
| 46-50 | 75-196 |
| 51-55 | 55-250 |
| 56-60 | 35-200 |
| 61-65 | 50-187 |
| 66-70 | 37-220 |
| 71-80 | 25-200 |
| Старше 80 | 17-325 |
ИФР-1 также реагирует не только на соматотропин, но и уровень гормонов, выделяемых половыми железами, щитовидкой и надпочечниками. Самая высокая его концентрация наблюдается у подростков, а с годами она снижается. Это тоже связано с ростом и развитием организма. Поэтому ИФР-1 часто называют маркером старения. Чем старше организм, тем ниже концентрация этого гормона.
Однако значительное превышение уровня ИФР-1 в немолодом возрасте не сулит ничего хорошего. Такие больные в 2-3 раза чаще заболевают возрастным слабоумием – болезнью Альцгеймера, а также различными раковыми опухолями.
Можно ли повысить уровень соматотропного гормона с помощью пищевых добавок
Такие вещества часто используют спортсмены и бодибилдеры, которые хотят нарастить мышцы и укрепить кости. Однако чужой соматотропный гормон никогда не заменит свой, поэтому будет оказывать эффект только во время приёма.
Точно дозировать соматотропин, не сдавая анализов и не посещая эндокринолога, невозможно. Поэтому у больных развивается гормональный дисбаланс. Возникает задержка жидкости, приводящая к отекам, боли в суставах и мышцах. В тяжелых случаях происходит отек глазных тканей, вызывающий ухудшение зрения. Могут возникать подъемы внутричерепного давления, сопровождающиеся тошнотой, рвотой, скачками АД, шумом в ушах.
Поскольку этот гормон тесно связан с инсулином и сахаром, его передозировка может привести к гипогликемии – резкому падению уровня сахара в крови и гипогликемической коме. Иногда может развиться акромегалия, как и при избытке собственного гормона.
Поэтому этот вид гормонов назначают только при необходимости после консультации врача и подробной диагностики организма. Иначе может возникнуть передозировка, приводящая к тяжелому эндокринному сбою.
Лучший вариант – повысить концентрацию собственного соматотропина, нормализовав режим сна и отдыха, уменьшив количество мучного и сладкого и регулярно занимаясь спортом.
Вопросы эффективности и безопасности применения препаратов гормона роста в педиатрической практике
В настоящее время препараты гормона роста широко применяются в практике детского эндокринолога. Доказана эффективность гормона роста в лечении низкорослости при использовании препаратов с заместительной целью. Однако прогнозирование эффективности терапии
Currently, growth hormone preparations are widely used in practice of child’s endocrinologist. The efficiency of growth hormone in using its preparations with the purpose of substitution for treatment of stunting was proven. However, forecasting of the therapeutic efficiency remains the issue which requires detailed study.
Применение препаратов гормона роста (ГР) в терапевтических алгоритмах заболеваний, сопровождающихся нарушениями динамики ростовых показателей, сегодня обусловлено широкой доступностью несмотря на высокую стоимость. Рекомбинантный человеческий ГР, полученный биосинтетическим путем, используют в педиатрической практике как средство стимуляции роста, так и как метаболический регулятор нарушенных обменных процессов начиная с 1985 г. Вместе с тем препараты соматропина (МНН препаратов гормона роста) имеют определенные показания с доказанной эффективностью. Основным показанием к назначению соматропина является гипопитуитаризм. Именно лечение недостаточности ГР при гипопитуитаризме препаратами соматропина является патогенетически обоснованным и проводится с заместительной целью.
Применение ГР при других вариантах низкорослости возможно, но прогностически непредсказуемо. К настоящему времени имеются данные об эффективности лечения ГР детей с внутриутробной задержкой роста, семейной низкорослостью, синдромами Шерешевского–Тернера, Прадера–Вилли, Рассела–Сильвера, анемией Фанкони, гликогенозом, хронической почечной недостаточностью, скелетными дисплазиями, муковисцидозом [1].
С 2003 г. в США используют биосинтетический ГР для лечения детей с идиопатической низкорослостью. Возраст в начале терапии ГР и ответ на терапию ГР в первый год лечения являются основными факторами, определяющими конечный рост при идиопатической низкорослости. Предполагалось, что дети с хорошим ростовым ответом в первый год лечения ГР при идиопатической низкорослости скорее всего будут иметь хороший конечный рост при использовании даже низких доз ГР [2]. Однако результаты наблюдения показали, что индивидуальный эффект терапии остается сложным для предсказания. Большая вариабельность ауксиологических данных, возраст, показатели роста и костного возраста на момент начала терапии, скорость роста в первый год лечения определяют многофакторный анализ, сложный для прогнозирования.
Достаточно сложно прогнозировать ответ на лечение ГР также и при заместительной терапии. Оценка эффективности лечения ГР при соматотропной недостаточности по ауксиологическим параметрам показала, что ростовой ответ является переменным и различен в каждом конкретном случае [3]. Характерной особенностью терапии соматотропной недостаточности является то, что по данным наблюдений за терапией пациентов результат первого года лечения выше, чем в последующие годы. При этом отмечено, что единственным клинически значимым предиктором ответа роста на начало лечения в первый год является возраст начала терапии. Тогда как ни пик ГР при проведении стимуляционных тестов, ни пол, ни рост на момент начала терапии, индекс массы тела (ИМТ), костный возраст, доза ГР не влияют на скорость роста в первый год терапии. Более ранняя диагностика и лечение ГР позволяют достичь лучшего конечного роста в тяжелых случаях недостаточности ГР. Показано, что лучший ответ на лечение отмечался у детей с тяжелой степенью недостаточности ГР [4]. Но, по другим данным, конечный рост не имеет существенных различий у пациентов с тяжелым дефицитом ГР и пациентов с парциальным дефицитом ГР [5].
Рядом исследований было показано, что рост родителей является одним из показателей, который позволяет прогнозировать конечный рост у пациентов с дефицитом ГР, получающих заместительную терапию ГР. Было отмечено, что лечение ГР имеет лучшую эффективность у пациентов, в семьях которых не было родственников с низкорослостью [6].
Хотя лечение препаратами ГР не всегда сопровождается достижением генетически детерминированного роста, увеличение роста в первый год лечения в возрасте до начала полового развития коррелирует с общей прибавкой в росте при терапии. Это подтверждает важность начала лечения до начала пубертата [7].
В настоящее время ведется ряд исследований, с помощью которых подбирается необходимое сочетание лекарственных препаратов, комбинация с которыми ГР улучшит результаты лечения. Так, было показано, что одновременное назначение при врожденном дефиците ГР заместительной терапии ГР и агониста гонадолиберина с целью торможения инициации полового развития не имеет преимуществ перед назначением только ГР [8].
Ростовые эффекты ГР при соматотропной недостаточности у пациентов и с изолированным дефицитом ГР, и у пациентов с множественной недостаточностью гормонов гипофиза выражены с одинаковой степенью: 89% пациентов с изолированной недостаточностью ГР и 81% пациентов при множественном дефиците гормонов гипофиза достигают прогнозируемого роста. Причем бо?льшая прибавка в росте наблюдается в возрасте до начала пубертата [9].
Многолетний опыт лечения препаратами ГР показал, что лечение детей с низкорослостью с использованием дозы соматропина, рассчитанной на массу тела ребенка, сопровождается большой вариабельностью в ростовом ответе на терапию ГР. Вопрос, почему дети с недостаточностью ГР, терапия которых направлена на простое замещение недостающего ГР, имеют такие различные клинические исходы, до настоящего времени не решен.
Ведутся исследования, направленные на поиск фармакогеномных маркеров с прогностической значимостью чувствительности клеток к ГР.
Изучено изменение уровня инсулиноподобного фактора роста 1 (ИФР-1) после 1 месяца лечения ГР у детей с недостаточностью ГР и доказано, что имеется зависимость между полиморфизмом клеточного регулятора CDK4 и степенью изменения концентрации ИФР-1. Дальнейшее изучение взаимосвязи геномных маркеров и ранних изменений уровня ИФР-1 может позволить разработать стратегию быстрого индивидуального подбора дозы ГР при врожденной соматотропной недостаточности [10].
Также на конечный рост пациентов, получающих лечение ГР, оказывает влияние наличие или отсутствие полиморфизма SOCS2 (rs3782415). Полиморфизм, выявляемый в GHR, IGFBP3 и SOCS2 локусах, влияет на результаты роста пациентов с врожденной соматотропной недостаточностью, получающих ГР. Использование этих генетических маркеров может определить пациентов, генетически предрасположенных к менее результативному лечению [11].
Конечным результатом подобных исследований должно стать признание важности индивидуального дозирования ГР для каждого пациента на основе конкретных индивидуальных геномных характеристик. Это позволит значительно улучшить терапию, которая в течение долгих лет базируется на принципе «одна дозировка подходит всем».
Насколько терапевтическая эффективность соматропина сопоставима с его безопасностью — вопрос, требующий глубокого детального анализа, решение которого возможно путем накопления опыта применения ГР при лечении различных форм низкорослости.
Безопасность во время лечения и неблагоприятные эффекты лечения ГР тщательно отслеживаются и описываются у детей с дефицитом ГР (как с изолированной, так и с множественной недостаточностью гормонов аденогипофиза) и у детей с идиопатической низкорослостью [12]. Согласно имеющейся информации, полученной в основном из постмаркетинговых исследований, поддерживаемых производителями препаратов ГР, имеется низкая частота (менее 3% пролеченных детей) побочных эффектов и увеличение благоприятного профиля безопасности ГР. Тем не менее, полный спектр потенциальных побочных эффектов ГР не точно диагностируется при помощи постмаркетинговых исследований. Это связано с достаточно длительным сроком лечения, меняющимися в динамике характеристиками больного и невозможностью отследить нежелательные явления после окончания лечения пациента [13–15].
Редко возникающим нежелательным явлением при лечении ГР является внутричерепная гипертензия. Более высокий риск ее развития отмечен в группах больных с хронической почечной недостаточностью, синдромом Шерешевского–Тернера и с органическими причинами дефицита ГР. Внутричерепная гипертензия обычно развивается в начальном периоде лечения или при увеличении дозы препаратов соматропина, прекращается с окончанием терапии ГР. Показанием для проведения фундоскопии офтальмологом являются симптомы, указывающие на внутричерепную гипертензию, такие как сильная головная боль, двоение/нечеткое зрение и рвота. Лечение часто может быть возобновлено при более низких дозах ГР без возврата симптомов.
К осложнениям терапии соматропином относят изменения в костной системе — эпифизеолиз и сколиоз. Эпифизеолиз диагностируется с частотой 73 на 100 000 лет лечения и встречается реже у больных с изолированным дефицитом ГР и идиопатической низкорослостью по сравнению с теми пациентами, у которых дефицит ГР наблюдается вследствие внутричерепных новообразований, краниофарингеомы [16]. Средняя продолжительность от начала терапии ГР до появления эпифизеолиза колеблется от 0,4 до 2,5 лет. Рекомендовано регулярное наблюдение за появлением соответствующих симптомов, таких как боли в бедре и/или боли в колене, изменения в походке, в случае положительного результата — тщательное обследование и консультация ортопеда. Эпифизеолиз требует хирургического вмешательства на эпифизе бедренной кости.
Сколиоз прогрессирует во время лечения ГР из-за быстрого роста, а не является прямым побочным эффектом ГР. Наиболее часто сколиоз развивается при лечении синдромальных форм низкорослости (например, при синдроме Шерешевского–Тернера и синдроме Прадера–Вилли) [17]. У 0,2% детей с идиопатической низкорослостью или с изолированным дефицитом ГР, получавших ГР, отмечено прогрессирование сколиоза [18]. Регулярное обследование на предмет наличия или прогрессирования сколиоза рекомендуется всем пациентам, получающим препараты ГР.
Данные научных публикаций и собственный практический клинический опыт свидетельствуют о необходимости мониторинга показателей метаболизма глюкозы у пациентов, получающих ГР. Это связано с доказанным фактом наличия резистентности к инсулину при лечении препаратами соматропина. Заболеваемость сахарным диабетом (СД) 1-го типа не увеличивается при терапии ГР. Вместе с тем известно, что больные с синдромом Шерешевского–Тернера, Прадера–Вилли имеют высокий риск развития неиммунных форм сахарного диабета. Снижение чувствительности к инсулину и компенсаторное увеличение секреции инсулина с обеспечением эугликемии сопровождается нарушением толерантности к глюкозе и требует коррекции метаболических нарушений, а в ряде случаев отмены препаратов ГР [19]. Мониторинг потенциального развития сахарного диабета с тестированием крови на уровень глюкозы и/или HbA1c должен быть включен в алгоритм наблюдения за всеми пациентами, получающими препараты ГР.
Патофизиологические и эпидемиологические наблюдения позволяют выразить опасение, что ГР может увеличить риск развития злокачественной опухоли во время или после терапии. Известно, что реализация ростового эффекта ГР опосредована соматомединами, один из которых ИФР-1. ИФР-1 и ГР относятся к веществам с митогенной и антиапоптозной активностью, и их рецепторы обнаружены в опухолях. Состояния нарушенной и избыточной секреции/действия ГР ассоциированы со снижением и повышением риска злокачественности соответственно. Снижение ИФР-1 через ограничение калорийности индуцирует апоптоз и предотвращает или замедляет рост опухоли [20–22]. Некоторые немногочисленные эпидемиологические исследования соотносят увеличение ГР и уровни ИФР-1 с опухолями толстой кишки, молочной железы, щитовидной железы и раком предстательной железы у взрослых [23]. В целом данные литературы указывают на разрешающую/факультативную, а не причинную роль ГР в онкогенезе.
Заболеваемость впервые выявленными во время лечения лейкемией или злокачественными новообразованиями в целом после лечения у детей без сопутствующих факторов риска не увеличивается по сравнению с таковой в общей популяции. Несмотря на данные об отсутствии влияния ГР на появление второго новообразования у детей, в анамнезе которых была неоплазия [24, 25], пункт о повышенном риске развития второго новообразования у пациентов, получавших ГР, в настоящее время присутствует в инструкции по применению на всех препаратах ГР в США. Отсутствуют данные относительно эффектов ГР на риск развития неоплазии у больных с заболеваниями, которые сами отнесены в группу повышенного риска возникновения новообразований. Риск новообразований у пациентов, получающих лечение ГР, был рассмотрен Комитетом по лекарственным средствам и терапии Общества детских эндокринологов, и ключевой рекомендацией является необходимость продолжающегося наблюдения всех пациентов, получавших лечение ГР, и это имеет первостепенное значение [26].
Перед началом терапии ребенка препаратами гормона роста его родители должны быть информированы о неопределенности в отношении долгосрочной безопасности (о неблагоприятных эффектах после терапии в зрелом возрасте).
Долгосрочные исследования (в среднем 17 лет) по наблюдению 6928 детей с изолированной соматотропной недостаточностью идиопатической низкорослостью, или низким гестационным возрастом, которые начали лечение ГР в период между 1985 и 1996 гг., во Франции показали 30%-й рост общей смертности по сравнению с населением в целом [27]. Все виды смертности, связанной с раком, не были увеличены, но стандартизованные показатели смертности были повышены в группах больных с опухолями костной системы, больных с нарушениями в системе кровообращения и больных с кровоизлиянием в мозг. Применение дозы препаратов ГР более 50 мкг/кг/день не рекомендовано. Полученные из той же базы данные в недавнем исследовании показали значительно более высокий риск развития инсульта (особенно геморрагического инсульта) среди пациентов, получавших ГР в детстве [28]. В противоположность этому последующее наблюдение 2543 пациентов с изолированной соматотропной недостаточностью, идиопатической низкорослостью или низким гестационным возрастом из других европейских стран не выявили никакого эффекта воздействия ГР и/или дозы на смертность или частоту развития сердечно-сосудистых событий [29].
Таким образом, имеющиеся данные относительно безопасности терапии ГР для детей с различными формами низкорослости определяют необходимость формирования персонализированного алгоритма диспансерного наблюдения пациента и должны включать информирование родителей ребенка об имеющихся сегодня сведениях о нежелательных явлениях как во время лечения, так и в отдаленные периоды жизни.
Применение высоких доз препаратов гормона роста при синдромальных формах низкорослости должно иметь взвешенный подход к сопоставлению показателей эффективности и безопасности лечения. Увеличение дозы ГР определяет рост шансов, отдаленных метаболических или злокачественных рисков, не обнаруженных в ходе проведенных на сегодняшний день исследований. Изменение характеристик пациентов, этнических особенностей и рост уровня ожирения в детстве может увеличить риск развития СД 2-го типа у получающих ГР.
Определенные побочные эффекты препаратов ГР, связанные с ускоренным ростом (прогрессирование сколиоза и эпифизеолиз) и другими неизвестными механизмами (внутричерепная гипертензия), встречаются редко, однако требуют упреждающего разъяснения и тщательного контроля.
Кроме того, следует помнить об отдаленных последствиях гормонального лечения. Поскольку исследования населения, не получающего ГР, свидетельствуют о том, что высокие нормальные уровни свободного ИФР-1 (часто выявляемые у детей, получавших ГР) могут увеличить риски онкологических заболеваний, потенциальные связи между воздействием ГР и будущими рисками возникновения неоплазии требуют постоянного контроля. И, наконец, соответствующий уровень допустимого риска для новейшей и потенциально самой большой группы пациентов, получавших ГР, — практически здоровых, но низкорослых детей — еще предстоит определить [30].
Литературы
Е. Б. Башнина, доктор медицинских наук, профессор
О. С. Берсенева 1
ФГБОУ ВО СЗГМУ им. И. И. Мечникова МЗ РФ, Санкт-Петербург