кортикостероиды используются в эндодонтической практике для снижения
Глюкокортикоидная терапия сегодня: эффективность и безопасность
В каких случаях проводится терапия глюкокортикоидами? Какие виды гормональной терапии используются? История применения глюкокортикостероидов (ГКС) в клинической практике насчитывает чуть более полувека, хотя «антиревматическая субстанция Х» была изве
В каких случаях проводится терапия глюкокортикоидами?
Какие виды гормональной терапии используются?
История применения глюкокортикостероидов (ГКС) в клинической практике насчитывает чуть более полувека, хотя «антиревматическая субстанция Х» была известна еще с 20-х годов ХХ столетия. Детальное изучение клинической значимости гормонов коры надпочечников, начатое Edward Calvin Kendall и Tadeus Reichstein, было продолжено только после того, как Philip Hench в конце 40-х годов обратил внимание на улучшение течения ревматоидного артрита при желтухе и беременности. В 1950 году всем троим была присуждена Нобелевская премия за «. открытия в отношении гормонов коры надпочечников, их структуры и биологических эффектов».
В настоящее время к ГКС относятся как естественные гормоны коры надпочечников с преимущественно глюкокортикоидной функцией — кортизон и гидрокортизон (кортизол), так и их синтезированные аналоги — преднизон, преднизолон, метилпреднизолон и др., включая галогенированные (фторированные) производные — триамцинолон, дексаметазон, бетаметазон и др. Широкий спектр физиологических и фармакологических эффектов глюкокортикоидов (адаптогенный, противовоспалительный, обезболивающий и жаропонижающий, неспецифический мембраностабилизирующий и противоотечный, противоаллергический и иммуносупрессивный, гематологический, гемодинамический и противошоковый, антитоксический, противорвотный и др.) делает эти препараты чуть ли не универсальными лекарственными средствами, и сегодня трудно найти такое патологическое состояние, при котором на том или ином этапе развития они не были бы показаны. Среди показаний в первую очередь можно выделить так называемые ревматические заболевания, болезни почек, крови, аллергические заболевания, трансплантации, ургентные состояния.
В зависимости от цели различаются три варианта терапии ГКС; при этом любая из них может быть как ургентной, так и плановой.
В отличие от плановой терапии применение ГКС в ургентных ситуациях носит, как правило, симптоматический, реже патогенетический характер и не заменяет, а дополняет другие методы лечения. В рамках неотложной терапии ГКС применяются при острой надпочечниковой недостаточности, тиреотоксическом кризе, аллергических заболеваниях (сывороточная болезнь, анафилактический шок, бронхиальная астма, крапивница, отек Квинке), заболеваниях печени (печеночно-клеточная недостаточность), неврологических заболеваниях (туберкулезный и бактериальный менингит, некоторые формы отека мозга), различных видах шока (кроме кардиогенного).
Из-за обилия побочных эффектов терапия ГКС направлена в основном на достижение максимального эффекта при назначении минимальных доз, величина которых определяется заболеванием и не зависит от массы тела и возраста; доза корректируется в соответствии с индивидуальной реакцией. Приняты две принципиально разные схемы назначения ГКС:
В зависимости от суточной дозы (в пересчете на преднизолон) и длительности применения ГКС принято выделять несколько видов терапии, имеющих различные показания:
Результат терапии ГКС зависит не только от дозы, но и от режима дозирования. Наиболее перспективными можно считать прерывистые схемы применения, когда за счет увеличения суточной дозы препарат принимается не каждый день. Самой эффективной представляется внутривенная пульс-терапия максимальными дозами, однако она оказывается и самой небезопасной. Значительно более безопасным должен быть признан режим «мини-пульс», который, однако, уступает по эффективности пульс-терапии. Столь же эффективно назначение умеренной/высокой дозы, разделенной на несколько приемов; но по безопасности этот режим уступает «мини-пульсу». Далее по эффективности следуют альтернирующий режим (через день удвоенные суточные дозы с последующим постепенным уменьшением) и режим ежедневного однократного назначения умеренной/высокой дозы; первый из них безопаснее и по этому критерию приближается к «мини-пульсу». Наиболее безопасна терапия низкими дозами, которая, однако, обеспечивает лишь поддерживающий эффект. При всех ежедневных схемах ГКС следует назначать в ранние утренние часы (между 6 и 8 часами); если же одноразовый прием невозможен из-за величины дозы, 2/3 дозы назначаются в 8 часов и 1/3 — днем (около полудня). При любом режиме дозирования по достижении планируемого эффекта доза постепенно снижается до поддерживающей или препарат отменяется вовсе.
Важной проблемой терапии ГКС является выбор препарата. Фармакокинетические и фармакодинамические свойства ГКС, включая их побочные эффекты, существенно различаются у отдельных препаратов (табл. 1, табл. 2). Приняв за единицу выраженность различных эффектов гидрокортизона, можно получить количественные характеристики активности отдельных препаратов. При сравнении ГКС чаще всего анализируется противовоспалительное действие этих препаратов, в соответствии с которым и рассчитывается эквивалентная пероральная доза, снижающаяся по мере увеличения противовоспалительной активности. Ее возрастание, параллельное увеличению длительности действия отдельных ГКС, сопровождается уменьшением минералокортикоидной активности, которой у метилпреднизолона (солу-медрола) и фторированных соединений вообще можно пренебречь.
Соотношение терапевтического и побочных эффектов позволяет утверждать, что в настоящее время препаратом выбора для длительной и пожизненной терапии является метилпреднизолон (солу-медрол). В настоящий момент солу-медрол широко используется в лечении аутоиммунных заболеваний, в трансплантологии и интенсивной терапии. Многообразие форм выпуска позволяет использовать препарат во всех возрастных категориях в оптимальных дозировках.
Вторым по эффективности препаратом остается в большинстве случаев преднизолон. Во многих же ургентных ситуациях определенными достоинствами обладают фторированные соединения: дексаметазон (дексазон, дексона) и бетаметазон (целестон, дипроспан). Однако в случае неотложной терапии, при которой противовоспалительное действие не играет ведущей роли, сравнительная оценка эффективности и безопасности различных препаратов весьма затруднительна по крайней мере по двум причинам:
В связи с вышеуказанными трудностями была предложена условная эквивалентная единица (УЭЕ), за которую принимаются минимальные эффективные дозы. Показано, что выраженные в УЭЕ максимальные суточные эффективные дозы фторированных ГКС (дексаметазона и бетаметазона) в пять раз меньше, чем у негалогенированных препаратов. Это обеспечивает не только более высокую эффективность и безопасность данной группы препаратов, назначаемых в определенных ситуациях, но и их фармакоэкономические преимущества.
Как бы тщательно ни проводился выбор препарата, режима дозирования и вида терапии, полностью предотвратить развитие тех или иных побочных эффектов при применении ГКС не удается. Характер побочных реакций может зависеть от ряда причин (табл. 3).
Вероятность и выраженность подавления оси ГГКН с развитием вначале функциональной недостаточности, а позже и атрофии коры надпочечников определяются дозой и длительностью терапии. Прекращение глюкокортикоидной терапии почти всегда сопряжено с угрозой развития острой надпочечниковой недостаточности.
Частым побочным действием ГКС оказываются инфекционные осложнения, которые в этом случае протекают атипично, что связано с противовоспалительной, аналгетической и жаропонижающей активностью этих средств. Это затрудняет своевременную диагностику и требует проведения ряда профилактических мероприятий. Из-за склонности к генерализации, затяжному течению, тканевому распаду и резистентности к специфической терапии эти осложнения становятся особенно грозными. Столь же коварны и «стероидные язвы», отличающиеся бессимптомным течением и склонностью к кровотечениям и перфорациям. Между тем желудочный дискомфорт, тошнота, другие диспепсические жалобы на фоне приема ГКС чаще не связаны с поражением слизистой. Экзогенный синдром Кушинга как осложнение терапии ГКС встречается далеко не всегда, однако отдельные нарушения метаболизма, гормональной регуляции и деятельности тех или иных систем развиваются почти во всех случаях глюкокортикоидной терапии.
С сожалением приходится отметить, что утверждение Е. М. Тареева, назвавшего терапию ГКС трудной, сложной и опасной, до сих пор справедливо. Как писал Тареев, такую терапию гораздо легче начать, чем прекратить. Однако ответственный подход к лечению позволяет значительно повысить его безопасность. Это достигается благодаря строгому учету противопоказаний (абсолютных среди которых нет) и побочных эффектов ГКС (оценка отношения «ожидаемый эффект/предполагаемый риск»), а также проведению «терапии прикрытия» в группах риска (антибактериальные препараты при хронических очагах инфекции, коррекция доз сахароснижающих средств или переход на инсулин при сахарном диабете и др.). Особое место при длительном применении ГКС занимает метаболическая терапия, которая проводится в целях предупреждения и коррекции нарушений электролитного обмена и катаболических процессов в первую очередь в миокарде (дистрофия) и костной ткани (остеопороз). Однако наиболее надежным путем обеспечения безопасности терапии ГКС остается соблюдение основного принципа клинической фармакологии и фармакотерапии — назначение лечения по строгим показаниям.
В. В. Городецкий, кандидат медицинских наук
А. В. Тополянский, кандидат медицинских наук
Кортикостероиды используются в эндодонтической практике для снижения
Автор: Маланьин Игорь Валентинович
доктор медицинских наук,
профессор, академик РАЕ,
заслуженный деятель науки и образования
Статья опубликована: журнал Дентал Юг № 1(30). Краснодар, 2005. с. 10-12.
Взгляд на некоторые популярные материалы для обтурации корневых каналов.
Эндодонтия сегодня продолжает стремиться к высоким технологиям и новым материалам.
По мере того, как все большее число исследователей предлагали свои решения для часто встречающихся клинических ситуаций, сложность арсенала материалов для обтурации корневых каналов возрастала. Высокий уровень мануальных навыков, необходимых в эндодонтии, неизбежно определяет совершенствование персонального мастерства. Отсюда совершенно очевидно появление многочисленных публикаций, относящихся к конкретному материалу или методу.
Большинство из применяемых в настоящее время материалов для обтурации корневых каналов успешно использовались в течение нескольких десятилетий. Основное внимание обычно уделялось клиническим данным и исследованиям, направленным на улучшение или модификацию устоявшихся клинических методов. Это часто приводило к усовершенствованию известных методик, а не к разработке новых материалов.
Кроме личностных, субъективных влияний, в литературе по материалам для обтурации корневых каналов отражаются преобладающие в эндодонтической практике концепции, популярные на данный период времени. Это происходит несмотря на почти всеобщее убеждение, что основу клинической эндодонтической практики составляют очистка, формирование и пломбирование системы корневого канала. Например, когда специалисты были абсолютно уверены, что депульпированные зубы являются «очагами инфекции», основной упор они делали на инструментальные методики, направленные на «дезинфекцию» корневого канала и на пломбировочные материалы с сильным и длительным антисептическим действием. Позже эндодонтические методы постепенно были переориентированы на уменьшение травматического повреждения инструментами периодонтальной связки и на использование материалов, которые лучше переносятся пульпой и периапикальными тканями. До недавнего времени материалы для обтурации корневых каналов не исследовались как таковые вне связи с клиническими методиками.
Современный, вновь созданный материал для обтурации корневых каналов имеет непродолжительную жизнь. Многие из технологий и методов лечения, которые студенты изучают сегодня, будут модифицированы или вообще заменены другими к тому времени, когда эти студенты станут врачами. Для того, чтобы идти в ногу со временем, врач-стоматолог должен обладать способностью оценивать потенциальные возможности каждого нового материала и метода лечения.
Общеизвестно, что последней стадией эндодонтического лечения является полное, плотное и герметичное заполнение системы корневого канала и всех труднодоступных отделов нераздражающими материалами. Для успешного лечения необходимо трехмерное пломбирование всего пространства канала, апикального отверстия в области дентинно–цементного соединения и дополнительных каналов инертным, биологически совместимым материалом, имеющим пространственную стабильность. Ампутационные методы лечения пульпита, применяемые до недавнего времени в отечественной стоматологии считаются в современной стоматологической практике грубейшей ошибкой.
Материалы для корневых каналов контактируют с биологической тканью, не защищенной слоем эпителия, поэтому их биосовместимость представляет особую важность. Общепринято, что биологически приемлемый материал должен быть инертным. На практике не всегда этого можно достичь. Поэтому создатели материалов стремятся добиться благоприятного взаимовлияния между материалом и биологической средой, в которой он находится, и которая не оказывала бы отрицательного влияния на сам материал. Важно, чтобы материал не вызывал воспалительной реакции ткани, так как это может вызвать ее раздражение, боль и некротические изменения.
Постоянной проблемой эндодонтического лечения является возможность рецидива инфекции у верхушки корня зуба из-за присутствия там микроорганизмов. Это диктует еще одно требование к материалам для заполнения корневых каналов — обладать противомикробным действием.
В современной стоматологии довольно трудно объединить эти два требования к материалу, поскольку это предполагает необходимость учитывать высокую степень избирательности биологической реакции. Ведь хорошо известно, что материал, обладающий противомикробным действием, вызывает воспалительную реакцию в прилежащих тканях, а те материалы, которые ее не вызывают, имеют наилучшие бактериостатические свойства. Если согласиться, что полной герметизации корневого канала достичь невозможно, используемые материалы должны иметь достаточную антимикробную активность, чтобы предупредить инфильтрацию микробов в пространство канала и их пролиферацию. В тоже время, антимикробные свойства материала не должны достигаться за счет его биосовместимости.
Гуттаперча является биосовместимым материалом при очень низкой цитотоксичности, поэтому только используемые с ней цементы будут определять реакцию ткани.
Гуттаперчевые штифты используются в сочетании с цементом, который необходим для заполнения пространств между штифтом и стенкой корневого канала, предупреждая, таким образом, проникновение микроорганизмов. Он также смазывает штифты в процессе их уплотнения, заполняя неровности канала и боковые канальцы.
Использование цементов для герметизации корневого канала без обтурирующих штифтов не рекомендуется. При внесении цементов в канал большой массой, они подвергаются более интенсивному растворению и дают избыточную усадку при отверждении. В дополнение к этому, довольно трудно определить адекватное заполнение канала, к тому же существует опасность выхода цемента за верхушку корня в окружающие ткани.
До недавнего времени принято считалось, что заполнение канала цементом не может гарантировать от проницаемости тканей зуба, и поэтому основное внимание уделяется приданию этим материалам противомикробных свойств.
В клинической практике для заполнения корневых каналов используется большое количество материалов, включая:
Эндометазон — материал на основе цинк-оксидэвгеноловой пасты; содержит кортикостероиды (гидрокортизон и дексаметазон), антисептики, дийодотимол и параформальдегид, а также рентгеноконтрастный наполнитель.
Антисептики обеспечивают стерилизацию органических остатков в микроканалах, дельтовидных ответвлениях, воздействуют на микрофлору периапикального очага при периодонтитах. По мере отвердевания пасты действие этих веществ ослабевает, а затем прекращается. Если эндометазон выводится за верхушку, то эвгенол довольно быстро диффундирует в кровяное русло, а затем постепенно рассасываются и остальные компоненты пасты (сначала за апикальным отверстием, а затем в канале).
Что касается кортикостероидов, то они, помимо положительного действия, имеют и ряд отрицательных свойств. Например, ослабляют защитные механизмы периапикального участка, в частности, из-за подавления фагоцитоза, в результате чего происходит размножение микроорганизмов; не исключены также их побочные эффекты.
Входящее в состав эндометазона для снижения осложнений после пломбирования, относятся также средства, содержащие формальдегид. Предложенный в начале прошлого века и очень широко применявшийся в течение длительного времени резорцин формалиновый метод подвергся в 80-х — начале 90-х годов внимательному анализу на предмет его токсического действия, примеров которого накопилось достаточно много.
Электронно-микроскопическое исследование продемонстрировало, что формальдегид денатурирует белки пульпы и, осаждаясь в кристаллическом виде на поверхности денатурата, плотно связывается с ним. Если белкового материала в корневых каналах достаточно для того, чтобы связать формалин, его системные эффекты незначительны. Если же пульпа частично или полностью удалена, антисептик может попадать в периодонт, вызывая местные и общие неблагоприятные эффекты.
С применением параформальдегида и кортикостероидов связаны многие негативные явления. При контакте формальдегида с живыми тканями он распространяется по всему организму. При системных исследованиях нашли меченый параформальдегид в крови, регионарных лимфатических узлах, почках и печени после пульпэктомии у собак при использовании меченого 14-градусного формокрезола. Кроме того, общеизвестно, что формальдегид обладает мутагенными и канцерогенными свойствами. В этой связи возникает вопрос о возможности контакта с живыми тканями.
Популярность данного материала среди некоторых врачей объясняется тем, что ведение в состав эндометазона кортикостероидных препаратов и параформальдегида позволяет значительно снизить риск развития болезненных реакций со стороны периодонта после эндодонтического лечения, даже при случайном (постоянном) выведении материала за верхушку.
При не доведении материала до апекса или некачественной обработке канала эндометазон хорош для так называемой химической пульпотомии. В первом случае ведущим является антисептическое действие, во втором — предусматривается также возможность вызвать асептический некроз и мумификацию пульпы без полной механической экстракции. Другими словами, данный препарат является препаратом выбора у врачей, имеющих недостаточные мануальные навыки.
Не перечисляя перечень отрицательных свойств эндометазона и ему подобных препаратов, хочется добавить, что не только Международная ассоциация стоматологов и ассоциация дантистов Америки, но и многие Российские учебные центры не рекомендуют (запрещают) пломбирование корневых каналов пастами, так как последние не обеспечивают надёжной обтурации.
Так же нецелесообразно применять цементы, содержащие гидроксид кальция (Apexit, Ivoclar; Sealapex, Kerr ), для постоянного пломбирования. Это связано с тем, что гидроксид кальция выделяясь из материала уменьшает его пространственный обьём, что недопустимо при постоянном пломбировании. Также врачи забывают, что гидроксид кальция действует непродолжительное время и применяется для временного пломбирования.
АН-26, АН Plus.
По мнению автора, неплохой альтернативой вышеперечисленным материалам, является АН-26, широко применяемый, не только в Краснодарском крае, но и в мировой эндодонтической практике. Впервые о нем сообщили примерно в 1957 году. Он является эпоксидной смолой с плохой растворимостью. Состоит из порошка серебра (10%), триоксида висмута (60%), диоксида титана (5%) и гексаметилен тетрамина (25%), которые смешиваются до консистенции густой пасты с жидкостью — бисфенол диглицидиловым эфиром (100%). Имеет хорошие адгезивные свойства, антибактериальную активность, низкую токсичность и хорошо переносится периапикальными тканями.
АН 26 — тонкотекучий медленно отверждающийся материал. Если процесс его отверждения проходит в контакте с тканевой жидкостью, из него высвобождаются небольшие количества формальдегида. Время затвердевания составляет около 34 часов. При некоторых техниках пломбирования это считается преимуществом, так как обеспечивается время для коррекции пломбирования после рентгенологического контроля. В последствии была представлена модификация этого пломбировочного материала — АН Plus, представляющая собой двупастовую систему, исключающую содержание гексаметил-тетрамина, ответственного за высвобождение формальдегида.
АН-26 содержит порошок серебра, поэтому, чтобы избежать изменения цвета зуба, все остатки корневого цемента нужно удалять до уровня края десны. В связи с этим, выпускаемые современной промышленностью АН-26 и АН Plus серебра не содержат.
Умеренная цитотоксическая реакция на свежеприготовленный АН26 может быть связана с высвобождением формальдегида, который образуется как побочный продукт процесса полимеризации. Поскольку для полимеризации АН26 необходимо некоторое время, у пациентов может появляться некоторая степень чувствительности, которая может быть связана с его использованием. Как было показано, АН Plus высвобождает лишь небольшое количество формальдегида (3,9 мг/кг) по сравнению с АН26 (1347 мг/кг). Тем не менее, АН26 обладает цититоксичностью, хотя она значительно снижается после отверждения материала.
Endion.
В своей повседневной работе многие врачи отдают предпочтение использованию стеклоиономерных цементов для постоянного пломбирования корневых каналов в силу биосовместимости с тканями зуба и периодонта. Клинические исследования материала, Endion (Voko), проводимые автором, показали неплохие отдалённые результаты (в течение 7 лет), которые сопоставлялись с данными исследований других пломбировочных материалов. Исследования показали высокую биосовместимость, хорошее сцепление с дентином и незначительную усадку.
Недостатком стеклоиономерных цементов является трудность их извлечения из корневых каналов. Хотя, по мнению автора, он относительно легко удаляется из корневого канала при помощи ультразвука.
Также «нелюбовь» многих врачей к данному материалу объясняется тем, что из за непродолжительного времени затвердевания, затруднена качественная латеральная конденсация. При выходе его за верхушку возникает сильная болезненность. Однако, при совершенствовании мануальных навыков эти проблемы легко устранимы.
Автор, работая материалом Epiphani, довольно непродолжительное время, всё же сделал попытку отразить свои впечатления об этом материале:
В связи с тем, что можно полимеризовать светом обтурацию Epiphani сразу после заполнения канала, произойдет немедленное коронарное запечатывание. Это избавит пациента от повторного посещения.
Epiphani может использоваться с любой техникой обтурации и имеет высокую рентгеноконтрастность.
В случае необходимости извлечения из каналов Epiphani не возникает ни каких трудностей, он легко извлекается, не сложнее чем гуттаперча с цинк-оксидным герметиком.
На сегодняшний день Epiphani представляет собой альтернативу системам обтурации на базе гуттаперчи, в связи с тем, что ей присущи все достоинства гуттаперчи, но при этом она свободна от недостатков, гуттаперчи.
Несмотря на внедрение в практику большого числа материалов для заполнения корневых каналов, многие врачи-эндодонты, к сожалению, предпочитают использовать для этих целей материалы на основе цинк-оксид-эвгеноловой пасты.
На сегодняшний день успех эндодонтического лечения является реальностью. Многие наши счастливые пациенты, избавившись от боли, согласятся с этим. Однако неправильно выполненные методики нельзя считать успешными только на основании отсутствия у пациента явных симптомов.
Мы сами являемся самыми строгими критиками и устанавливаем слишком жесткие критерии успеха. При онкологических заболеваниях врачи считают успехом выживаемость в течение 5 лет, а при протезировании бедренной кости — в течение 3-5 лет. Являются ли эти цифры произвольными? Имеют ли они реальную основу? Считают ли врачи их обоснованными, если большинство их пациентов укладываются в этот 3-5-летний срок? Должны ли мы, подобно этому, стремиться добиться кратковременного успеха или в стоматологии нужно предвидеть отдаленные неудачи?
Мы не должны обманывать себя. Неудачи случаются, и будут встречаться, несмотря на большие старания врачей и постоянное совершенствование методик. Наши цели могут быть благородными и высокими, однако мы не всегда можем достичь их, и зачастую это происходит из-за того, что мы имеем дело с человеческим организмом, который не всегда ведет себя так, как написано в книгах.
Новые варианты при лечении глубокого кариеса
В лечении кариозных процессов важно не только владеть мануальными навыками и быть в курсе новинок пломбировочных материалов, но и также знать биологические особенности кариеса и пульпы зуба. Больше не существует необходимости препарировать зуб, далеко выходя за границы здоровых тканей, напротив, с развитием адгезивной стоматологии, мы стараемся производить иссечение тканей максимально консервативно. Даже удаление тканей, которые потенциально могут быть инфицированы, остается под вопросом.
Данная статья обсуждает лечение глубокого кариозного процесса, а также пытается ответить на некоторые вопросы, поставленные в стоматологической литературе. Необходимо ли удалять все кариозные ткани в каждом клиническом случае (даже когда экскавация близко к пульповой камере)? Может ли кариозный процесс быть остановлен? Какой вид пломбировочного материала обеспечит самый лучший результат для пациента?
Традиционные концепции
В классическом тексте (1908) G.V.Black писал: «Лучше обнажить пульпу зуба, чем оставить ее закрытой лишь слоем размягченного дентина». В тоже самое время Black утверждал, что дантисты должны понимать патанатомию и патофизиологию кариозного процесса, иначе они могут считать себя лишь механиками. Конечно же, стоматологическая наука продвинула наше понимание о кариозном процессе и возможности герметичного пломбирования с воссозданием борозд и фиссур. Сам G.V. Black возможно опроверг бы свое высказывание 100 лет спустя.
Традиционная концепция полного удаления кариозных тканей при глубокой полости была поставлена под сомнение. Абсолютное удаление всех измененных тканей может не являться обязательным для остановки кариозного процесса. Хорошо известно, что бактерии в дентине вызывают воспаление в пульпе. Однако этот слабый воспалительный процесс может быть стимулятором регенерации. Оставление небольшого количества кариозных тканей под пломбой необязательно пагубно повлияет на успех лечения. Короткие исследования от 36 до 45 месяцев показали, что надежно запломбированные полости с кариозным дентином, показали малый процент рецидива и абсолютное снижение числа микроорганизмов. Реминерализация оставшегося кариозного дентина доказана и биохимически, и рентгенологически. В данных исследованиях применялись прокладки с гидроокисью кальция.
Оставление кариозных тканей под пломбой весьма противоречивая концепция. Традиционный подход непрямого покрытия пульпы обычно требует временного пломбирования. Спустя несколько недель или месяцев, зуб повторно раскрывают, удаляют оставшиеся кариозные ткани и пломбируют повторно уже постоянно.
При непрямом методе деминерализованные ткани оставляются в самых глубоких местах полости для предотвращения вскрытия пульпы. Применение такого метода ограничивается пациентами без симптомов воспаления и патологии пульпы. Полное удаление всех кариозных тканей со стенок пульповой камеры необходимо для контроля микроподтека. Поражение может медленно или быстро прогрессировать. Клинически, рентгенологически и бактериологически доказано, что кариозный процесс останавливается. В таких случаях герметичная, хорошо прилегающая по краям реставрация является необходимым условием успешного исхода.
Смена ориентиров
Всеми давно принято, что использование силантов защищает подлежащие структуры зуба, предотвращая аккумуляцию зубного налета и потерю минералов. Совсем недавно, полученные доказательства показали, что купирование неполостных кариозных изменений возможно с применением силантов. Но пока данный неинвазивный способ лечения начального кариеса широко не внедрен в стоматологическую практику.
Конечный результат консервативного иссечения и полной экскавации был тщательно сравнен. В данном исследовании в случаях, когда постановка временной пломбы была возможна, глубокая экскавация не проводилась. На дне пульповой камеры оставлялся мягкий, влажный и дисколорированный дентин. Поверх кариозного дентина накладывалась прокладка из гидроокиси кальция, которая затем закрывалась временной пломбой из стекло-иономерного цемента. Спустя 8-12 недель полость заново раскрывалась с целью проведение окончательной экскавации. Прокладка гидроокиси кальция накладывалась еще раз, и зуб восстанавливался композитным материалом. Авторы наблюдали гораздо меньшее число вскрытых пульповых камер при проведении пошагового удаления кариозных тканей, нежели при полной радикальной экскавации.
Кроме того, при оценке отдаленных результатов спустя 1 год, приведенная методика также оказалась более успешной. Такие результаты в очередной раз поставили акцент на важности сохранения дентинного барьера между пульпой и полостью, даже если в нем остаются кариозные очаги.
Лечебные прокладки: эффект на пульпу зуба
Прокладки достаточно часто устанавливаются под реставрацию для снижения потенциальной полеоперационной чувствительности. Для идеальной прокладки важны следующие характеристики:
1. Способность материала уничтожать микроорганизмы
2. Индукция минерализации
3. Осуществлять плотное прилегание и изоляцию
Послеоперационная чувствительность частично связана с остаточной толщиной дентина (RDT) после препарирования и присутствия некоторого числа микроорганизмов на стенках полости. Никакой материал не сможет защитить пульпу лучше, чем собственный дентин. Остаточная толщина дентина по дну полости является одним самых важных факторов для защиты пульпы от токсинов. Толщина в 0,5 мм сокращает эффект токсинов на 75%, 1мм – 90%, сохранение 2 мм и более – приводит к невероятно малой реакции пульпы или вообще ее полном отсутствии. В ситуациях, когда остается около 0,5 мм применение прокладок особенно важно. Со снижением толщины дентинного слоя снижается выживаемость одонтобластов и сохранность репаративных механизмов.
Реактивное восстановление дентина наблюдалась под полостями как с RTD выше 0,5 мм, так и с RTD меньше 0,25 мм. Однако максимальная активность наблюдалась под полостями с RTD от 0,5 до 0,25. Также восстановление дентина находилось под влиянием выбранного материала (от большего к меньшему: гидроксид кальция, композит, модифицированный СИЦ и цинк-оксид эвгенол). Одонтобласты сохранялись при RTD больше 0,25 мм.
Гидроксид кальция используется в качестве материала для прокладок с 1920-х годов. Благодаря своему pH равному 11, гидроксид кальция сам по себе является бактерицидным, а также нейтрализует кислые продукты бактерий. Высокий pH создает хорошие условия для репарации дентина. Вдобавок, гидроксид кальция обладает способностью мобилизовать факторы роста дентинного матрикса, вызывающего образование нового дентина. Гидроксид кальция является идеальным прокладочным материалом для очень глубоких полостей как при прямом, так и непрямом покрытии пульпы.
Адгезивные смолы могут быть слишком кислыми и вызывать раздражение пульпы. А многие дентинные бондинговые агенты и модифицированные СИЦ вообще токсичны для ткани пульпы. Также прокладки из гидроокиси кальция показывают высокий потенциал для восстановления мягкой ткани зуба, по сравнению с цементами и смолами.
К сожалению, самоотверждаемые прокладки из гидроокиси кальция высоко растворимы и могут рассасываться с течением времени. Традиционные гидроокисные прокладки легко растворяются во время кислотного травления. Компоненты бонда: вода, ацетон, спирт также могут разрушительно действовать на свойства прокладок из кальция. Герметичное закрытие полости поможет стабилизировать поражение и остановить кариозный процесс. Таким образом, если планируется постановка композитной пломбы, поверх гидрооксидной прокладки следует устанавливать защитную прокладку из СИЦ.
Реставрационные материалы, которые обладают антимикробными свойствами, особенно полезны при малоинвазивных и других видах стоматологического вмешательства. Некоторые исследования показывают, что модифицированные СИЦ практически одинаковы с обычными гидроокись кальциевыми прокладками. Оставленный мягким, деминерализованным дентин становится вновь минерализованным после покрытия СИЦ. Это происходит в основном благодаря высвобождению фтора и наличия фосфата кальция в цементе. Этот феномен также называют «лечение пораженного дентина». Однако в некоторых других исследованиях модифицированный СИЦ пагубно влиял на однотобласты, сокращая их количество. Поэтому перед внесением модифицированного СИЦ в глубокую полость рекомендуется проложить хотя бы тонкий слой гидроокиси кальция. Это позволяет осуществить пульпу от повреждения и бактериального микроподтека.
В последние несколько лет проведена презентация MTA (ProRoot MTA Dentsply Tilsa Dental Specialties). Эти силикантные цементы являются антибактериальными, биосовместимыми, имеют высокий pH и позволяют высвобождать биоактивные протеины дентинного матрикса. MTA представляет собой порошок, состоящий из гидрофобного трикальций силиката, трикальций алюмината, трикальций оксида и силиката оксида. Также эта смесь содержит небольшое количество других оксидов, что модифицирует ее химические и физические свойства. Добавление жидкости к порошку приводит к образованию коллоидного геля с pH 12,5 (что схоже с гидроксилом кальция), который отверждается до плотной субстанции в течение 3-4 часов. Существует гипотеза, что под воздействием тканевой жидкости трикальций оксид превращается в гидроксид кальция.
Материал обладает слабой растворимостью и слегка более рентгеноконтрастен, чем дентин. Так как MTA весьма слабо устойчив к компрессиям, его не стоит использовать в высокофункциональных зонах. Другой значительный недостаток – это долгое отверждение: несколько часов.
Клинические случаи
Клинический случай 1
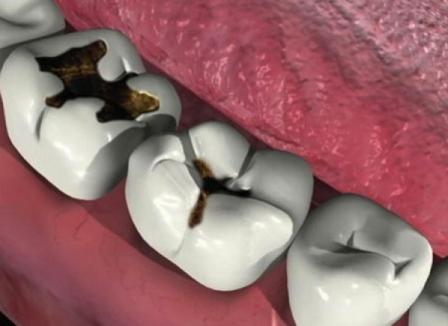
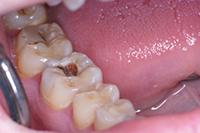
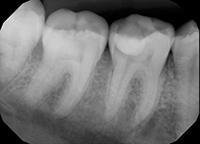
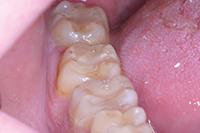
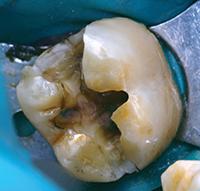
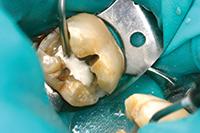
В клиническом случае представлен 30-летний пациент с большой кариозной полостью на первом нижнем моляре (Фото 1). Пациент отмечал чувствительность зуба к холодному, в остальном кариес протекал бессимптомно. Тест на холодное подтвердил слова пациента, болевой приступ длился около 30 секунд. Прицельный рентгеновский снимок показал близкое прилегание полости к пульпе зуба. Экскавация кариозного дентина продолжалась, пока дентинная стенка приблизилась к толщине в 1 мм (Фото 2).
Фото 1. Крупная кариозная полость с минимальными симптомами.
Фото 2: Проведено частичное удаление кариозного дентина. Мягкий, влажный, измененный в цвете дентин на дне полости оставлен.
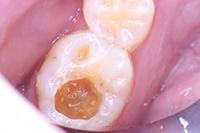
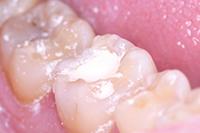
Биодентин (Septodont) использован для постановки временной пломбы (Фото 3). Зуб оставлен для восстановления на 4 месяца. В течение этого периода зуб не беспокоил. Для подтверждения витальности пульпы вновь проведен тест на холод и выполнен прицельный рентгеновский снимок (Фото 4). Было принято решение восстановить зуб композитом как окончательная реставрация (Фото 5).
Фото 4: Рентгенография временно запломбированного зуба. Оставшийся кариес хорошо заметен на снимке. На усмотрение стоматолога некоторое количество Биодентина может быть оставлено под постоянную реставрацию.
Фото 5: Окончательная реставрация зуба.
Обсуждение материала
Исходя из опыта автора, применение Биодентина является гораздо более удобным и эффективным по сравнению с MTA. Биодентин является биоактивным материалом для прямого и непрямого покрытия пульпы, а также в эндодонтической практике. Процесс изготовления биосиликатных материалов исключает металлическое загрязнение. Процесс отверждения наступает при увлажнении трикальций силиката, который затем образует кальций-силикатный гель и гидроксид кальция. При соединении этих веществ с фосфат ионами происходит образование преципитата, напоминающего гидроксиапатит. «В месте соединения дентина и материала Биодентин происходит увеличение карбонатных соединений, что свидетельствует о диффузии минералов из материала с созданием гибридной зоны». Биодентин препятствует микроподтеку схоже с модифицированным СИЦ и также имеет антибактериальный эффект.
Биодентин окончательно отверждается через 10-12 минут. Это намного быстрее, чем время отверждения MTA, однако биодентин к тому же проявляет более высокую компрессионную устойчивость. Таким образом, он может с легкостью применять как подходящая временная пломба. Производитель рекомендует использовать материал 2-шагово. На последующем приеме стоматолог формирует нужную ему полость и оставляет на дне слой Биодентина в качестве прокладки, сверху которой устанавливает постоянная реставрация.
Клинический случай 2
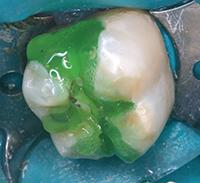
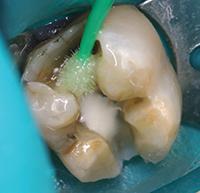
Нижний моляр на фото 6 имел дефект амальгамной пломбы с рецидивом кариеса. Пломба удалена, измененный дентин удален. На дно полости при помощи шприца тонким слоем наложена прокладка TheraCal LC (BISCO Dental Products) (Фото 7) и затем отверждена светом в течение 20 секунд. Полость протравлена (Фото 8), промыта, покрыта адгезивом, подсушена и отверждена (Фото 9), теперь зуб готов к постановке постоянной пломбы.
Фото 6: Глубокая экскавация дентина.
Фото 7: В качестве прокладки использован светоотверждаемый модифицированный кальций-силикатный материал TheraCal (BISCO Dental Products).
Фото 8 и 9: Кислотное протравливание и установка пломбы производится поверх прокладки.
Обсуждение материала
Материал обладает сильными механическими характеристиками, низкой растворимостью и может быть отвержден слоем в 1 мм. TheraCal LC является одобренным стимулятором образования гидроксиапатита со способностью индуцировать синтез кристаллов, схоже с продуктами МТА.
Дентинная жидкость, поглощаемая TheraCal, производит высвобождение кальция и гидроксид ионов. Кальций необходим для быстрой стимуляции синтеза апатита, а щелочная среда обеспечивает необходимые условия для восстановления и заживления. TheraCal LC предназначен для использования в качестве изолирующей прокладки, надежно защищающей пульпу. При прямом покрытии пульпы важными аспектами успешного лечения является использование коффердама и контроля пульпарного кровотечения. Материал подходит специалистам, которые хотят облегчить использование обычных прокладок из гидроксида кальция, но, тем не менее, хотят применить плюсы более новых кальций силикатов. TheraCal LC позволяет производить непрямое покрытие пульпы одноэтапно.
Заключение
Сегодня стоматологу необходимо анализировать предыдущий опыт и клинические случаи для осуществления оптимального лечения пациента. На данный момент имеется значительное количество литературы, описывающей успешное непрямое покрытие пульпы. В то же самое время анализ информации позволяет сделать вывод, что прямое покрытие, особенно в зрелых зубах, не может обеспечить такой же успех без эндодонтической терапии. Также существуют ситуации, когда стоматологи предпочитают провести непрямое покрытие и затем осуществить повторный вход в полость для удаления остатков кариозных тканей.
Данная статья показывает, что пошаговая техника удаления дентина не всегда необходима. Новые кальций-силикатные цементы могут быть особенно полезными в таких случаях. Для общего принятия такой концепции, конечно же, необходимо продолжение клинических исследований. Также стоматологам следует знать, что в некоторых случаях материал, покрывающий пульпу, следует удалять не полностью и оставлять под постоянную реставрацию.