в течении какого времени происходит обновление половины белка
Все, что вы хотели знать о яйцеклетках. Мнение врача-гинеколога.
По статистике к 35 годам в организме женщины остается около 25-70 тысяч яйцеклеток. С возрастом яйцеклеток не только становится меньше, кроме этого, они постепенно теряют в своем качестве. Поэтому, чем старше женщина, тем острее стоит вопрос с беременностью и рождением здорового ребенка.
Врач-гинеколог КЛИНИКИ21 Федорова Ольга Аркадьевна ответила на часто задаваемые вопросы пациенток:
Фолликулы с яйцеклетками закладываются во время внутриутробного развития плода женского пола на сроке от 8 недель до 12 недель беременности. При нормальном течении беременности закладывается около 9 млн фолликулов. Если мама болеет в эти сроки беременности, принимает какие-то ЛВ самостоятельно, работает на вредном производстве, имеет вредные привычки, подвергается любым облучениям (особенно в области малого таза), неправильно питается – все это приведет к тому, что закладывается меньшее количество яйцеклеток.
К моменту рождения девочки в ее яичниках остается около 2 млн яйцеклеток, некачественные, «битые», подвергаются атрезии и не развиваются, проходит естественный отбор генетического материала, а также патологическое течение беременности с развитием хронической плацентарной недостаточности.
Ограничен ли запас яйцеклеток?
С момента рождения и до начала полового созревания погибает большее количество фолликулов в результате перенесенных вирусных заболеваний (ОРВИ, ветряная оспа и другие детские инфекции) с высокой температурой, прием ЛВ, иногда бесконтрольно, без назначения врача и не учитывая возрастные дозы, или даже прием препаратов, противопоказанных для детей. К моменту менархе (начало менструаций) остается около 400 тысяч яйцеклеток.
Можно ли восстановить яйцеклетки?
Можно ли восстановить яйцеклетки, увеличить овариальный резерв и продлить жизнь яичников? Определенное количество яйцеклеток девочка получает от рождения, затем оно постепенно уменьшается. Больше яйцеклетки организмом не вырабатываются, а оставшиеся испытывают все негативные воздействия.
Поэтому для рождения здорового ребенка бесполезно воздерживаться от вредных привычек непосредственно перед беременностью, нужно вести здоровый образ жизни с самого детства.
Что влияет на количество яйцеклеток?
С менархе в каждом менструальном цикле происходит созревание и овуляция 1, редко 2 фолликулов. Кроме доминантного фолликула погибают еще ее окружение («свита») до 10-15 фолликулов. Чем раньше начались менструации, чем короче менструальный цикл (норма 24-35 дней), тем больше яйцеклеток «тратится». Когда запас яйцеклеток заканчивается в яичниках, женщина уходит в менопаузу (норма старше 45 лет), или раннюю менопаузу (40-45 лет) или происходит преждевременное истощение яичников и наступает менопауза до 40 лет.
Что помогает сохранить яйцеклетки в организме женщины?
Беременность и кормление грудью, когда у женщины не происходит овуляция и нет менструации. Сохраняют ли гормональные контрацептивы яйцеклетки, так как они тоже блокируют овуляцию? Тут мнение специалистов расходятся.
В нашем организме все время происходит естественный отбор, и в овуляцию идет самая здоровая и качественная яйцеклетка. Соответственно в 20-35 лет вероятность родить здорового ребенка намного выше. Ведь потом овулируют те яйцеклетки, которые не прошли естественный отбор в 20 лет.
Что способствует более быстрому истощению яичников?
Факторов очень много:
1. Вредные привычки. Любые. Чем раньше появляются вредные привычки, тем больший урон наносят на количество и качество яйцеклеток, которые находятся у девушки (женщины) в яичниках. При планировании беременности, когда женщина отказывается от вредных привычек, прекращается дальнейшее воздействие вредных факторов на яйцеклетки, но яйцеклетки не восстанавливаются.
2. Инфекции, передаваемые половым путем (гонококки, хламидии, мико-уреаплазмы и др).
3. Оперативные вмешательства на яичнике по поводу кист яичников, апоплексии яичников, эндометриоза яичников и т.д.
4. Хронические воспалительные заболевания яичников.
5. Избыточные физические нагрузки, спортивное питание.
6. Аутоиммунные заболевания. Иногда иммунная система женщины начинает вырабатывать антитела против ткани собственных яичников, часто сочетается с аутоиммунным тиреоидитом, СД и др.
7. Химиотерапия, радиооблучение или другая терапия онкозаболеваний. Если женщине репродуктивного возраста предстоит пройти лечение по поводу онкозаболевания, а она не выполнила свою репродуктивную функцию (нет детей), есть возможность заморозки яйцеклеток или ткани яичника до начала терапии.
8. Стрессы. Как ни странно.
Как определить количество яйцеклеток?
Как определить сколько яйцеклеток осталось в организме женщины?
Для этого можно сдать анализ крови на:
Не зря, еще в старину, говорили, что во время беременности закладывается репродуктивное здоровье на 2 поколения вперед: детей и внуков. Берегите репродуктивное здоровье смолоду.
Здоровье наших будущих детей, в основном, в наших руках.
Периодичность ОБНОВЛЕНИЯ организма человека
Наш организм великолепный и гениальный. Что нам нужно только — не мешать ему работать. Ну и естественно, не кормить его всякой ядовитой гадостью.
Отказавшись от ядов и начав питаться здоровой пищей, мы через какое-то время получим совершенно здоровый организм, если конечно до этого не имели каких-то очень тяжёлых заболеваний. Но мои любимые учёные, говорят, что даже тяжёлые заболевания можно значительно облегчить и со временем вылечить, перейдя на правильное питание.
Так вот к чему я это всё.
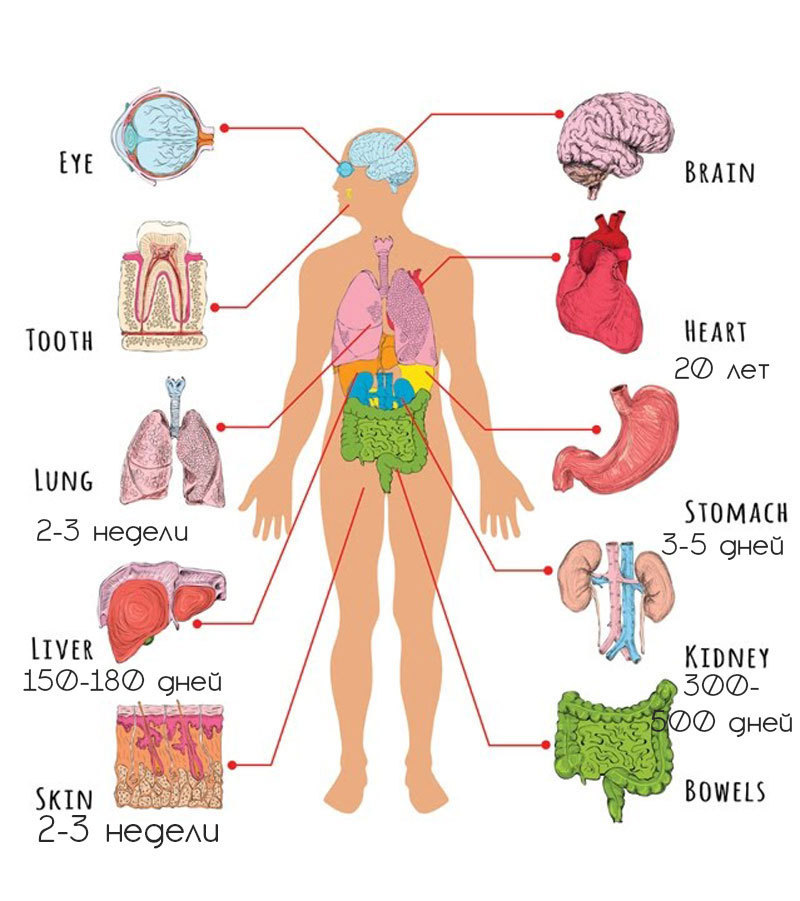
Все клетки нашего организма постоянно обновляются, и мы имеем, с какой-то периодичностью (у каждого органа свой период), совершенно новые органы.
Кожа: быстрее всего обновляется наружный слой кожи, соприкасающийся с окружающей средой. Клетки эпидермиса обновляются каждые 2-3 недели. Более глубокие слои чуть медленнее, но в среднем за 60-80 дней происходит полный цикл обновления кожи. Кстати, интересная информация: за год организм вырабатывает около двух миллиардов новых клеток кожи.
Но тогда встаёт вопрос, почему же у годовалого ребёнка и у шестидесятилетнего человека кожа выглядит совершенно по-разному. Очень много неизученного в нашем организме, но пока считается, что кожа стареет из-за ухудшения (с годами) выработки и обновления коллагена, с чем это связано пока ещё в стадии изучения.
На данный момент установлено только, что весьма существенными являются такие факторы, как неправильное и плохое (отсутствие жиров и нехватка белков) питание, а так же слишком агрессивное влияние окружающей среды.
Они ухудшают выработку и качество коллагена. Переизбыток ультрафиолета так же негативно влияет на регенерацию кожи. Но, 20-30 минут на солнце считаются терапевтической дозой, благотворно влияющей на многие процессы в организме, в том числе и обновление кожи.
Клетки эпителия, покрывающего желудок и кишечник, контачат с самой агрессивной средой (желудочные соки и ферменты, перерабатывающие пищу) и истончаются, постоянно проходящей по ним пищей. Они обновляются каждые 3-5 дней!
Схема строения слизистой языка очень сложная, и мы не будем вдаваться в подробности. Скорость обновления различных клеток составляющих слизистую оболочку языка (рецепторы) различна. Упрощённо можно сказать, что цикл обновления этих клеток составляет 10-14 дней.
Кровь — жидкость, от которой зависит вся наша жизнь. Ежедневно в теле среднестатистического человека погибает около половины триллиона различных клеток крови. Они должны вовремя умереть, чтобы зародились новые. В организме здорового человека число мёртвых клеток равно числу новорожденных. Полное обновление крови происходит в течение 120-150 дней.
Бронхи и лёгкие тоже контактируют с агрессивной средой, потому относительно быстро обновляют свои клетки. Наружные клетки лёгких, являющиеся первым слоем обороны от агрессоров, обновляются за 2-3 недели. Остальные клетки, в зависимости от их функций обновляются с различными скоростями. Но в целом, чуть менее года необходимо организму для полного обновления тканей лёгких.
Альвеолы бронхов обновляются каждые 11-12 месяцев.
Волосы растут в среднем на 1-2 см в месяц. То есть через какое-то время мы имеем полностью новые волосы в зависимости от длины.
Жизненный цикл ресниц и бровей 3-6 месяцев.
Ногти на пальцах рук растут со скоростью 3-4 мм в месяц, цикл полного обновления составляет 6 месяцев. На пальцах ног ногти растут со скоростью 1-2 мм в месяц.
Печень, поистине самый волшебный орган в нашем организме. Мало того, что он всю жизнь очищает нас от всего того мусора, который мы засовываем в наш организм, так она ещё и чемпион регенерации. Установлено, что даже при потере 75% своих клеток (в случае оперативного вмешательства), печень способна восстановится полностью, и уже через 2-4 месяца мы имеем полный её объём.
При чём, в возрасте до 30-40 лет, она регенерирует объём даже с лихвой – на 113%. С возрастом восстановление печени происходит лишь на 90-95%.
Полное обновление клеток печени происходит за 150-180 дней. Установлено так же, что если полностью отказаться от отравляющих продуктов (химикаты, лекарства, жареное, сахар и алкоголь) печень самостоятельно и полностью (!) очищается от вредных последствий за 6-8 недель.
Клетки почек и селезёнки обновляются каждые 300-500 дней.
Скелет нашего тела ежедневно вырабатывает сотни миллионов новых клеток. Он постоянно регенерирует, и в структуре своей имеет и старые и новые клетки. Но полное клеточное обновление структуры костей происходит за 7-10 лет. При существенных перекосах питания, клеток вырабатывается гораздо меньше и худшего качества, и как следствие, с годами, мы имеем такую проблему, как остеопороз.
Клетки всех видов мышечной ткани полностью обновляются за 15-16 лет.
Сердце, глаза и мозг до сих пор меньше всего изучены учёными.
Очень долгое время считалось, что мышцы сердца не обновляются (в отличие от всей остальной мышечной ткани), но недавние открытия показали, что это заблуждение, и мышечная ткань сердца обновляется так же, как и остальные мышцы.
Изучения только начаты, однако по предварительным данным известно — полное обновление сердечных мышц происходит приблизительно (точных данных пока нет) за 20 лет. То есть 3-4 раза за среднестатистическую жизнь.
Загадкой до сих пор является тот факт, что хрусталик глаза совершенно не обновляется, вернее, почему не обновляется хрусталик. Восстанавливаются и обновляются только клетки роговицы глаза. Цикл обновления достаточно быстр – 7-10 дней. При повреждениях, роговица способна восстановится всего за сутки.
Однако это не отменяет того, что клетки хрусталика не обновляются вообще никогда! Центральная часть хрусталика формируется на шестой неделе внутриутробного развития плода. И всю оставшуюся жизнь к центральной части хрусталика «прирастают» новые клетки, что делает его более толстым и менее гибким, с годами ухудшая качество фокусировки.
Мозг — вот уж загадка из загадок…
Мозг является самым малоизученным органом нашего тела. Конечно, это сопряжено с рядом объективных факторов. Мозг живого человека очень сложно изучить, не причинив ему вреда. Запрещены у нас эксперименты на людях (по крайней мере, официально). Потому исследования проходят на животных и смертельно больных человеческих особях-добровольцах, что совсем не равнозначно со здоровым, нормально функционирующим человеком.
До недавнего времени считалось, что клетки мозга не обновляются никогда. В принципе, воз и ныне там. Мозг, который контролирует всю нашу наисложнейшую систему под названием организм, мозг, который даёт сигналы для регенерации всем нашим органам, сам не обновляется вообще… Хм.
Ещё в 60-е годы прошлого столетия Жозеф Олтман открыл нейрогенез (рождение новых нейронов), в таламусе и коре головного мозга. Учёный мир, по обыкновению своему, отнёсся к этому открытию весьма скептически и об этом позабыли. В середине 80-х годов это открытие «открыл» заново другой учёный — Фернандо Ноттебум. И опять тишина.
Но с конца 90-х годов прошлого столетия начались, наконец, полномасштабные изучения нашего с вами мозга.
На нынешний момент (в ходе новейших исследований) сделано несколько открытий. Уже достоверно установлено, что гиппокамп и обонятельная луковица, всё же регулярно обновляют свои клетки. У птиц, низших позвоночных и млекопитающих скорость возникновения новых нейронов достаточно велика. У взрослых крыс в течение месяца образуется и замещается примерно 250 000 новых нейронов (это примерно 3% от общего числа).
Человеческий организм так же обновляет клетки этих отделов мозга. Установлено так же, что чем активнее физическая и мозговая деятельность, тем активнее образуются новые нейроны в этих областях. Но всё ещё находится в стадии изучения. Ждём-с…
За последние 20 лет наука сделала огромные шаги в изучении нашего питания и зависимости от него нашего здоровья. Выяснили, наконец, что большую роль в правильной работе органов играет правильное питание. Достоверно выяснено — что нам есть необходимо, а что есть не стоит, если хотим быть здоровыми. Но в целом? Что же выходит в целом? А выходит, что «подетально» мы обновляемся без остановки, всю свою жизнь. Так что же заставляет нас болеть, стареть и умирать?
Мы летаем в космос, думаем о завоевании и колонизации других планет. Но при этом так мало знаем о нашем теле. Учёные, что в древние времена, что в нынешние, совершенно не имеют понятия, отчего же при такой огромной способности к обновлению мы стареем. Почему появляются морщины, и ухудшается состояние мышц. Почему мы теряем гибкость и наши кости становятся хрупкими. Почему мы глохнем и глупеем… Никто, ничего вразумительного сказать, по-прежнему, не может.
Некоторые говорят, что старение заложено в нашей ДНК, однако эта теория не имеет доказательной базы, подтверждающей её.
Другие считают, что старение заложено в нашем мозге и психологии, что мы, как бы, сами себя заставляем стареть и умирать. Что в нашем подсознании заложены программы старения. Тоже просто теория без каких-либо доказательств и подтверждений.
Третьи (совсем свежие теории) считают, что это происходит вследствие «накопления» определённых мутаций и повреждений в митохондриальной ДНК. Но почему происходит накопление этих повреждений и мутаций они не знают.
То есть выходит, что вопреки теории эволюции товарища Дарвина, клетки, вновь и вновь обновляясь, возобновляют ухудшенную версию себя, вместо улучшенной. Странновато…
Оптимистичные «алхимики» считают, что эликсиром молодости мы наделены с рождения, и на стороне искать его незачем. Он находится внутри нас. Нужно лишь правильно подобрать ключи к нашему телу и научится правильно и в полной мере пользоваться своим мозгом.
И тогда наше тело будет, если не бессмертным, то очень и очень долгоживущим!
Давайте будем правильно кормить наше тело. Мы чуть-чуть поможем ему, а вернее сказать не будем мешать ему всякими ядами, и оно в ответ отблагодарит нас хорошей работой и долгой, ЗДОРОВОЙ жизнью! опубликовано econet.ru
Понравилась статья? Напишите свое мнение в комментариях.
Подпишитесь на наш ФБ:
Алгоритм метаболизма

Решение организационных вопросов питания у лиц старших возрастов, разработка и назначение индивидуализированных рационов рационального, профилактического и лечебного питания в существенной степени зависит от правильной оценки врачом нутриционного статуса пожилого человека, особенностей состояния обменных процессов. Именно поэтому профессионально грамотный клиницист, участвующий в решении проблем лечебно-профилактического питания у лиц пожилого и старческого возраста, должен быть достаточно хорошо ориентирован в области основ клинической биохимии и физиологии питания стареющего организма.
Белковый обмен
Белки — сложные азотсодержащие биополимеры, мономерами которых служат аминокислоты (органические соединения, содержащие карбоксильные и аминные группы). Их биологическая роль многообразна. Белки выполняют в организме пластические, каталитические, гормональные, транспортные и другие функции, а также обеспечивают специфичность. Значение белкового компонента питания заключается прежде всего в том, что он служит источником аминокислот.
Аминокислоты делятся на эссенциальные и неэссенциальные в зависимости от того, возможно ли их образование в организме из предшественников. К незаменимым аминокислотам относятся гистидин, лейцин, изолейцин, лизин, метионин, фенилаланин, триптофан и валин, а также цистеин и тирозин, синтезируемые соответственно из метионина и фенилаланина. Девять заменимых аминокислот (аланин, аргинин, аспарагиновая и глутамовая кислоты, глутамин, глицин, пролин и серин) могут отсутствовать в рационе, так как способны образовываться из других веществ. В организме также существуют аминокислоты, которые продуцируются путем модификации боковых цепей вышеперечисленных (например, компонент коллагена — гидроксипролин — и сократительных белков мышц — 3-метилгистидин).
Большинство аминокислот имеют изомеры (D- и L-формы), из которых только L-формы входят в состав белков человеческого организма. D-формы могут участвовать в метаболизме, превращаясь в L-формы, однако утилизируются гораздо менее эффективно.
Взаимоотношение аминокислот
По химическому строению аминокислоты делятся на двухосновные, двухкислотные и нейтральные с алифатическими и ароматическими боковыми цепями, что имеет большое значение для их транспорта, поскольку каждый класс аминокислот обладает специфическими переносчиками. Аминокислоты с аналогичным строением обычно вступают в сложные, часто конкурентные взаимоотношения.
Так, ароматические аминокислоты (фенилаланин, тирозин и триптофан) близкородственны между собой. Хотя фенилаланин является незаменимой, а тирозин — синтезируемой из него заменимой аминокислотой, наличие тирозина в рационе как будто бы «сберегает» фенилаланин. Если фенилаланина недостаточно или его метаболизм нарушен (например, при дефиците витамина С) — тирозин становится незаменимой аминокислотой. Подобные взаимоотношения характерны и для серосодержащих аминокислот: незаменимой — метионина — и образующегося из него цистеина.
Триптофан в ходе превращений, для которых необходим витамин В 6 (пиридоксин), включается в структуру НАД и НАДФ, то есть дублирует роль ниацина. Приблизительно половина обычной потребности в ниацине удовлетворяется за счет триптофана: 1 мг ниацина пищи эквивалентен 60 мг триптофана. Поэтому состояние пеллагры может развиваться не только при недостатке витамина РР в рационе, но и при нехватке триптофана или нарушении его обмена, в том числе вследствие дефицита пиридоксина.
Аминокислоты также делятся на глюкогенные и кетогенные, в зависимости от того, могут ли они при определенных условиях становиться предшественниками глюкозы или кетоновых тел (см. табл. 1).
Таблица 1. Классификация аминокислот
| Виды | Эссенциальные аминокислоты | Неэссенциальные аминокислоты |
| Алифатические | Валин (Г), лейцин (К), изолейцин (Г, К) | Глицин (Г), аланин (Г) |
| Двухосновные | Лизин (К), гистидин (Г, К)* | Аргинин (Г)* |
| Ароматические | Фенилаланин (Г, К), триптофан (Г, К) | Тирозин (Г, К)** |
| Оксиаминокислоты | Треонин (Г, К) | Серин (Г) |
| Серосодержащие | Метионин (Г, К) | Цистеин (Г)** |
| Дикарбоновые и их амиды | Глутамовая кислота (Г), глутамин (Г), аспарагиновая кислота (Г), аспарагин (Г) | |
| Иминокислоты | Пролин (Г) |
Обозначения: Г — глюкогенные, К — кетогенные аминокислоты; * — гистидин незаменим у детей до года; ** — условно-незаменимые аминокислоты (могут синтезироваться из фенилаланина и метионина).
Необходимые азотсодержащие соединения
Поступление азотсодержащих веществ с пищей происходит в основном за счет белка и в менее значимых количествах — свободных аминокислот и других соединений. В животной пище основное количество азота содержится в виде белка. В продуктах растительного происхождения большая часть азота представлена небелковыми соединениями, также в них содержится множество аминокислот, которые не встречаются в организме человека и зачастую не могут метаболизироваться им.
Синтез пуриновых оснований
Человек не нуждается в поступлении с пищей нуклеиновых кислот. Пуриновые и пиримидиновые основания синтезируются в печени из аминокислот, а избыток этих оснований, поступивших с пищей, выводится в виде мочевой кислоты.
Прием белка
Обычный (но не оптимальный) ежедневный прием белка у среднестатистического человека составляет приблизительно 100 г. К ним присоединяется примерно 70 г белка, секретируемого в полость желудочно-кишечного тракта. Из этого количества абсорбируется около 160 г. Самим организмом в сутки синтезируется в среднем 240–250 г белка. Такая разница между поступлением и эндогенным преобразованием свидетельствует об активности процессов обратного восстановления исходного сложного химического соединения из «осколков», образовавшихся при его метаболизме (ресинтеза белков из аминокислот, а аминокислот из аммиака и «углеродных скелетов» аминокислот).
Азотное равновесие
Для здорового человека характерно состояние азотного равновесия, когда потери белка (с мочой, калом, эпидермисом и т. п.) соответствуют его количеству, поступившему с пищей. При преобладании катаболических процессов возникает отрицательный азотный баланс, который характерен для низкого потребления азотсодержащих веществ (низкобелковых рационов, голодания, нарушения абсорбции белка) и многих патологических процессов, вызывающих интенсификацию распада (опухолей, ожоговой болезни и т. п.). При доминировании синтетических процессов количество вводимого азота преобладает над его выведением, и возникает положительный азотный баланс, характерный для детей, беременных женщин и реконвалесцентов после тяжелых заболеваний.
После прохождения энтерального барьера белки поступают в кровь в виде свободных аминокислот. Следует отметить, что клетки слизистой оболочки желудочно-кишечного тракта могут метаболизировать некоторые аминокислоты (в том числе глутамовую кислоту и аспарагиновую кислоту в аланин). Способность энтероцитов видоизменять эти аминокислоты, возможно, позволяет избежать токсического эффекта при их избыточном введении.
Аминокислоты, как поступившие в кровь при переваривании белка, так и синтезированные в клетках, в крови образуют постоянно обновляющийся свободный пул аминокислот, который составляет около 100 г.
Путь белка
75 % аминокислот, находящихся в системной циркуляции, представлены аминокислотами с ветвящимися цепями (лейцином, изолейцином и валином). Из мышечной ткани в кровоток выделяются аланин, который является основным предшественником синтеза глюкозы, и глутамин. Многие свободные аминокислоты подвергаются трансформации в печени. Часть свободного пула инкорпорируется в белки организма и при их катаболизме вновь поступает в кровоток. Другие непосредственно подвергаются катаболическим реакциям. Некоторые свободные аминокислоты используются для синтеза новых азотсодержащих соединений (пурина, креатинина, адреналина) и в дальнейшем деградируют, не возвращаясь в свободный пул, в специфичные продукты распада.
Роль печени
Постоянство содержания различных аминокислот в крови обеспечивает печень. Она утилизирует примерно ⅓ всех аминокислот, поступающих в организм, что позволяет предотвратить скачки в их концентрации в зависимости от питания.
Первостепенная роль печени в азотном и других видах обмена обеспечивается ее анатомическим расположением — продукты переваривания попадают по воротной вене непосредственно в этот орган. Кроме того, печень непосредственно связана с экскреторной системой — билиарным трактом, что позволяет выводить некоторые соединения в составе желчи. Гепатоциты — единственные клетки, обладающие полным набором ферментов, участвующих в аминокислотном обмене. Здесь выполняются все основные процессы азотного метаболизма: распад аминокислот для выработки энергии и обеспечения глюконеогенеза, образование заменимых аминокислот и нуклеиновых кислот, обезвреживание аммиака и других конечных продуктов. Печень является основным местом деградации большинства незаменимых аминокислот (за исключением аминокислот с ветвящимися цепями).
Инсулиновый ответ
Синтез азотсодержащих соединений (белка и нуклеиновых кислот) в печени весьма чувствителен к поступлению их предшественников из пищи. После каждого приема пищи наступает период повышенного внутрипеченочного синтеза белков, в том числе альбумина. Аналогичное усиление синтетических процессов происходит и в мышцах. Эти реакции связаны прежде всего с действием инсулина, который секретируется в ответ на введение аминокислот и/или глюкозы.
Некоторые аминокислоты (аргинин и аминокислоты с ветвящимися цепями) усиливают продукцию инсулина в большей степени, чем остальные. Другие (аспарагин, глицин, серин, цистеин) стимулируют секрецию глюкагона, который усиливает утилизацию аминокислот печенью и воздействует на ферменты глюконеогенеза и аминокислотного катаболизма. Благодаря этим механизмам происходит снижение уровня аминокислот в крови после поступления их с пищей. Действие инсулина наиболее выражено для аминокислот, содержащихся в кровотоке в свободном виде (аминокислот с ветвящимися цепями), и малозначимо для тех, которые транспортируются в связанном виде (триптофана). Обратное инсулину влияние на белковый метаболизм оказывают глюкокортикостероиды.
Аминокислоты на «экспорт»
Печень обладает повышенной скоростью синтеза и распада белков по сравнению с другими тканями организма (кроме поджелудочной железы). Это позволяет ей синтезировать «на экспорт», а также быстро обеспечивать лабильный резерв аминокислот в период недостаточного питания за счет распада собственных белков.
Особенность внутрипеченочного белкового синтеза заключается в том, что он усиливается под действием гормонов, которые в других тканях производят катаболический эффект. Так, при голодании белки мышц, для обеспечения организма энергией, подвергаются распаду, а в печени одновременно усиливается синтез белков, являющихся ферментами глюконеогенеза и мочевинообразования.
Избыток белка и голодание
Прием пищи, содержащей избыток белка, приводит к интенсификации синтеза в печени и в мышцах, образованию избыточных количеств альбумина и деградации излишка аминокислот до предшественников глюкозы и липидов. Глюкоза и триглицериды утилизируются как горючее или депонируются, а альбумин становится временным хранилищем аминокислот и средством их транспортировки в периферические ткани.
При голодании уровень альбумина прогрессивно снижается, а при последующей нормализации поступления белка медленно восстанавливается. Поэтому хотя альбумин и является показателем белковой недостаточности, он низкочувствителен и не реагирует оперативно на изменения в питании.
7 из 10 эссенциальных аминокислот деградируют в печени — либо образуя мочевину, либо впоследствии используясь в глюконеогенезе. Мочевина преимущественно выделяется с мочой, но часть ее поступает в просвет кишечника, где подвергается уреазному воздействию микрофлоры. Аминокислоты с ветвящимися цепями катаболизируются в основном в почках, мышцах и головном мозге.
Роль мышц
Мышцы синтезируют ежедневно 75 г белка. У среднего человека они содержат 40 % от всего белка организма. Хотя белковый метаболизм происходит здесь несколько медленнее, чем в других тканях, мышечный белок представляет собой самый большой эндогенный аминокислотный резерв, который при голодании может использоваться для глюконеогенеза.
Мышцы являются основной мишенью воздействия инсулина: здесь под его влиянием усиливается поступление аминокислот, увеличивается синтез мышечного белка и снижается распад.
В процессе превращений в мышцах образуются аланин и глутамин, их условно можно считать транспортными формами азота. Аланин непосредственно из мышц попадает в печень, а глутамин вначале поступает в кишечник, где частично превращается в аланин. Поскольку в печени из аланина происходит синтез глюкозы, частично обеспечивающий мышцу энергией, получающийся круго- оборот получил название глюкозо- аланинового цикла.
К азотсодержащим веществам мышц также относятся высокоэнергетичный креатин-фосфат и продукт его деградации креатинин. Экскреция креатинина обычно рассматривается как мера мышечной массы. Однако это соединение может поступать в организм с высокобелковой пищей и влиять на результаты исследования содержания его в моче. Продукт распада миофибриллярных белков — 3-метилгистидин — экскретируется с мочой в течение короткого времени и является достаточно точным показателем скорости распада в мышцах — при мышечном истощении скорость его выхода пропорционально снижается.
Механизм голодания
В отсутствие пищи синтез альбумина и мышечного белка замедляется, но продолжается деградация аминокислот. Поэтому на начальном этапе голодания мышцы теряют аминокислоты, которые идут на энергетические нужды. В дальнейшем организм адаптируется к отсутствию новых поступлений аминокислот (снижается потребность в зависящем от белка глюконеогенезе за счет использования энергетического потенциала кетоновых тел) и потеря белка мускулатуры уменьшается.
Хотите больше новой информации по вопросам диетологии?
Оформите подписку на информационно-практический журнал «Практическая диетология»!
Роль почек
Почки не только выводят конечные продукты азотного распада (мочевину, креатинин и др.), но и являются дополнительным местом ресинтеза глюкозы из аминокислот, а также регулируют образование аммиака, компенсируя избыток ионов водорода в крови.
Глюконеогенез и функционирование кислотно-щелочной регуляции тесно скоординированы, поскольку субстраты этих процессов появляются при дезаминировании аминокислот: углерод для синтеза глюкозы и азот — для аммиака. Существует даже мнение, что именно производство глюкозы является основной реакцией почек на ацидоз, а образование аммиака происходит вторично.
Белок в нервной ткани
Для нервной ткани характерны более высокие концентрации аминокислот, чем в плазме. Это позволяет обеспечить мозг достаточным количеством ароматических аминокислот, являющихся предшественниками нейромедиаторов.
Некоторые заменимые аминокислоты, такие как глутамат (из которого при участии пиридоксина образуется гамма-аминомасляная кислота) и аспартат, также обладают влиянием на возбудимость нервной ткани. Их концентрация здесь высока, при этом заменимые аминокислоты способны синтезироваться и на месте.
Сон после еды
Специфическую роль играет триптофан, являющийся предшественником серотонина. Именно с повышением концентрации триптофана (а следовательно, и серотонина) связана сонливость после еды. Такой эффект особенно выражен при приеме больших количеств триптофана совместно с углеводистой пищей. Повышенная секреция инсулина снижает уровень в крови аминокислот с ветвящимися цепями, которые при преодолении барьера «кровь — мозг» обладают конкурентными взаимоотношениями с ароматическими аминокислотами, но в то же время не оказывает влияния на концентрацию связанного с альбумином триптофана. Благодаря подобным эффектам препараты триптофана могут использоваться в психиатрической практике.
При заболеваниях печени
Ограничение ароматических аминокислот в рационе, в связи с их влиянием на центральную нервную систему, имеет профилактическое значение при ведении пациентов с печеночной энцефалопатией. Элементные аминокислотные диеты с преимущественным содержанием лейцина, изолейцина, валина и аргинина помогают избежать развития белковой недостаточности у гепатологических больных и в то же время не приводят к возникновению печеночной комы.
Основные пластические функции протеиногенных аминокислот перечислены в таблице 2.
Таблица 2. Основные функции аминокислот
| Аланин | Предшественник глюконеогенеза, переносчик азота из периферических тканей в печень |
| Аргинин | Непосредственный предшественник мочевины |
| Аспарагиновая кислота | Предшественник глюконеогенеза, предшественник пиримидина, используется для синтеза мочевины |
| Глутаминовая кислота | Донор аминогрупп для многих реакций, переносчик азота (проникает через мембраны легче, чем глутамин), источник аммиака, предшественник ГАМК |
| Глицин | Предшественник пуринов, глютатиона и креатинина, входит в состав гемоглобина и цитохромов, нейротрансмиттер |
| Гистидин | Предшественник гистамина, донор углерода |
| Лизин | Предшественник карнитина (транспорт жирных кислот), составляющая коллагена |
| Метионин | Донор метальных групп для многих синтетических процессов (в т. ч. холина, пиримидинов), предшественник цистеина, участвует в метаболизме никотиновой кислоты и гистамина |
| Фенилаланин | Предшественник тирозина |
| Серин | Составляющая фосфолипидов, предшественник сфинголипидов, предшественник этаноламина и холина, участвует в синтезе пуринов и пиримидинов |
| Триптофан | Предшественник серотонина и никотинамида |
| Тирозин | Предшественник катехоламинов, допамина, меланина, тироксина |
| Цистеин | Предшественник таурина (желчные кислоты), входит в состав глютатиона (антиоксидантная система) |
Нормы потребления белка
Современные рекомендации по обеспечению пожилых людей и стариков основными питательными веществами, в первую очередь белками, свидетельствуют о целесообразном некотором снижении суточного количества белковых продуктов в пищевом рационе до 0,75–0,8 г/кг веса. Это связано с тем, что интенсивность основных физиологических функций с каждым десятилетием жизни человека после 50 лет снижается почти на 10 % (Rogers J., Jensen G., 2004), потребность белка уменьшается за счет инволюции синтетических и пластических процессов и ферментообразования, продукции гормонов, ряда биологически активных веществ, обеспечения мышечной деятельности и т. д.
Рекомендуемые нормы потребления для белка с учетом приведенных выше показателей составляют 55–62 г/сут (для мужчины весом 77 кг в возрасте 60–70 лет) и 45–52 г/сут (для женщины весом 65 кг в возрасте 60–70 лет) по выводам IV Американского национального исследования по оценке здоровья и питания (2006).
Вместе с тем установлено, что при сохранении физической активности пожилых людей (профессиональной физической нагрузки, занятий физкультурой, работы на дачном участке и т. п.) для поддержания азотного равновесия организма требуется повышение белкового обеспечения пожилого человека в количестве 1–1,25 г/кг в день. Эта же квота пищевого белка полностью обеспечит потребности пожилого человека, находящегося в состоянии стресса, болезни или ранения (Lowenthal D. T., 1990).
Рис. 1. Влияние пищевых веществ на развитие болезней избыточного питания (по А. А. Покровскому)
Дефицит белка = старение
Важно отметить, что организм пожилого человека очень чувствителен как к дефициту экзогенно поступающих белков, так и к их избытку. В условиях белкового дефицита прогрессирующе развиваются процессы дистрофии и атрофии клеточных структур, в первую очередь мышечной ткани, слизистых оболочек (желудочно-кишечного тракта, дыхательной системы и др.), паренхиматозных органов (поджелудочной железы, печени, эндокринных желез и др.), структур иммунной системы. Белковый дефицит питания активизирует процессы старения организма.
Механизмы патологического действия на организм пожилого и старого человека пищевой белковой перегрузки связаны в первую очередь с белковой «агрессией» печени и связанной с этим несостоятельностью ферментных систем, неполной деполимеризацией всех фракций белка, накоплением в крови токсических продуктов незавершенных окислительно-восстановительных реакций и т. д.
Белковая перегрузка
Интоксикационный процесс метаболического генеза при избыточном белковом питании пожилых и старых людей многократно усиливается по причине развития процессов гнилостной кишечной диспепсии в условиях относительной ферментной недостаточности желудка, поджелудочной железы, тонкой кишки и развития синдромов мальдигестии и мальабсорбции, а также кишечного дисбиоза (Барановский А. Ю., Кондрашина Э. А., 2008).
Белковая пищевая перегрузка в рамках интоксикационного синдрома способствует перевозбуждению центральной нервной системы, иногда — состояниям, близким к неврозам. При этом наблюдается повышенный расход витаминов в организме с формированием витаминной недостаточности.
При длительном высокобелковом питании вначале наблюдается компенсаторное усиление, а затем угнетение секреторной функции желудка и поджелудочной железы, повышается риск развития таких заболеваний, как подагра, мочекаменная болезнь.
В следующем выпуске журнала «Практическая диетология» мы продолжим рассказ о геронтологических особенностях основных видов обмена веществ пациентов пожилого и старческого возраста — углеводном и жировом обмене.
// ПД
Хотите больше новой информации по вопросам диетологии?
Оформите подписку на информационно-практический журнал «Практическая диетология»!