вакцина спутник какой этап испытаний прошла
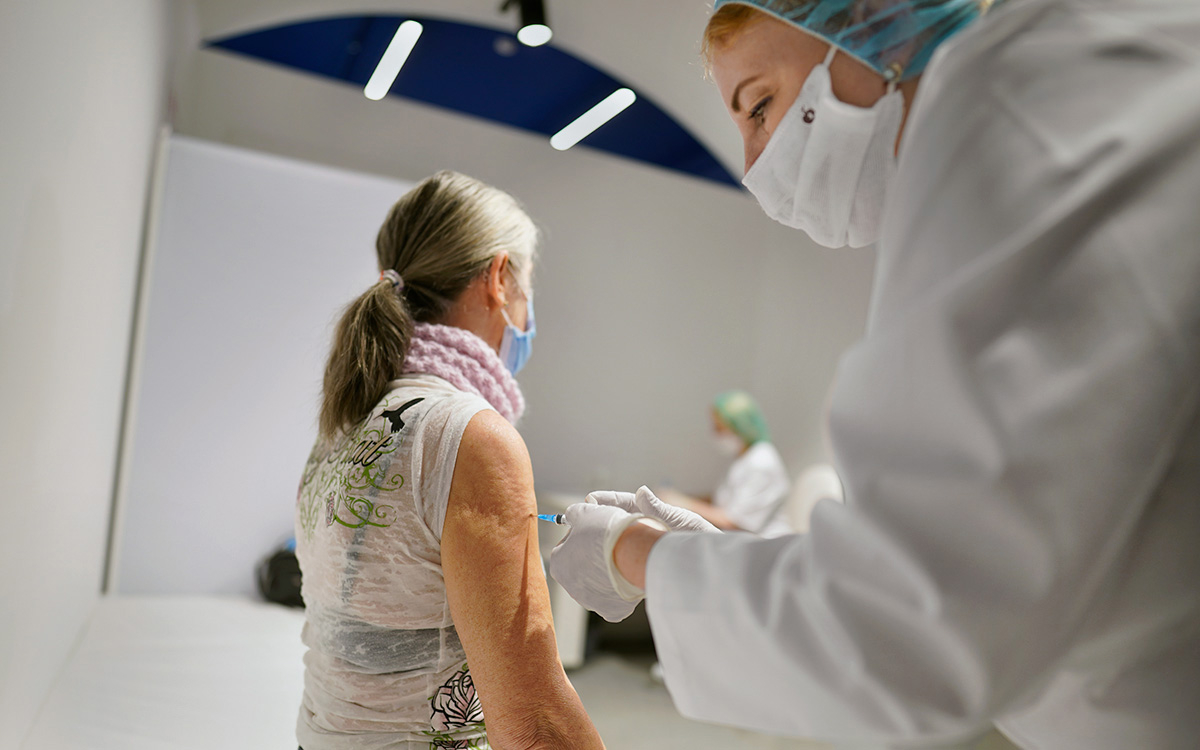
Клинические испытания
Клинические испытания
Прежде чем приступать к клиническим испытаниям, вакцина прошла в полном объеме все стадии доклинических испытаний по эффективности и безопасности, которые включали эксперименты на различных видах лабораторных животных, в том числе на 2-х видах приматов.
Фаза 1 и 2 клинических испытаний вакцины были завершены 1 августа 2020 года. Все добровольцы хорошо перенесли испытания, не было зарегистрировано непредвиденных и серьезных нежелательных явлений, вакцина индуцировала формирование высокого как антительного, так и клеточного иммунного ответа. Ни один участник нынешнего клинического испытания не заразился коронавирусом после введения вакцины. Высокая эффективность вакцины была подтверждена высокоточными тестами на антитела в сыворотках крови добровольцев (в том числе проводили анализ на антитела, которые нейтрализуют коронавирус), а также способностью иммунных клеток добровольцев активироваться в ответ на S белок шипа коронавируса, что говорит о формировании и антительного и клеточного иммунного ответа в результате вакцинации.
Пострегистрационные клинические исследования с участием более 31 000 человек в России и Беларуси начались 25 августа 2020 года. Ряд стран, таких как ОАЭ, Индия и Венесуэла, начали местные клинические исследования вакцины «Спутник V». Вакцина получила регистрационное свидетельство Минздрава России 11 августа и в соответствии с правилами в связи с чрезвычайной ситуацией, принятыми во время пандемии COVID-19, может использоваться для вакцинации населения в России.
В ходе клинических испытаний фазы III вакцины «Спутник V» продемонстрировал высокую эффективность, иммуногенность и безопасность.
«Спутник V» обеспечивает полную защиту от клинических случаев тяжелой степени COVID-19 «Спутник V» гарантирует устойчивый гуморальный (выработка антител, являющихся первой линией защиты) и клеточный (долгосрочная защита) иммунный ответ.
Результаты клинических испытаний фазы III подтвердили высокий уровень безопасности и иммуногенности вакцины «Спутник V», в том числе для пожилых людей.
По результатам анализа 3,8 млн вакцинированных россиян эффективность вакцины «Спутник V» составила 97,6%.
Активное вещество вакцины Спутник V и способ его использования имеет патентную защиту на территории России, которая принадлежит Национальному исследовательскому центру эпидемиологии и микробиологии имени почетного академика Н. Ф. Гамалеи.
В России завершилась третья фаза испытаний «Спутник V»
Московский Центр им. Гамалеи завершил третью фазу испытаний вакцины от коронавируса «Спутник V», в котором в том числе участвовали пожилые люди. Об этом на заседании президиума координационного совета при правительстве по борьбе c коронавирусом заявил министр здравоохранения Михаил Мурашко.
«Мы проводили III фазу клинического исследования вакцины «Гам-КОВИД-Вак», или «Спутник V», которая завершилась с участием пациентов старше 60 лет», — сказал он.
Мурашко сообщил, что испытания показали высокую эффективность и безопасность вакцины, готовится итоговый отчет. «Получив уже новые данные о больших, даже огромных объемах исследования, в котором были задействованы более 23 тыс. человек, фактически мы видим хороший профиль безопасности, и институт Гамалеи разрабатывает новые показания для вакцинации и использования вакцины», — сказал министр.
Минздрав выдал разрешение на проведение III и IV фазы постклинических исследований «Спутника V» в августе. Они начались 25 августа и должны закончиться в декабре 2022 года, в них примут участие 40 тыс. человек. Около 10 тыс. добровольцев должны получить не препарат, а плацебо — вещество без явных лечебных свойств, говорил глава Центра им. Гамалеи Александр Гинцбург.
Российскую вакцину «Спутник V» зарегистрировали в России 11 августа 2020 года. Она стала первым в мире зарегистрированным препаратом от COVID-19. Применение этой вакцины для пожилых Минздрав одобрил в конце декабря.
Центр Гамалеи подал документы для постоянной регистрации «Спутника V»
Центр имени Н.Ф.Гамалеи, разработавший вакцину от коронавируса «Спутник V», завершил пострегистрационные испытания и подал необходимые документы для постоянной регистрации препарата. Об этом заявил директор центра Александр Гинцбург, передает «РИА Новости».
«Да, они завершились, документы поданы и они сейчас рассматриваются», — рассказал глава Центра.
«Спутник V» зарегистрировали в России 11 августа прошлого года до окончания исследований. Он стал первой в мире зарегистрированной вакциной от COVID-19. Препарат создан на платформе аденовирусных вирусов человека.
Разработчик начал третий этап пострегистрационных исследований в начале сентября прошлого года. Минздрав ожидал провести третью и четвертую фазы испытаний до конца декабря 2022 года. В них планировалось задействовать 40 тыс. человек; причем около 10 тыс. из них, согласно плану, получили вместо препарата плацебо — вещество, не имеющее лечебных свойств.
Третий этап испытаний завершился в конце сентября, в исследованиях приняли участие в том числе пожилые люди старше 60 лет. По словам главы Минздрава Михаила Мурашко, вакцина во время испытаний зарекомендовала себя как эффективная и безопасная. «Были задействованы более 23 тыс. человек, фактически мы видим хороший профиль безопасности», — указал он.
«Спутник V» пока не одобрен для применения Всемирной организацией здравоохранения (ВОЗ). Там полагают, что препарат может получить одобрение к концу этого года в случае подписания некоторых важных документов. «Если документы будут подписаны в ближайшие пару дней, после чего оценка возобновится, то очень возможно, что инспекция также произойдет до конца года и процесс может быть завершен», — сообщила представитель ВОЗ Сумия Сваминатан.
Кроме того, в России проходят испытания «Спутника V» на подростках 12–17 лет, они начались в июле. Исследования проходят на базе двух столичных медучреждений — Морозовской детской больницы и Детской больницы им. Башляевой при участии 100 добровольцев; позднее к ним присоединятся еще 250 подростков. Гинцбург отмечал, что несовершеннолетним введут тот же препарат, что и взрослым, но в меньшей дозировке. По его словам, к середине июля только у двоих медики выявили повышенную температуру.
Российские вакцины не прошли все фазы клинического исследования?
Клинические исследования во всем мире являются неотъемлемым этапом разработки препаратов, который предшествует его регистрации и широкому медицинскому применению. В ходе клинических исследований новый препарат изучается для получения данных о его эффективности и безопасности. На основании этих данных уполномоченный орган здравоохранения принимает решение о регистрации препарата или отказе в регистрации.
Проведение клинических исследований в РФ регламентируют: Федеральный закон от 12.04.2010 N 61-ФЗ «Об обращении лекарственных средств» (Статья 40. Проведение клинического исследования лекарственного препарата для медицинского применения), ГОСТ Р 56701-2015 от 2016-07-01 ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ (УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 11 ноября 2015 г. N 1762-ст.), ГОСТ Р 52379-2005 от 2006-04-01 НАДЛЕЖАЩАЯ КЛИНИЧЕСКАЯ ПРАКТИКА (УТВЕРЖДЕН Приказом Федерального агентства по техническому регулированию и метрологии от 27 сентября 2005 года N 232-ст), Правила надлежащей клинической практики ОСТ 42-511-99 (согласно международного стандарта этических норм и качества научных исследований Good Clinical Practice; GCP), Приказ Минздрава России от 01.04.2016 N 200н «Об утверждении правил надлежащей клинической практики» (Зарегистрировано в Минюсте России 23.08.2016 N 43357), приказ Минздрава России от 09.01.2014 № 2н «Об утверждении порядка проведения оценки соответствия медицинских изделий в форме технических испытаний, токсикологических исследований, клинических испытаний в целях государственной регистрации медицинских изделий».
Обычно выделяют четыре фазы клинических испытаний. Фаза I. Цель этапа — убедиться, что препарат можно применять у людей. Фаза II. Цель этапа — дополнительно оценить безопасность лекарства и выяснить, работает ли препарат. Фаза III. Цель этапа — сравнить новый препарат со стандартным лечением. Фаза IV называется постмаркетинговой — этот этап клинического испытания начинается, когда готовое лекарство уже поступает в продажу.
Существует государственный реестр лекарственных средств, который содержит перечень лекарственных препаратов, прошедших государственную регистрацию (Федеральный закон от 12.04.2010 N 61-ФЗ «Об обращении лекарственных средств» Статья 33), другими словами реестр разрешений на проведение клинических исследований (РКИ).
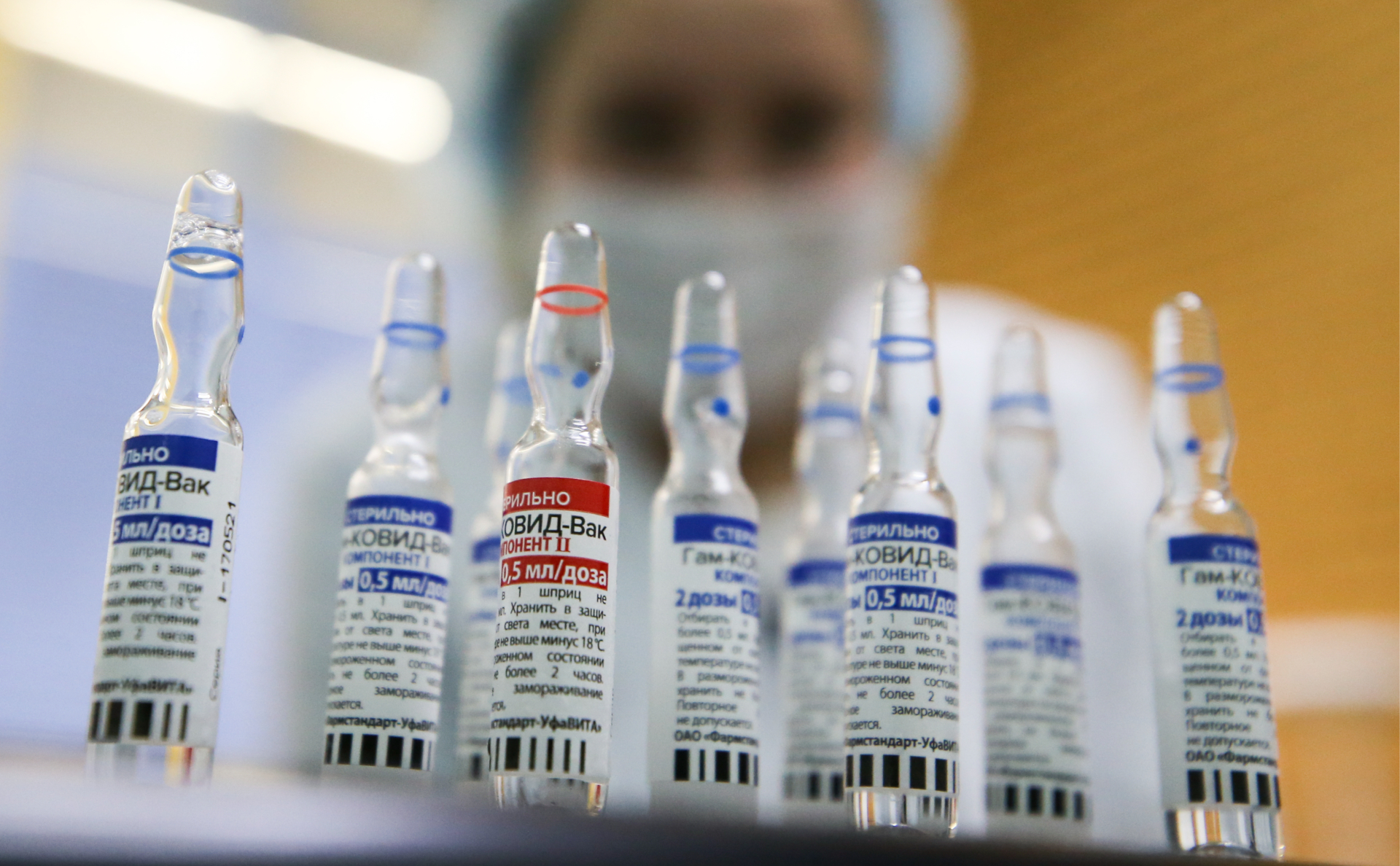
В настоящий момент, у Российской Федерации известно существование нескольких вакцин от коронавируса: «Спутник V» и «Спутник Лайт» («Гам-КОВИД-Вак», Национального исследовательского центра эпидемиологии и микробиологии имени Н. Ф. Гамалеи), «ЭпиВакКорона» (Федерального бюджетного учреждения науки «Государственный научный центр вирусологии и биотехнологии Вектор» Роспотребнадзора), «КовиВак» (Федерального научного центра исследований и разработки иммунобиологических препаратов имени М.П. Чумакова Российской академии наук).
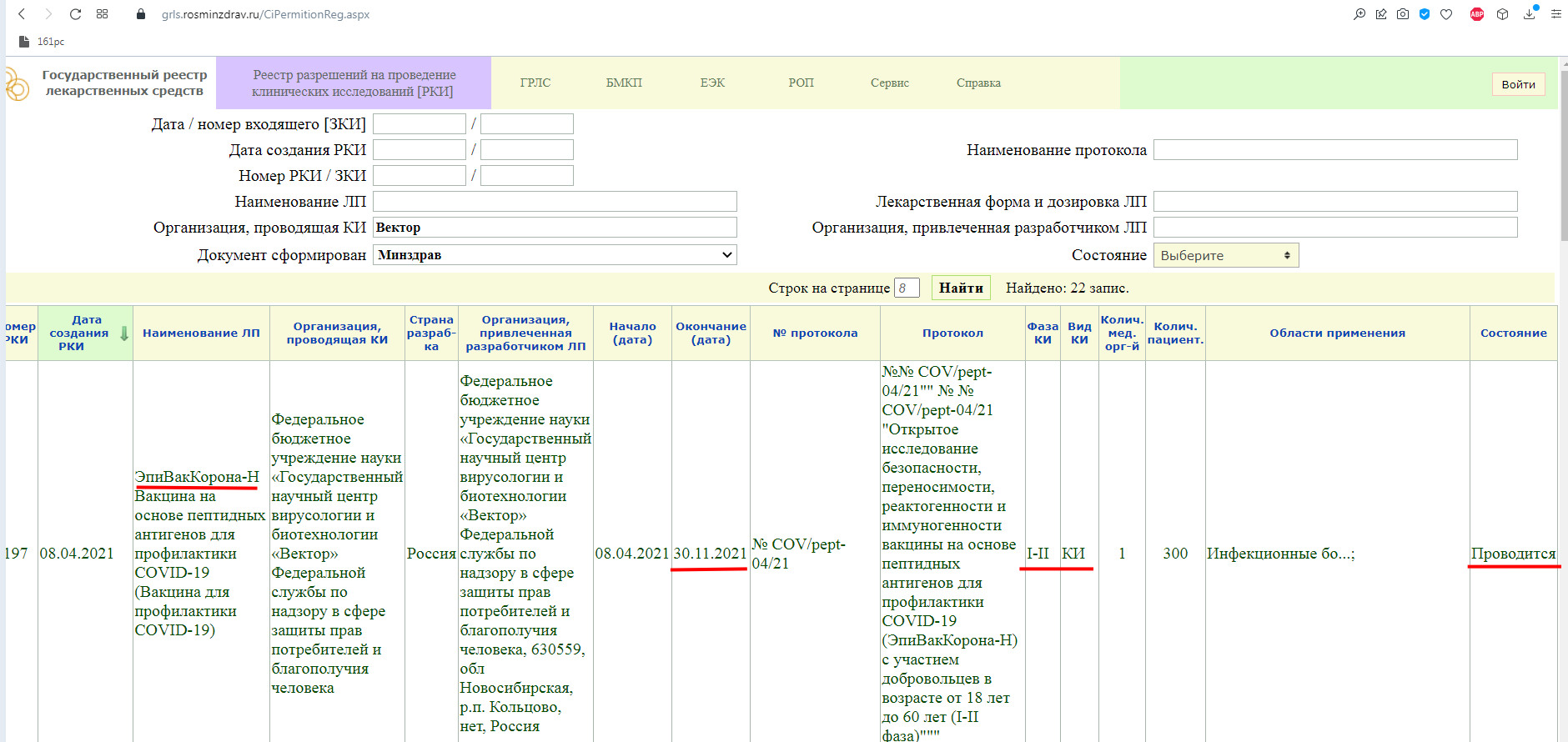
Как мы видим, в настоящий момент, проводится фаза клинического исследования 1-2 с участием добровольцев от 18 до 60 лет, и завершится она 30 ноября 2021 года.
Так же, проводится фаза клинического исследования 3-4 с участием добровольцев от 18 лет, и завершится она 31 августа 2021 года.
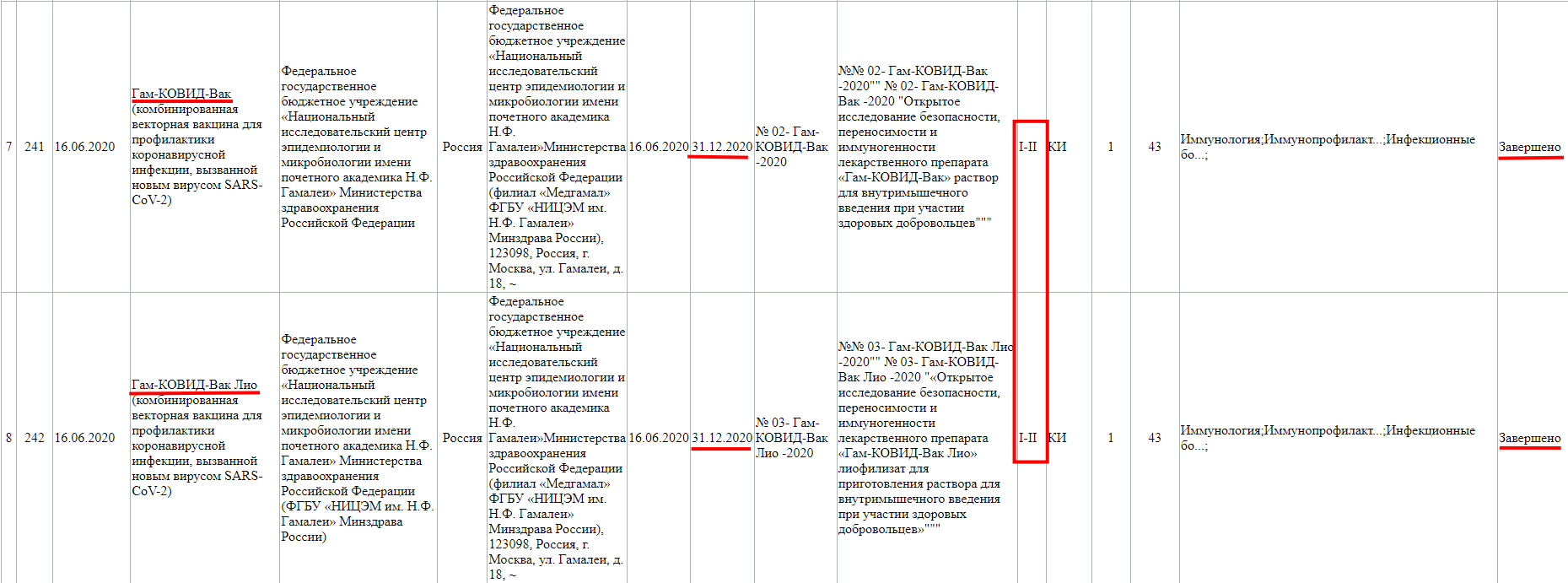
Завершенная фаза 3 клинического исследования, с участием добровольцев от 60 лет, и завершилась она 15 мая 2021 года.
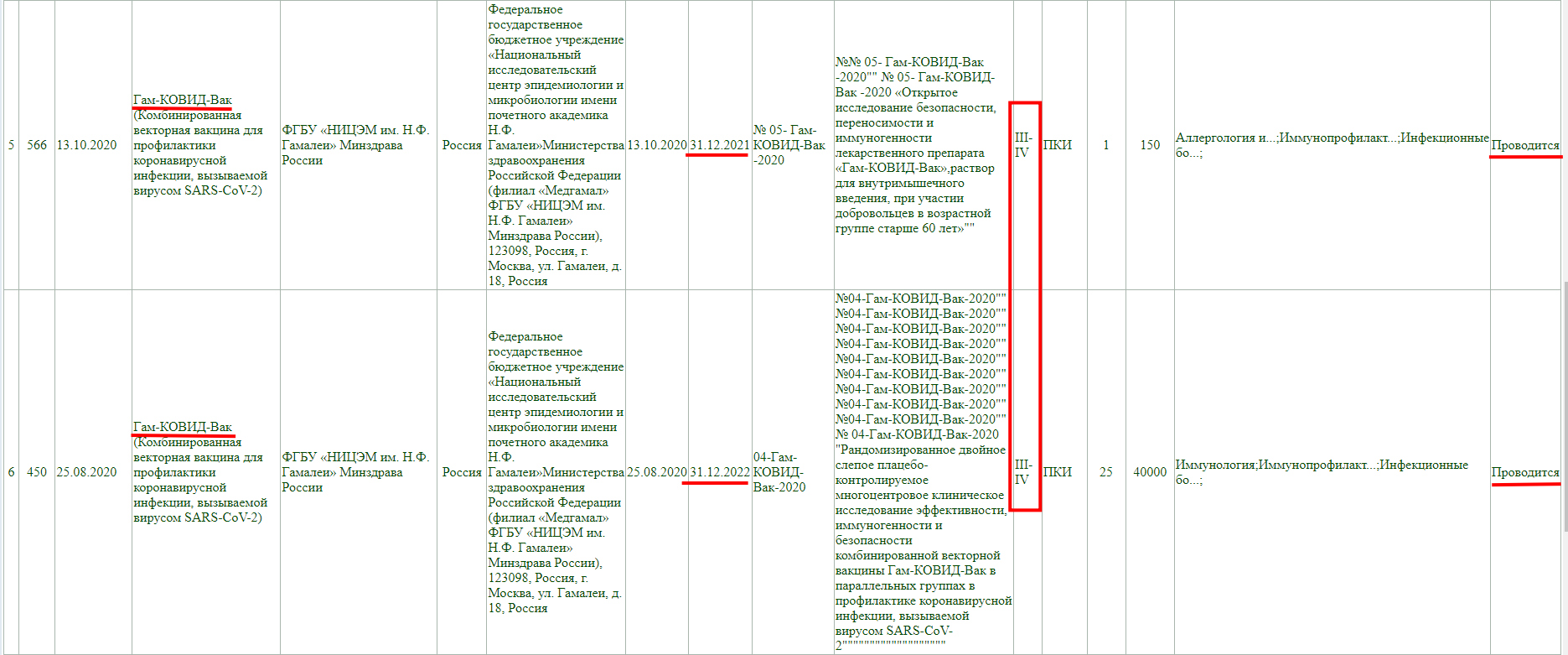
Фаза клинического исследования 1-2 с участием добровольцев от 18 до 60 лет, проводится до 30 декабря 2021 года.
Тут так же видно, что проводится фаза клинического исследования 3 с участием добровольцев от 18 до 60 лет, и завершится она 30 декабря 2022 года.
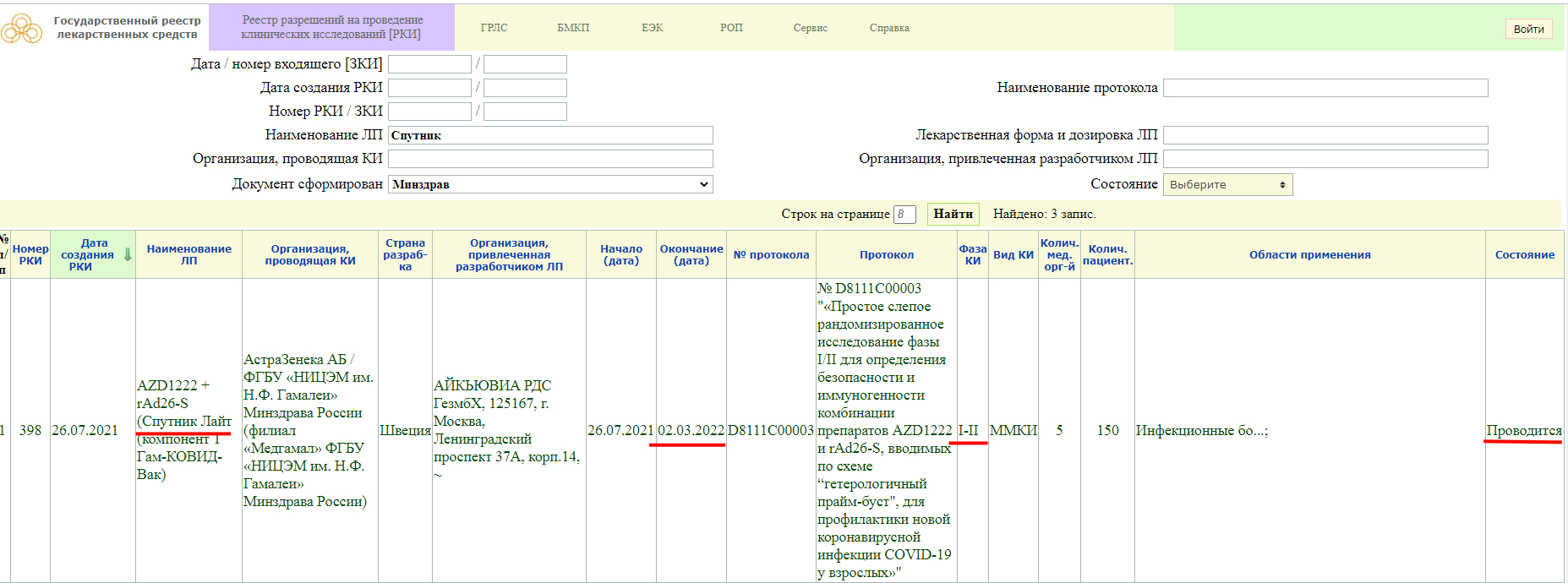
Как мы видим, в настоящий момент, у «Спутника Лайт» проводится фаза клинического исследования 1-2, и завершится она 2 марта 2022 года. Кстати обратите внимание, страна разработки Швеция.
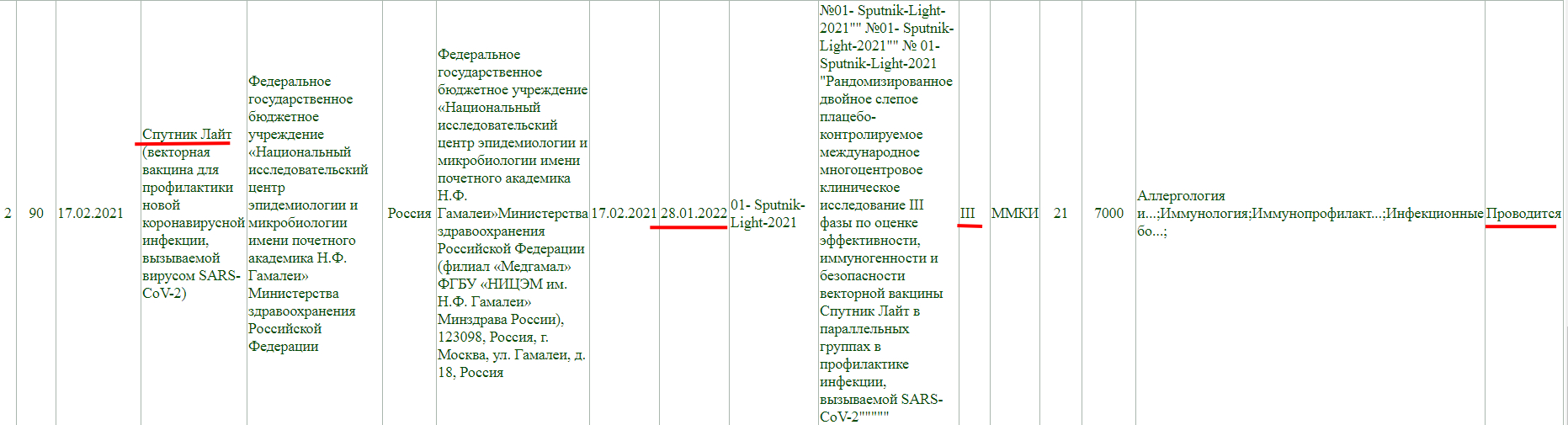
Так же, проводится фаза клинического исследования 3, и завершится она 28 января 2022 года.
Фаза клинического исследования 1-2, проводится до 31 декабря 2021 года.
Как и у остальных, клинические исследования не завершены, и в настоящий момент проводится фаза 3 с участием добровольцев от 18 до 60 лет, а завершится она 30 декабря 2022 года.
Тут аналогично, клинические исследования не завершены, проводится фаза 3-4, и завершится она 30 декабря 2022 года.
А тут клиническое исследование завершено, но только фазы 1-2.
Кроме того, отсутствие данных о клинических испытаниях вакцины «Спутник V» необходимых для ее регистрации в Европе, 15 мая 2021 года, уже сообщало одно из крупнейших в мире международных агентств новостей и финансовой информации, Reuters.
И в завершение, по данным ВОЗ на 14 марта 2021 г., российские вакцины против COVID-19, в перечне безопасных и эффективных, отсутствуют.
Опубликовано видео удара фосфорными боеприпасами ВСУ по военным ДНР на юге республики
Глава Крыма Аксёнов: «Сам получу сертификат фармацевта, надоело враньё»
Житель Екатеринбурга вакцинировался два раза подряд ради QR-кода
Песков назвал слова Мурашко об использовании «Спутника Лайт» только для ревакцинации вырванными из контекста
В России выявили 39 008 новых случаев заражения COVID-19
Путин заявил, что в России складывается сложная ситуация с COVID-19
Гинцбург сообщил об отсутствии нареканий на побочные эффекты у трижды привитых «Спутником V»
Более 25% граждан России прошли вакцинацию от гриппа
Сайт Avia.pro: военные ДНР одним ударом по понтонному мосту у Старомарьевки уничтожили два бронетранспортера ВСУ
В столичном транспорте 1,5 тыс контролеров следят за соблюдением масочного режима
Инфекционист Чуланов заявил, что «Спутник Лайт» не следует применять для первичной вакцинации
На Филиппинах пожар уничтожил почти 150 тысяч доз вакцин против COVID-19
Путин назвал вакцинацию реальным спасением от смерти из-за COVID-19
Российские вакцины не прошли все фазы клинического исследования?
Станьте членом КЛАНА и каждый вторник вы будете получать свежий номер «Аргументы Недели», со скидкой более чем 70%, вместе с эксклюзивными материалами, не вошедшими в полосы газеты. Получите премиум доступ к библиотеке интереснейших и популярных книг, а также архиву более чем 700 вышедших номеров БЕСПЛАТНО. В дополнение у вас появится возможность целый год пользоваться бесплатными юридическими консультациями наших экспертов.
Анализ третьей фазы испытаний Спутник V
Пропагандисты вакцинации стали сыпать цифрами, от которых глаз дёргается, поэтому посмотрела результаты испытаний Спутника, опубликованные в «Ланцете».
На эксперимент заявились 35963 добровольца.
Из них 13986 (38,9%) было отказано.
Не брали с ВИЧ, гепатитом В или С, антителами к ковиду, положительным ПЦР, контактировавших с ковидными, перенесших инфекционные или респираторные заболевания в течение 14 дней до поступления, с наркотиками или алкоголем в крови, беременных, кормящих грудью, отказывающихся предохраняться от беременности на время исследований тем, чем скажут, больных туберкулёзом, перенесших инфаркт или инсульт, принимавших стероиды. и ещё длинный список.
Первый укол получили 21977, из них препарат 16501, плацебо 5476.
Попали в анализ данных 21862 (16427+5435)
Второй укол получили 19866 (14964+4902)
В общий анализ безопасности вошли 12296 (9258+3038)
По результатам всех уколов зафиксировано 7966 «нежелательных событий», из них
68 (45+23) получили серьёзные побочные эффекты, ни один из них не признали связанным с вакцинацией.
С момента получения второй дозы и до 24 ноября (менее чем за 2 месяца) заболели ковидом 78 (16+62) из 19866 (но «нет данных» по 7570 (?))
От всего этого вспомнились «Десять негритят» Агаты Кристи и задёргался второй глаз.
По списку избирателей у нас 108,6 млн. взрослых в стране.
Уколятся первый раз 66,4 млн
Из них 6 млн второй укол делать не станут.
Среди сделавших уколы:
«Нежелательные последствия 1 степени» получат 22,6 млн.
Чтобы понять, много это или мало, посмотрю, сколько бед по статистике принёс сам ковид за время проведения исследования (с 7 сентября по 24 ноября) и поправлю эти цифры на 38,9% которым в прививке будет отказано.
заразились 677 тыс. (всех степеней тяжести)
Теперь могу сравнить образно.
С одной стороны стоят:
205 тыс. с серьёзными побочными эффектами
1,5 млн. с «нежелательными последствиями» хуже 1 степени
22,6 млн. с небольшой температурой
из них считаются заболевшими ковидом 72 тыс.
С другой стороны стоят:
677 тыс. людей с положительными тестами ПЦР и разными состояниями от «бессимптомных» до тяжёлых
А между ними 42,2 млн тех, кому прививку делать нельзя по списку показаний.
The Lancet is an independent, international weekly general medical journal founded in 1823 by Thomas Wakley.
По твоей же ссылке
В ходе исследования было зарегистрировано четыре смерти: трое (
Не рефлексируйте, а распространяйте, классика.
@moderator, а считается ли за вброс и потенциально опасную информацию подобная ахинея от ноунейма с ЖЖ как источник?
Эмм 11,7 мертвых? Откуда вы этот бред взяли?
Хватит всякую пургу постить.
Не будем проверять пока цифры, возьмем только данные из поста. И.
По офиц. данным от ковида, сейчас переболели 5 350 919, умерли 130 347. https://стопкоронавирус.рф/
Я думаю тут более качественный перевод.
«Авторитетный медицинский журнал The Lancet опубликовал итоги третьей фазы испытаний российской вакцины от коронавируса «Спутник V». Она оказалась эффективна на 91,6%, ранее ее создатели заявляли о достижении 95%»
Зачем читать эту галиматью, сейчас главный пропагандист вакцинации это Собянин, который призвал повторно вакцинироваться уже привитых и радостных носителей Спутника. Как ни странно я ему верю, это наверное первое его правдивое заявление во время всей пандемии.
Подождите. Я правильно понял? Если всем (ну или абсолютному большинству) сделать прививки в России, то из-за вакцины умрут 12 тыс чел.
Если я всё правильно посчитал, то сам вирус всего в 5,7 раз смертельнее прививки?
У «Спутника V» завершилась третья фаза испытаний
В журнале «The Lancet» выложена официальная информация:
> В ходе третьей фазы клинических исследований «Спутник V» продемонстрировал высокие показатели эффективности, иммуногенности и безопасности.
> Эффективность вакцины составила 91,6% на основе анализа данных 19866 добровольцев, получивших первую и вторую инъекцию вакцины или плацебо.
На момент достижения финальной контрольной точки было 78 подтвержденных случаев заболевания коронавирусом.
> В то же время эффективность AstraZeneca — 62,1%, Sinovac — 50,4%, Sinopharm — 79,3%.
Сейчас комбинация с одним из двух компонентов «Спутника V» помогает компании AstraZeneca повысить эффективность ее вакцины с 62,1% до более высокого уровня.
> Важным фрагментом исследования стало участие добровольцев старше 60 лет (самому пожилому участнику в группе вакцины было 87 лет, а в группе плацебо – 84 года).
Показатели безопасности для пожилых людей оказались высокими. Эффективность для 2144 добровольцев в возрасте старше 60 лет составила 91,8% и статистически не отличалась от данных, полученных в группе добровольцев 18-60 лет.
> «Согласно рецензируемым результатам исследования, вакцина предоставляет полную защиту от тяжелых случаев заболевания новой коронавирусной инфекцией.
Все 20 подтвержденных тяжелых случаев заболевания коронавирусом были зарегистрированы в группе плацебо и ни одного — в группе получивших вакцину», — подчеркнули в РФПИ.
Российская вакцина от COVID-19 неофициально испытана на людях и дала нужный эффект
Сотрудники национального исследовательского центра эпидемиологии и микробиологии имени Н.Ф.Гамалеи Минздрава России (НИЦЭМ) проверили на себе свою векторную вакцину от COVID-19, и опыт оказался успешным: иммунитет есть, негативных эффектов не обнаружено, сообщил «Интерфаксу» директор центра академик РАН Александр Гинцбург.