аномальная хорда митрального клапана что это значит
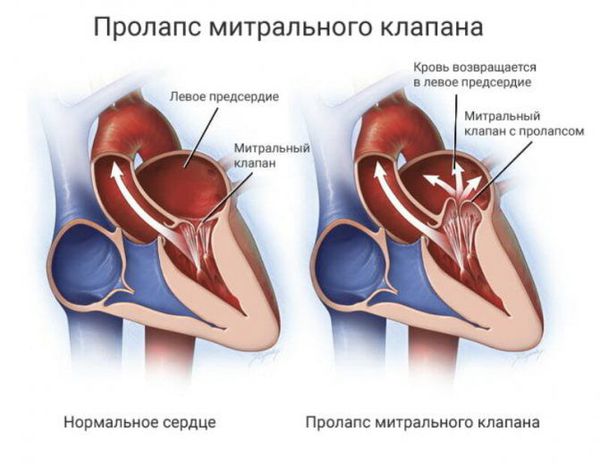
Что такое пролапс митрального клапана? Причины возникновения, диагностику и методы лечения разберем в статье доктора Карченова Е. В., кардиолога со стажем в 37 лет.
Определение болезни. Причины заболевания
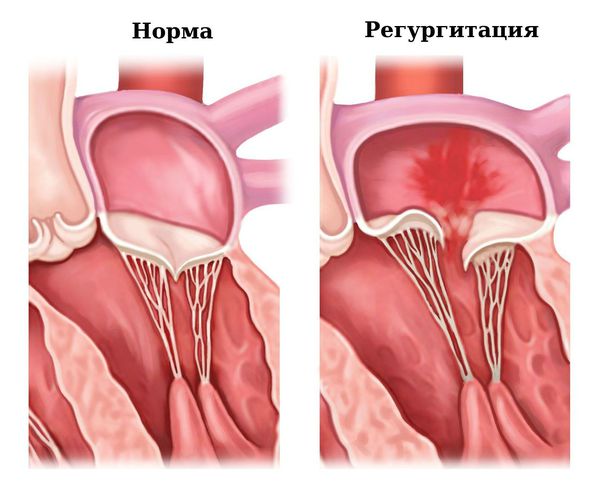
Из предсердий кровь должна поступать в желудочки сердца. Однако при определённой величине прогиба створки возможна митральная регургитация — обратный ток крови из желудочка в предсердие. Это может вызвать увеличение полости предсердия, повышенное гидростатическое давление и нагрузку на него.
Распространённость пролапса митрального клапана
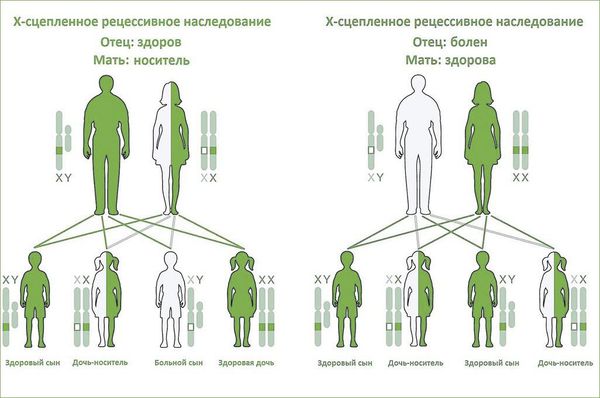
Выделяют первичный (врождённый) пролапс митрального клапана и вторичный (приобретённый). Первичный ПМК бывает семейным (наследственным) или несемейным (случайным).
Причины пролапса митрального клапана
Отмечается увеличение частоты случаев пролапса митрального клапана, ассоциированных со вторичным дефектом межпредсердной перегородки и/или левосторонними атриовентрикулярными дополнительными проводящими путями, а также с наджелудочковыми аритмиями.
Вторичным считают прогиб створки митрального клапана, который возникает в результате воспаления или повреждения окружающих тканей и самого клапана. ПМК вторичной природы может быть следствием различных состояний:
Симптомы пролапса митрального клапана
Болевой синдром в груди чаще сосредоточен в области сердца, бывает длительным, в отличие от стенокардии, он не связан с физической нагрузкой. Пациенты обычно описывают острые, «колющие» боли, однако обычно они не являются предвестниками тяжёлого состояния.
Симптомы врождённого и приобретённого ПМК
При врождённом пролапсе митрального жалоб у пациентов может не быть вовсе или они незначительны и не сильно беспокоят.
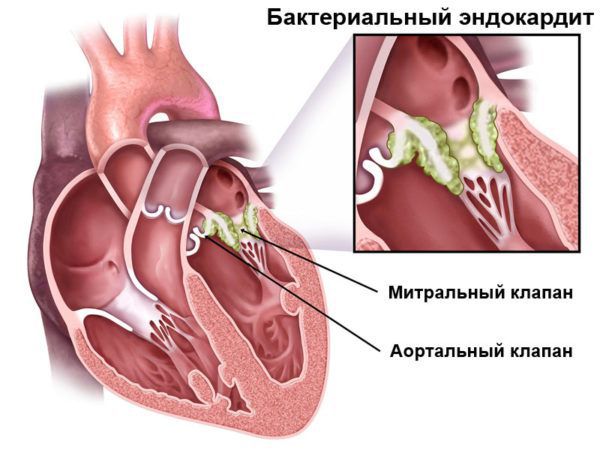
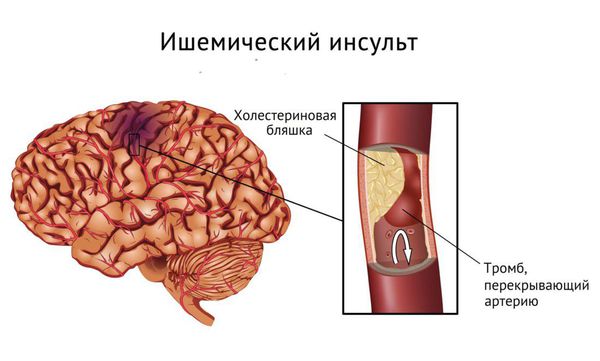
Приобретённый пролапс митрального клапана возникает после тяжёлых заболеваний: ишемической болезни сердца, инфаркта миокарда, ревматических заболеваний сердца, инфекционного септического эндокардита и в редких случаях при травме грудной клетки. Отдельных жалоб из-за пролапса митрального клапана может не быть, но пациента беспокоят симптомы основных болезней, например одышка при небольшой физической нагрузке и отёки.
Симптомы пролапса митрального клапана у детей
Симптомы ПМК у детей те же, что и у взрослых: повышенная утомляемость, психоэмоциональная неустойчивость и ощущение перебоев в работе сердца.
Патогенез пролапса митрального клапана
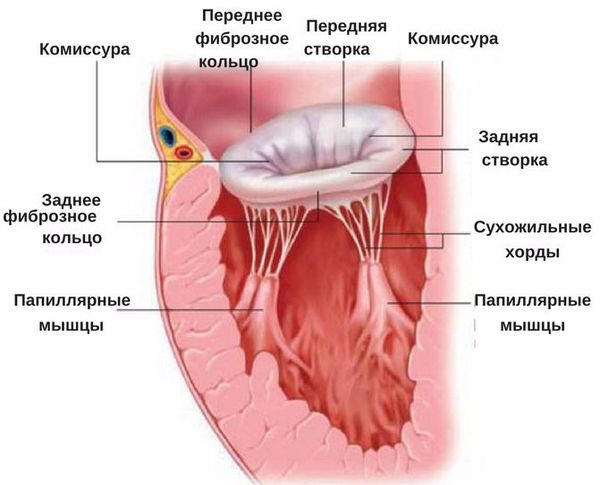
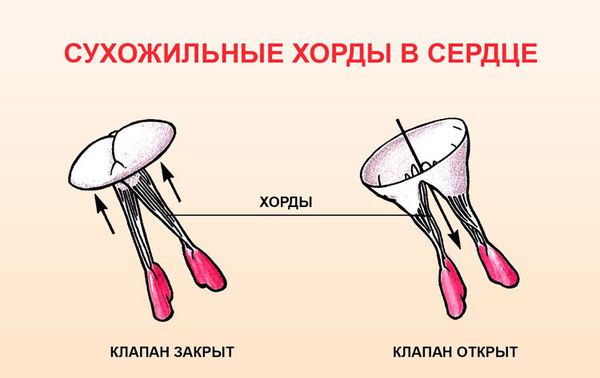
Строение митрального клапана [3] [4]
Многочисленными исследованиями показано, что митральный клапан в норме состоит из трёх зон, расположенных от кольца клапанного отверстия до свободного края клапана:
Механизм развития ПМК различен при первичных и вторичных пролапсах. При первичной патологии прогиб створок митрального клапана происходит из-за избыточности ткани створки и включает в себя как неизменённые, так и деформированные участки створок. Основные особенности внутреннего строения при первичном пролапсе митрального клапана:
Всё это приводит к тому, что в период систолы под влиянием внутрижелудочкового давления створки прогибаются в сторону левого предсердия. По мере взросления человека увеличивается нагрузка на все органы, в том числе и на клапаны сердца. Так как ткани митрального клапана имеют более «хрупкое» строение, у людей с генетически обусловленными особенностями клапан начинает провисать, хорды, которые его удерживают, утолщаются или удлиняются. В результате кровь движется в обратном направлении (регургитация) из желудочка в предсердие.
В связи с вегетативной дисфункцией ( нарушением регулирования сосудистого тонуса) у пациентов появляются боли в области сердца, нарушения ритма, нестабильное артериальное давление, липотимии (предвестники обмороков — слабость, бледность, нарушение потоотделения), гипервентиляционный (одышка) и астенический синдромы.
При вторичном пролапсе имеется поверхностный фиброз (уплотнение, рубцевание) створок клапана, истончение и/или удлинение хорд и нарушение желудочковой жёсткости. При этом сами «листочки» клапана теряют эластичность из-за недостатка фиброэластина. Уплотняется мышечное кольцо клапана, в результате чего размер отверстия и площадь створок клапана перестают совпадать. Это приводит к обратному «забросу» крови, недостаточности митрального клапана, от степени которой зависит состояние и самочувствие человека.
Классификация и стадии развития пролапса митрального клапана
Пролапс классифицируют по степени прогиба (пролапса) створок клапана:
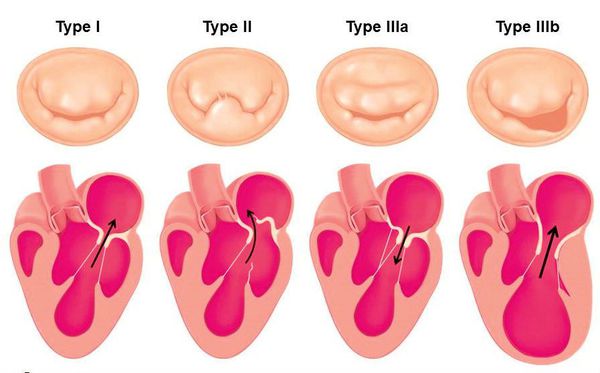
На прогноз клинического течения пролапса митрального клапана влияет наличие и степень митральной регургитации. Согласно Клиническим рекомендациям, утверждённым Министерством здравоохранения Российской Федерации в 2016 году, для оценки типа и степени митральной регургитации применяется анатомо-функциональная классификация по Карпантье [12] :
Тип I. Нормальная подвижность створок:
Тип II. Прогибание створок:
Тип III. Ограничение подвижности створок.
Тип IIIА. Нормальные сосочковые мышцы:
Тип IIIБ. Аномалия сосочковых мышц:
При пролапсе митрального клапана может развиваться митральная недостаточность. Она бывает первичной и вторичной:
В зависимости от степени регургитации выделяют 4 степени митральной недостаточности:
Диагностируют и оценивают степень тяжести регургитации при проведении эхокардиографии с помощью специальных программ.
Осложнения пролапса митрального клапана
Наиболее тяжёлыми осложнениями пролапса митрального клапана являются:
Несмотря на то, что у мужчин пролапс митрального клапана встречается реже, тяжесть осложнений этого заболеваний у них более выражена. Этот факт требует дальнейшего изучения, так как его причина неизвестна.
Диагностика пролапса митрального клапана
Критерии постановки диагноза
Пролапс митрального клапана чаще всего диагностируется неинвазивными методами обследования — врач учитывает жалобы пациента и наследственность. Но окончательный диагноз устанавливается с помощью трансторакальной эхокардиографии.
Инструментальные методы диагностики
При аускультативном обследовании (выслушивании сердца) с помощью стетоскопа врач может услышать характерный систолический щелчок и/или поздний систолический шум над верхушкой сердца. В положении пациента стоя систолические щелчок и шум появляются в начале систолы (сокращения). В положении пациента лежа или сидя на корточках эти звуковые феномены уменьшаются.
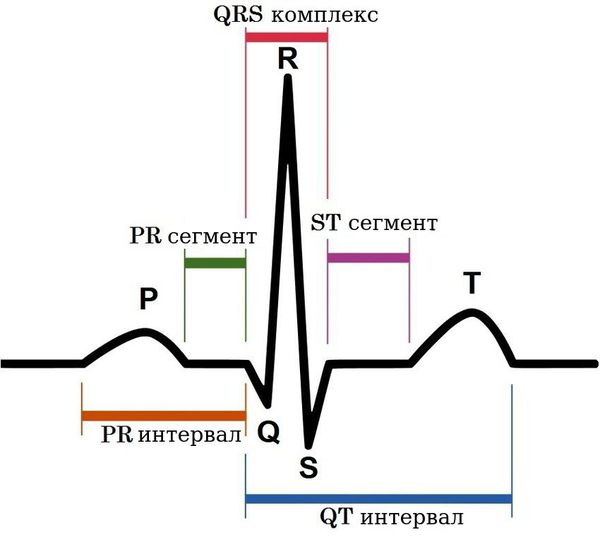
На электрокардиограмме можно обнаружить неспецифические изменения сегмента ST и зубца Т в отведениях III и aVF. При наличии пролапса митрального клапана на ЭКГ можно диагностировать феномен предвозбуждения («синдром укороченного PQ»), наджелудочковые (предсердные) тахикардии, желудочковую экстрасистолию.
Рентгенограмма грудной клетки может быть вариантом нормы или обнаружить признаки сглаженного лордоза («прямая спина»). Расширение сердца может быть диагностировано у некоторых больных с очень маленьким переднезадним размером грудной клетки.
Трансторакальная эхокардиография ( Эхо-КГ). Проводится с помощью ультразвукового датчика, поставленного врачом на определённые точки грудной клетки. Является самым важным рутинным методом обследования в диагностике пролапса митрального клапана. К отличительным и важным эхокардиографическим признакам данной патологии относят прогиб задней или обеих створок митрального клапана в полость левого предсердия в середине систолы, в позднюю систолу или во всю систолу. Чаще встречается прогиб (провисание) митрального клапана в середине систолы, что соответствует данным, получаемым при аускультации и при ангиографии.
Существуют и другие эхокардиографические признаки, они неспецифические, но высокочувствительные:
Трансторакальную эхокардиографию рекомендуется проводить каждые 6-12 месяцев всем бессимптомным пациентам с умеренной или тяжёлой митральной регургитацией. Это необходимо, чтобы оценить фракцию выброса (насосную функцию сердца, в норме она должна быть не менее 55 %) и конечный систолический размер.
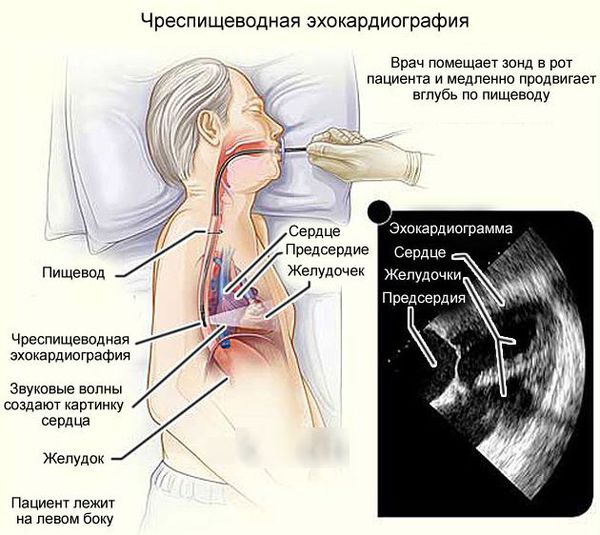
Чреспищеводная эхокардиография. Это ультразвуковое исследование, при котором датчик вводится в пищевод. Показано только при отсутствии противопоказаний в следующих случаях:
Разновидностью пролапса является так называемый болтающийся клапан (floppy mitral valve). Обычно он обнаруживается при разрыве хорд или отрыве папиллярной мышцы (чаще встречается при остром инфаркте миокарда). При эхокардиографии в В-режиме отчётливо видно свободно перемещающуюся сосочковую мышцу и «болтающуюся» створку митрального клапана. Створка совершает неправильные, произвольные движения в диастолу (период расслабления сердечной мышцы) и «проваливается» в полость левого предсердия в систолу желудочков. В М-режиме характерными эхокардиографическими признаками такого клапана является наличие:
Радионуклидная равновесная вентрикулография проводится для оценки фракции выброса и оценки степени тяжести сердечной недостаточности. Метод основан на внутривенном введении радионуклида с фиксацией его на эритроцитах крови и последующей количественной оценкой сократительной способности сердца.
Дифференциальная диагностика
Стратегия и тактика ведения пациента зависит от происхождения пролапса — врождённый он или приобретённый, поэтому дифференциальная диагностика проводится только между этими типами пролапса митрального клапана.
Лечение пролапса митрального клапана
При неосложнённом пролапсе митрального клапана лечение в большинстве случаев не требуется. В том числе лечение не назначают при колющих болях в области сердца и простых аритмиях. Пациенту рекомендуется обычный образ жизни, регулярные физические нагрузки, клинический контроль каждые 3-5 лет. Полезными аэробными нагрузками являются плавание, ходьба в быстром темпе, особенно «скандинавская», лыжи и велосипед.
В каких случаях требуется лечение ПМК
Медикаментозное лечение пролапса митрального клапана назначается при определённых клинических проявлениях. Больному с приступами сердцебиения, влияющими на функцию сердца, можно назначить препарат из группы β-адреноблокаторов. Если при перемене положения тела случаются потери сознания (ортостатические коллапсы), советуют увеличить количество жидкостей и соли.
Больному с перенесённой транзиторной ишемической атакой и ишемической болезнью сердца рекомендуется профилактическая доза ацетилсалициловой кислоты (выбирается лечащим врачом).
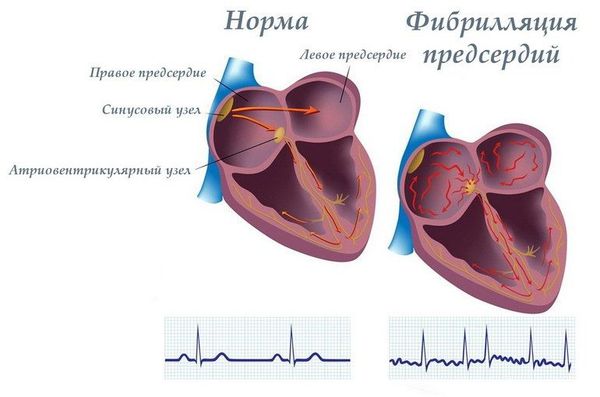
Больным с тяжёлой митральной недостаточностью и фибрилляцией предсердий (мерцательной аритмией) рекомендуется назначение противосвёртывающей (антикоагулянтной) терапии, рассматривается способ хирургического лечения ПМК.
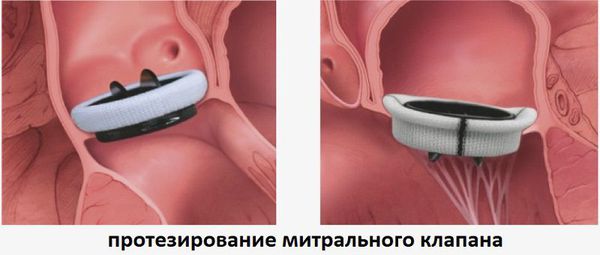
При тяжёлой митральной недостаточности, которая чаще всего возникает при растяжении или отрыве хорд митрального клапана, проводится реконструктивное хирургическое лечение. Операция, как правило, восстанавливает рабочие функции сердца. Хирургическое вмешательство на митральном клапане зависит от особенностей работы сердца у конкретного пациента и состояния его клапана. Возможно проведение реконструкции митрального клапана, протезирования клапана с сохранением части или всего митрального аппарата и протезирование с удалением митрального аппарата.
Людям с высоким операционным риском проводится полностью эндоскопическая клапаносохраняющая операция (т. е. без разреза на грудной клетке, через сосуды) с помощью инновационной технологии 3D-визуализации (в России — с 2018 года, НМИЦ им. акад. Е. Н. Мешалкина).
Как лечить ПМК при дисплазии соединительной ткани
Пациентам следует принимать курсами препараты, которые стимулируют образование коллагена: аскорбиновую кислоту, витамины группы В, магний оротат (но его не назначают пациентам младше 16 лет), хондропротекторы, некоторые БАДы и препараты с фосфорными соединениями.
Прогноз. Профилактика
Прогноз заболевания в целом благоприятный, однако важным является клиническое наблюдение за пациентами. Целью динамического клинического наблюдения является оценка степени недостаточности митрального клапана.
При отсутствии митральной недостаточности и бессимптомном течении достаточно повторять допплерэхокардиографию каждые 3-5 лет.
Пациентам, у которых есть выраженная митральная регургитация, миксоматозная дегенерация, увеличение створок, удлинение хорд, фракция выброса левого желудочка менее 50 %, необходимо каждые 6 месяцев проводить ЭКГ и эхокардиографию, а также мониторирование ЭКГ по Холтеру. При необходимости выполняется чреспищеводная эхокардиография.
Наличие пролапса митрального клапана часто не нарушает физическую выносливость, поэтому среди людей с пролапсом митрального клапана и гипермобильными суставами можно встретить известных спортсменов, цирковых акробатов, артистов балета.
Однако не всем людям с ПМК разрешены занятия спортом. Спортивные нагрузки не рекомендуются больным с пролапсом митрального клапана, у которых выявлено более одного из следующих признаков:
Таким лицам можно рекомендовать аэробные нагрузки, бильярд, гольф, боулинг и стрельбу.
Может ли измениться прогноз при ПМК
Прогноз может ухудшиться при чрезмерных физических нагрузках и частых нелеченых инфекциях. В результате степень пролапса может усилиться и появляются признаки сердечной недостаточности.
Беременность при ПМК
МАРС – синдром. Диагноз как название планеты.
В Беларуси в последние годы наблюдается увеличение числа детей с МАРС. Это обусловлено в первую очередь широким внедрением в практику детских врачей кардиологов ультразвукового исследования сердца.
Многие родители начинают волноваться, когда слышат, что их ребенку выставлен диагноз – МАРС. В популярной литературе об этом синдроме практически нет информации в доступной форме. Теперь попробуем разобраться в этом синдроме, ответив на самые распространенные вопросы, которые задают родители врачу кардиологу на приеме.
Что такое МАРС?
Малые аномалии развития сердца (или МАРС) – это одно из проявлений не совсем правильного развития соединительной ткани. Соединительная ткань находится во всех органов. Она формирует каркас сердца, клапаны и стенки крупных сосудов. За счет этого ткань сердце эластична, но довольно прочная. Малыми аномалиями развития сердца считают наличие анатомических врожденных изменений сердца и его крупных сосудов. При таком состоянии соединительная ткань или слишком слабая, или формируется в избытке, не в тех местах, где надо в норме. МАРС в основном выявляется у детей в первые 2 – 3 года жизни и не имеет тенденции к прогрессированию. Многие МАРС исчезают с ростом ребенка.
Причины развития МАРС?
Какие аномалии сердца встречаются у детей
Наиболее известная и распространенная МАРС – это пролапс митрального клапана (ПМК). ПМК – это провисание двустворчатого клапана в момент сокращения сердца в полость левого желудочка, за счет чего и возникает небольшое завихрение тока крови в сердце. К МАРС относят только первую степень пролапса. Все остальные степени сопровождаются выраженными нарушениями кровообращения и должны считаться пороками сердца.
Довольно распространенная вторая МАРС, это дополнительные хорды в полости левого желудочка (ДХПЛЖ) или по-другому аномальные хорды (АРХ ЛЖ). Эта МАРС, которая проявляется в наличии внутри полости желудочка дополнительных тяжей из соединительной ткани или мышц, прикрепленных к стенкам желудочка или межжелудочковой перегородке. В норме они прикрепляются к створкам клапанов. Чаще всего ложные (дополнительные) хорды встречаются у мальчиков. Ложные хорды бывают единичными, множественными, встречаются как отдельно, так и в сочетании с другими аномалиями. Расположение может быть вдоль тока крови, поперек его или по диагонали. От этого будет зависеть степень выраженности шума в сердце. Хорды могут давать нарушение ритма, поэтому пациенты требуют особого наблюдения врача кардиолога.
Третьей распространенной МАРС является открытое овальное окно (ООО). Вариантом нормы считается наличие незначительного дефекта до 2 – 3 мм в возрасте до года. Но при его наличии в старшем возрасте в одних случаях идет речь об аномалии развития (при размере дефекта до 5 мм), в других – о пороках сердца (когда дефект выражен и имеется нарушение кровообращения).
Как себя проявляет МАРС?
В большинстве случаев МАРС никак себя не проявляет, и дети ничем не отличаются от сверстников. Очень редко, но могут быть жалобы на боли в области сердца, чувство перебоев в сердце, скачки артериального давления, аритмии на электрокардиограмме.
Очень часто аномалии сердца сочетаются с другими аномалиями соединительной ткани: зрения, скелета, кожи, желчного пузыря, почек. Поэтому и проявления будут системными, то есть на уровне всего организма. Эти изменения могут быть как минимальными, так и достаточно выраженными.
Какие могут быть осложнения?
Не всегда, но в отдельных случаях могут отмечаться нарушения сердечного ритма, нарушения проведения импульса по сердцу, которые выявляются на электрокардиограмме и сопровождаются жалобами на боли в сердце, сердцебиение. Это требует дополнительного обследования у врача кардиолога. Как правило, эти нарушения характерны для пролапсов митрального клапана (ПМК) и аномально расположенных хорд.
Какое лечение данного синдрома?
Основные принципы лечения детей с МАРС это:
Резюме
УЗ «11-ая городская детская поликлиника»
Врач кардиолог, к. м. н. Бандажевская Г.С.
Клиническое значение малых аномалий развития сердца у детей
В последние годы большое внимание уделяется дисплазии соединительной ткани (ДСТ) у детей. Под ДСТ понимают врожденную аномалию соединительно-тканной структуры различных органов и систем, в основе которой лежит снижение содержания отдельных
В последние годы большое внимание уделяется дисплазии соединительной ткани (ДСТ) у детей. Под ДСТ понимают врожденную аномалию соединительно-тканной структуры различных органов и систем, в основе которой лежит снижение содержания отдельных видов коллагена и/или нарушение их соотношения, приводящее к снижению прочности соединительной ткани [12, 13, 24, 26].
В развитии ДСТ принимают участие эндогенные (хромосомные и генетические дефекты) и экзогенные (неблагоприятная экологическая обстановка, неадекватное питание, стрессы) факторы [12, 30, 43]. Особенность морфогенеза соединительной ткани заключается в том, что она участвует в формировании каркаса сердца практически на всех этапах онтогенеза, следовательно, влияние любого повреждающего фактора может привести к развитию ДСТ сердца [15].
В 1990 г. в классификации заболеваний сердечно-сосудистой системы Нью-Йоркской ассоциации кардиологов, а также в Омске, на симпозиуме, посвященном проблеме дисплазии соединительной ткани, был впервые выделен синдром ДСТ сердца, сопровождающий как дифференцированные, так и недифференцированные ДСТ. При синдроме ДСТ сердца в патологический процесс вовлекается его соединительно-тканный каркас — сердечные клапаны (атриовентрикулярные, полулунные, евстахиев клапан), подклапанный аппарат, перегородки сердца и магистральные сосуды.
В клинической практике, когда речь идет о морфологической основе изменений сердечно-сосудистой системы без гемодинамических нарушений, Ю. М. Белозеровым (1993) и С. Ф. Гнусаевым (1995) вместо термина «ДСТ сердца» был предложен другой — «малые аномалии развития сердца» (МАРС) [3, 8]. Согласно определению этих авторов, МАРС считаются анатомические изменения архитектоники сердца и магистральных сосудов, не приводящие к грубым нарушениям функций сердечно-сосудистой системы [9].
Классификация МАРС по С. Ф. Гнусаеву, 2001 (с изменениями)
предсердия и межпредсердная перегородка: пролабирующий клапан нижней полой вены, увеличенный евстахиев клапан более 1 см, открытое овальное окно, небольшая аневризма межпредсердной перегородки, пролабирующие гребенчатые мышцы в правом предсердии;
трикуспидальный клапан: смещение септальной створки в полость правого желудочка в пределах 10 мм, дилатация правого атриовентрикулярного отверстия, пролапс трикуспидального клапана;
легочная артерия: дилатация ствола легочной артерии, пролапс створок;
аорта: погранично узкий и широкий корень аорты, дилатация синуса Вальсальвы, двустворчатый клапан аорты, асимметрия и пролапс створок клапана аорты;
левый желудочек: трабекулы (поперечная, продольная, диагональная), небольшая аневризма межжелудочковой перегородки;
митральный клапан: пролапс митрального клапана, эктопическое крепление хорд, нарушенное распределение хорд передней и (или) задней створки, «порхающие» хорды, дополнительные и аномально расположенные папиллярные мышцы.
До сих пор нет единого мнения о клиническом значении МАРС, многие из которых имеют нестабильный характер, связанный с ростом ребенка. Так, возможно обратное развитие увеличенного евстахиева клапана, пролабирующих гребенчатых мышц в правом предсердии, пролапса митрального клапана (ПМК), закрытие открытого овального окна, нормализация длины хорд митрального клапана и диаметра магистральных сосудов. В ряде случаев МАРС изменяются не только в качественном, но и в количественном отношении [3]. Превышение установленного порогового уровня сердечной стигматизации у здоровых детей (более 3 МАРС), по мнению С. Ф. Гнусаева (1995), свидетельствует о возможном неблагополучии как в отношении факторов, влияющих на формирование здоровья, так и показателей, характеризующих его [8].
Учитывая, что МАРС являются вариантом висцеральных ДСТ, дети, как правило, имеют выраженный полиморфизм клинико-морфологических нарушений, зависящий от степени ДСТ и вовлечения в патологический процесс других органов и систем. Выявлена ассоциативная связь между числом внешних фенотипических маркеров ДСТ и МАРС [12, 16, 21, 22]. При этом имеют значение не только число внешних фенотипических маркеров, но и «диагностический вес» каждого из них. Отмечено, что дисплазии кожи и скелета наиболее часто сочетаются с МАРС [12].
Клиническая значимость патологии соединительной ткани у лиц с ДСТ подтверждается данными о высокой частоте нейровегетативных расстройств, изменений центральной нервной системы (энурез, дефекты речи, вегетососудистая дистония (ВСД)), нарушений психики [5, 12, 24]. Как правило, у таких пациентов всегда выявляется ВСД, что, вероятно, обусловлено наследуемыми (наследственными) особенностями структуры и функции лимбико-ретикулярного комплекса, определяющими аномальный характер нейровегетативных реакций [12]. Е. В. Буланкиной (2002) установлена отчетливая взаимосвязь между вегетативной дисфункцией и ДСТ [4]. При этом выраженность диспластических изменений сочеталась с тяжестью процессов дезадаптации регуляторных механизмов и снижением стрессовой устойчивости организма. Наиболее распространенными проявлениями вегетативной дисфункции являются цефалгии, вегетативные кризы, вегетовисцеральные пароксизмы, пре- и синкопальные состояния [12, 16]. Согласно данным С. Ф. Гнусаева (1995), у лиц с ПМК выявлена недостаточность сегментарных вегетативных структур [8]. Исследования Т. М. Домницкой (2000) позволили установить прямую зависимость между ПМК, аномально расположенными трабекулами (АРТ) и распространенностью невротических (невротические реакции, невроз навязчивых состояний, панические расстройства) и энцефалопатических (церебрастенический синдром, заикание, тики, нарушения сна, энурез, гипердинамический синдром, страхи) расстройств [10].
Нередко МАРС сопровождают такие патологические состояния, как нарушения сердечного ритма и проводимости, в том числе синдром ранней реполяризации, синдром слабости синусового узла, синдром Вольф–Паркинсон–Уайта, повышение электрической активности левого желудочка, блокада правой ножки пучка Гиса, экстрасистолия и пароксизмальная тахикардия [4, 6, 8, 34]. По данным Л. А. Балыковой и соавт. (2002), у 90% больных с нарушениями сердечного ритма с помощью эхографии были выявлены МАРС (преимущественно ПМК) [2]. Однако не все МАРС сопровождаются нарушениями сердечного ритма и (или) могут являться их причиной. К аритмогенным МАРС относятся фиброзно-мышечные аномально расположенные хорды (АРХ) и АРТ, ПМК и пролапс трикуспидального клапана (ПТК), аневризма межпредсердной перегородки, увеличенный и/или пролабирующий евстахиев клапан.
Наличие проводящих кардиомиоцитов в фиброзно-мышечных АРХ и АРТ формирует дополнительные проводящие пути, чем объясняется происхождение импульса, опережающего внутрижелудочковое проведение и вызывающего раннее возбуждение прилежащих к нему сегментов с последующей их более ранней реполяризацией [12, 15, 19, 20, 28]. Имеется гистологическое подтверждение наличия проводящих клеток в АРТ с диагонально-базальной, срединно-поперечной и продольной локализацией и в АРХ, соединяющих базальные септальные отделы и боковую стенку левого желудочка [3, 10, 33]. M. Suwa и соавт. (1986) отметили возрастание частоты желудочковых экстрасистол с увеличением толщины хорды. По мнению E. Chesler и соавт. (1983), появление желудочковых экстрасистол связано с миксоматозно измененными хордами, вызывающими механическое раздражение стенки левого желудочка [27]. Факт аритмогенности АРХ и АРТ также подтверждается исчезновением у пациентов экстрасистолии в случае их самостоятельного разрыва или оперативного рассечения либо при физической нагрузке, когда уменьшается степень их натяжения [8, 10, 12]. Довольно распространенным нарушением сердечного ритма при АРХ и АРТ является и синдром раннего возбуждения желудочков [6, 12].
Аритмии при ПМК и ПТК, по данным разных авторов, встречаются от 15 до 90% случаев [11]. Среди причин аритмий рассматриваются вегетативные дисфункции, механическая стимуляция эндокарда, дефицит внутритканевого магния, психологический стресс и миксоматозная дегенерация створок клапанов [3, 10–12, 18, 27, 29, 37, 39]. Установлена прямая корреляционная зависимость между частотой, а также степенью тяжести нарушений ритма и глубиной ПМК [1]. Ряд авторов полагают, что причиной развития аритмий при ПМК и ПТК может являться турбулентный поток, возникающий в результате регургитации через клапанное кольцо во время систолы желудочков, особенно при ПТК, когда происходит механическое раздражение зоны синусового узла [3, 8, 23]. Возможным механизмом развития желудочковых экстрасистол при ПМК большинство исследователей считают избыточное натяжение папиллярных мышц вследствие их аномальной тракции при пролабировании створок [12, 14, 25, 38].
Развитие аритмий может провоцировать пролабирующий евстахиев клапан и аневризма межпредсердной перегородки: условия для возникновения аритмий возникают в результате их холмистых движений и рефлекторного раздражения ими пейсмекерных образований в правом предсердии [42].
Согласно исследованиям О. А. Дианова (1999), нарушения сердечного ритма встречались у детей с погранично узкой аортой, у которых в 32,4% случаев регистрировалась суправентрикулярная и в 10,8% — желудочковая экстрасистолии, свидетельствующие о декомпенсации адаптации, особенно в условиях физической нагрузки [4].
По данным Ю. М. Белозерова, дети с МАРС отличаются сниженными возможностями кардиогемодинамики и демонстрируют плохую переносимость физических нагрузок [3]. По данным Н. А. Мазура, установлена связь между ПМК и синдромом внезапной смерти у взрослых. Накоплено достаточно сведений о том, что дети с МАРС относятся к группе риска по развитию инфекционного эндокардита.
Таким образом, существующие результаты исследований о том, что МАРС в ряде случаев являются основой кардиоваскулярной патологии у детей. В то же время неоправданным было бы преувеличение их роли в функциональных нарушениях сердечно-сосудистой системы. Очевидно, в каждом конкретном случае значимость структурных аномалий сердца должна рассматриваться индивидуально.
Принципы терапии детей с МАРС еще до конца не сформулированы. Однако на сегодняшний день можно предложить следующую тактику ведения детей с МАРС:
Общепризнанным является применение немедикаментозных методов лечения, включающих:
Вопрос о допуске к занятиям спортом решается индивидуально. При наличии ПМК необходимо учитывать семейный анамнез (случаи внезапной смерти у родственников), наличие жалоб на сердцебиения, кардиалгии; синкопальные состояния; изменения на ЭКГ (нарушения сердечного ритма, синдром укороченного и удлиненного QT) являются основанием для принятия решения о противопоказании спортивных тренировок. Это касается и наличия АРХ, АРТ с синдромом раннего возбуждения желудочков, которые, являясь аритмогенными МАРС, могут спровоцировать нарушения сердечного ритма у спортсменов в условиях физического и психоэмоционального напряжения.
Медикаментозное лечение включает применение:
В настоящее время терапия препаратами магния при МАРС приближается к патогенетической. Это обусловлено тем, что магний входит в состав основного вещества соединительной ткани и необходим для правильного формирования волокон коллагена. В условиях магниевой недостаточности нарушается способность фибробластов продуцировать коллаген [29, 31]. Кроме того, магний оказывает мембраностабилизирующее действие, удерживает калий внутри клетки, препятствует симпатикотоническим влияниям, что делает возможным его применение для лечения нарушений сердечного ритма [40, 41].
В работах О. Б. Степуры (1999), О. Д. Остроумовой и соавт. (2004) имеются сведения о достоверном уменьшении степени ПМК, симптомов ВСД, количества желудочковых экстрасистол на фоне терапии препаратами магния [17, 18].
Целесообразным может быть признано назначение следующих препаратов:
Магнерота, содержащего соль магния и оротовую кислоту. Последняя не только усиливает реабсорбцию Mg в кишечнике, но и обладает самостоятельным метаболическим действием. Детям назначают по 500 мг магнерота (32,8 мг магния 3 раза в день в течение 1 нед, затем 250 мг 3 раза в день в течение последующих 5 нед. Принимается препарат за 1 ч до еды).
Магне В6. Выпускается в таблетках (48 мг магния или в растворе для приема внутрь (100 мг магния). Детям с массой тела более 10 кг (старше 1 года) — 5–10 мг/кг/сутки в 2–3 приема. Детям старше 12 лет — 3–4 табл. в сут, в 2–3 приема. Продолжительность курса 6–8 нед.
Калия оротата. Детям препарат назначают из расчета 10–20 мг/кг/сут в 2–3 приема за 1 ч до еды или через 4 ч после еды. Продолжительность курса — 1 мес.
Следует проводить повторные курсы терапии этими препаратами (3–4 раза в год).
Для улучшения клеточной энергетикии миокарда применяют препараты, обладающие комплексным влиянием на метаболические процессы в организме, а также являющиеся активными антиоксидантами и мембраностабилизаторами:
Кроме указанных препаратов для улучшения метаболических процессов в соединительной ткани, миокарде и в организме в целом показано применение:
Показаны повторные курсы лечения (до 3 раз в год).
При наличии ВСД проводится комплексная длительная терапия по восстановлению баланса между симпатическим и парасимпатическим отделами вегетативной нервной системы (дифференцированная фитотерапия, вегетотропные препараты, ноотропы, вазоактивные препараты — кавинтон, вазобрал, инстенон, циннаризин и др.).
Таким образом, все вышесказанное позволяет сделать вывод, что МАРС, являясь висцеральным проявлением дисплазии соединительной ткани, составляют морфологическую основу функциональных изменений сердечной деятельности и нейровегетативных расстройств. Выбор индивидуальной программы курсового лечения способствует улучшению обменных процессов в соединительной ткани и профилактирует возможные осложнения ДСТ у детей и подростков.
По вопросам литературы обращайтесь в редакцию.
Н. А. Коровина, доктор медицинских наук, профессор
А. А. Тарасова, кандидат медицинских наук, доцент
Т. М. Творогова, кандидат медицинских наук, доцент
Л. П. Гаврюшова, кандидат медицинских наук, доцент
М. С. Дзис
РМАПО, Москва